
 鐵及其化合物在日常生活中隨處可見.
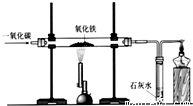
鐵及其化合物在日常生活中隨處可見. 2Fe+3CO2;一氧化碳與氧氣混合在有限的空間內會發生爆炸,故實驗過程中,要先通一氧化碳,后加熱原因就是將玻璃管中的空氣排盡,避免發生爆炸;
2Fe+3CO2;一氧化碳與氧氣混合在有限的空間內會發生爆炸,故實驗過程中,要先通一氧化碳,后加熱原因就是將玻璃管中的空氣排盡,避免發生爆炸; 2Fe+3CO2
2Fe+3CO2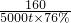 =
=
 2Fe+3CO2;將玻璃管中的空氣排盡,避免發生爆炸;2714.3
2Fe+3CO2;將玻璃管中的空氣排盡,避免發生爆炸;2714.3

科目:初中化學 來源: 題型:

| ||
| ||
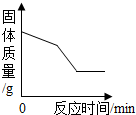 銅的混合溶液,加入一定量的鋅粉,有如圖所示的反應關系.則下列說法正確的是
銅的混合溶液,加入一定量的鋅粉,有如圖所示的反應關系.則下列說法正確的是查看答案和解析>>
科目:初中化學 來源: 題型:
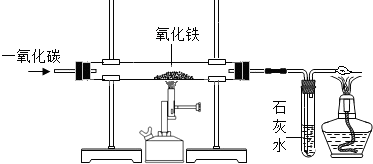 鐵及其化合物在日常生活中隨處可見.
鐵及其化合物在日常生活中隨處可見.
| ||
| ||
查看答案和解析>>
科目:初中化學 來源:2011-2012學年江蘇省南京三中(六中校區)九年級(下))期初考試化學試卷(解析版) 題型:解答題
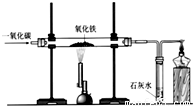
查看答案和解析>>
科目:初中化學 來源:2011-2012學年江蘇省南京市下關區九年級(上)期末化學試卷(樣卷)(解析版) 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com