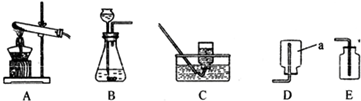
某校化學研究性學習小組的同學對一瓶敞口放置的氫氧化鈉產生了興趣,甲乙兩組同學圍繞這瓶氫氧化鈉進行了一系列的探究活動.
提出問題
提出問題
①氫氧化鈉是否完全變質②樣品中碳酸鈉的質量分數是多少?
查閱資料
查閱資料
①氫氧化鈉與二氧化碳反應生成碳酸鈉和水.
②向氫氧化鈉和碳酸鈉混合物中加入鹽酸時,鹽酸先與氫氧化鈉反應,再與碳酸鈉反應;
設計實驗
設計實驗
實驗一:探究氫氧化鈉固體的變質情況.
①取少量該固體樣品置于試管中,向其中加入稀鹽酸,發現有氣泡產生,說明該樣品中含有碳酸鈉,由此可確定該固體已發生變質.則反應方程式為:
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+2HCl=2NaCl+H2O+CO2↑
.
②如果氫氧化鈉已經完全變質,甲組同學認為取少量固體溶于水,向其中滴加無色酚酞后,溶液應呈無色,乙組同學思考后認為甲組同學的想法是錯誤的,原因是:
碳酸鈉和氫氧化鈉溶液都顯堿性,使酚酞試液變成紅色
碳酸鈉和氫氧化鈉溶液都顯堿性,使酚酞試液變成紅色
.
③為探究該固體中是否還有未變質的氫氧化鈉,同學們又進行了如下表所示的實驗.請將下表填寫完整.
| 實驗目的 |
實驗操作 |
現象 |
結論或化學方程式 |
| 除去碳酸鈉 |
取少量該固體樣品溶于水配成溶液,滴加適量的氯化鈣溶液,充分反應后過濾 |
產生白色沉淀 產生白色沉淀 |
有關反應的化學方程式為
Na2CO3+CaCl2=2NaCl+CaCO3↓ Na2CO3+CaCl2=2NaCl+CaCO3↓ |
| 檢驗是否含有氫氧化鈉 |
向過濾后的濾液中滴入 酚酞試液 酚酞試液 |
變紅 變紅 |
該樣品中含有氫氧化鈉 |
實驗二:測定其中碳酸鈉的質量分數
設計方案
設計方案
①甲組同學:稱取20.00樣品,放入過量的鹽酸直到反應停止,共收集到4.40g二氧化碳.(設計思路:根據樣品與鹽酸反應生成二氧化碳的質量求出碳酸鈉的質量,再計算樣品中碳酸鈉的質量分數.)
②乙組同學:稱取20.00g樣品,加水配成溶液,向溶液中加入過量的澄清石灰水.過濾、洗滌、干燥,共得到白色沉淀10.00g.(設計思路:根據樣品與石灰水反應生成沉淀碳酸鈣的質量,先求出碳酸鈉的質量,再計算樣品中碳酸鈉的質量分數.)
解決問題
解決問題
根據兩組同學的實驗結果,請你幫助他們計算出樣品中碳酸鈉的質量分數:(任選一組寫出計算過程)
交流與反思
交流與反思
(1)在交流時,老師問同學們“能否用上述實驗所得的數據計算出樣品中氫氧化鈉的質量分數”,甲乙兩組的同學都一致認為可以.但小明思考后,覺得甲、乙兩種方案都不妥,理由是:
樣品中有水,無法測出樣品的氫氧化鈉的質量
樣品中有水,無法測出樣品的氫氧化鈉的質量
.
(2)小明又重新設計新方案:先用電子秤準確稱取20.00g變質的NaOH樣品放入錐形瓶中,用電子秤秤得錐形瓶及樣品的總質量為70.00g,再把175.00g7.3%稀鹽酸平均分成7份依次加入樣品中,每次充分反應用電子秤秤得錐形瓶及所盛物質的質量,實驗數據記錄如下:
| 加入鹽酸的次數 |
第一次 |
第二次 |
第三次 |
第四次 |
第五次 |
第六次 |
第七次 |
| 錐形瓶及所盛物質的總質量 |
95.00 |
120 |
145 |
170 |
192.8 |
215.6 |
240.6 |
(2)請根據上述實驗數據,計算樣品中氫氧化鈉的質量分數為
40.0%
40.0%
(不要寫出計算過程)



 新題型全程檢測期末沖刺100分系列答案
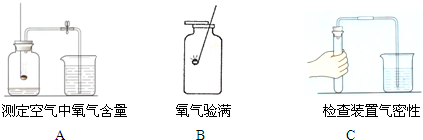
新題型全程檢測期末沖刺100分系列答案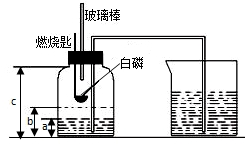 某校化學研究性學習小組在學習了“空氣中氧氣含量測定”的基礎上,改進了教材中的實驗,設計出了如圖所示的實驗裝置.實驗步驟如下:
某校化學研究性學習小組在學習了“空氣中氧氣含量測定”的基礎上,改進了教材中的實驗,設計出了如圖所示的實驗裝置.實驗步驟如下: