
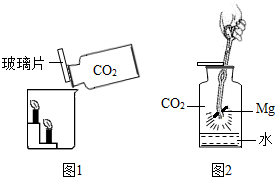
 (2012?東城區二模)(1)小方用如圖1所示裝置對二氧化碳的滅火實驗進行研究,觀察到的現象是
(2012?東城區二模)(1)小方用如圖1所示裝置對二氧化碳的滅火實驗進行研究,觀察到的現象是| 實驗步驟 | 實驗現象 | 實驗結論和化學方程式 | |||||||||
| 向廣口瓶中加入過量鹽酸,充分反應后過濾,在濾紙上留有黑色固體. | I、將黑色固體收集、洗滌、干燥后,點燃,在火焰上方罩一個蘸有澄清石灰水的燒杯. | 黑色固體燃燒,燒杯內壁出現白色渾濁. | 黑色固體是 碳 碳 ;反應的化學方程式是C+O2
C+O2 .
| ||||||||
| II、取少量濾液于試管中,逐滴加入氫氧化鈉溶液. | 開始 無明顯現象 無明顯現象 ,后有白色沉淀產生. |
白煙的成分是 氧化鎂 氧化鎂 . | |||||||||
| ||


科目:初中化學 來源: 題型:
| ||
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com