
將硫酸鈉和氯化鈉的固體混合物35克放入燒杯中,加入161.6克水后,固體混合物完全溶解,取此溶液一半,加入75克氯化鋇溶液恰好完全反應,生成沉淀23.3克.計算:
(1)原固體混合物中硫酸鈉的質(zhì)量分數(shù)(精確到0.1%).
(2)反應后所得溶液中溶質(zhì)的質(zhì)量分數(shù).
(3)往上述反應后所得溶液中再加50克水后,溶液中溶質(zhì)質(zhì)量分數(shù)是多少?
(1)81.1% (2)10% (3)7.5%
【解析】
試題分析:(1)設原固體混合物中硫酸鈉的質(zhì)量為x,生成的氯化鈉的質(zhì)量為y.
BaCl2+Na2SO4=BaSO4↓+2NaCl
142 233 117
x 23.3g y
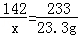
x=14.2g
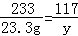
y=11.7g
原固體混合物中硫酸鈉的質(zhì)量分數(shù)=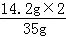 ×100%=81.1%
×100%=81.1%
(2)反應后所得溶液中溶質(zhì)質(zhì)量=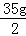 ﹣14.2g+11.7g=15g
﹣14.2g+11.7g=15g
反應后所得溶液的質(zhì)量=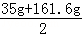 +75g﹣23.3g=150g
+75g﹣23.3g=150g
反應后所得溶液中溶質(zhì)的質(zhì)量分數(shù)= ×100%=10%
×100%=10%
(3)反應后所得溶液中再加50克水后,溶液中溶質(zhì)質(zhì)量分數(shù)=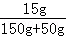 ×100%=7.5%
×100%=7.5%
答:(1)原固體混合物中硫酸鈉的質(zhì)量分數(shù)為81.1%.
(2)反應后所得溶液中溶質(zhì)的質(zhì)量分數(shù)為10%.
(3)往上述反應后所得溶液中再加50克水后,溶液中溶質(zhì)質(zhì)量分數(shù)是7.5%.
考點:根據(jù)化學反應方程式的計算;有關溶質(zhì)質(zhì)量分數(shù)的簡單計算.
點評:本考點考查了根據(jù)化學方程式的計算,屬于質(zhì)量分數(shù)和化學方程式的綜合應用,是中考計算題中經(jīng)常出現(xiàn)的題型.做題時要注意:化學方程式要寫正確,始終不要忘記質(zhì)量守恒定律.本考點主要出現(xiàn)在計算題中.


科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:
查看答案和解析>>
科目:初中化學 來源: 題型:解答題
查看答案和解析>>
科目:初中化學 來源: 題型:
將硫酸鈉和氯化鈉的固體混合物35克放入燒杯中,加入161.6克水后,固體混合物完全溶解,取此溶液一半,加入75克氯化鋇溶液恰好完全反應,生成沉淀23.3克。計算:
(1)原固體混合物中硫酸鈉的質(zhì)量分數(shù)(精確到0.1%)。
(2)反應后所得溶液中溶質(zhì)的質(zhì)量分數(shù)。
(3)往上述反應后所得溶液中再加50克水后,溶液中溶質(zhì)質(zhì)量分數(shù)是多少?

查看答案和解析>>
國際學校優(yōu)選 - 練習冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com