

 ,解得x≈14.5%
,解得x≈14.5%

科目:初中化學 來源:不詳 題型:實驗題


| 步驟③現象 | 步驟⑥結果 | 步驟⑦現象 | 結論 |
| 溶液中 , 帶火星的木條復燃。 | | 溶液中有氣泡放出, 。 | 猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立。 |


查看答案和解析>>
科目:初中化學 來源:不詳 題型:實驗題
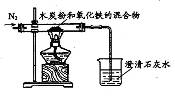
查看答案和解析>>
科目:初中化學 來源:不詳 題型:問答題
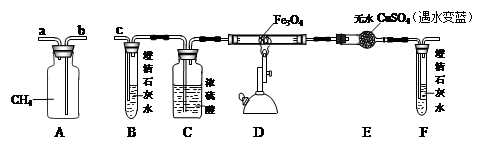
查看答案和解析>>
科目:初中化學 來源:不詳 題型:實驗題

查看答案和解析>>
科目:初中化學 來源:不詳 題型:實驗題
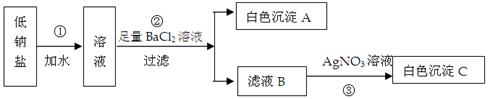
查看答案和解析>>
科目:初中化學 來源:不詳 題型:實驗題

查看答案和解析>>
科目:初中化學 來源:不詳 題型:實驗題
| 實驗操作 | 實驗現象 | 結論 |
| 用試管取該溶液1-2mL,滴入1-2滴無色酚酞試液,振蕩 | 無色酚酞試液不變色 | 猜想__________不成立 |
查看答案和解析>>
科目:初中化學 來源:不詳 題型:實驗題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com