CaCO
3廣泛存在于自然界,是一種重要的化工原料.某種大理石除主要成分為CaCO
3外,還有少量的硫化物.小平和小明同學(xué)用這種大理石和稀鹽酸反應(yīng),分別開展以下探究,請你參與探究并回答相關(guān)問題.
[查閱資料]資料一:在常溫下,測得濃度均為a%的下列六種溶液的pH大小情況:
| 溶質(zhì) |
H2SO4 |
HCl |
H2S |
H2CO3 |
HClO |
| pH |
小→大 |
表中pH大小情況揭示出復(fù)分解反應(yīng)的一條規(guī)律,即較強(qiáng)酸發(fā)生類似反應(yīng)可以生成較弱酸.下列反應(yīng)均能發(fā)生,其中不符合該規(guī)律的是
D
D
(填字母
A.H
2SO
4+2NaHCO
3=2NaCl+2H
2O+2CO
2↑ B.2HCl+CaS=CaC
2l+H
2S↑
C.CO
2+H
2O+Ca(ClO)
2=CaCO
3↓+2HClO D.H
2S+CuSO
4=H
2SO
4+CuS↓
資料二:CuS是黑褐色無定形粉末或粒狀物,不溶于濃鹽酸,不溶于水和硫化鈉溶液.
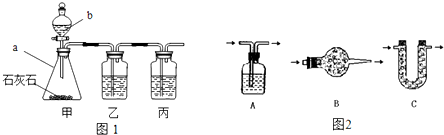
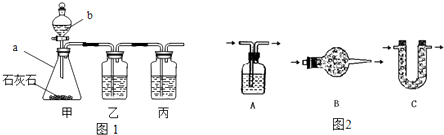
[實(shí)驗(yàn)探究]小平同學(xué)為了得到純凈的二氧化碳,設(shè)計(jì)了如下裝置,請你分析:
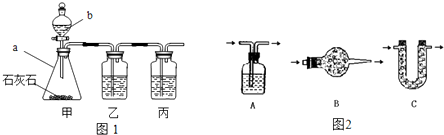
[制取CO
2]利用圖1、與圖2干燥裝置制得純凈干燥的CO
2.
(1)儀器a的名稱是
錐形瓶
錐形瓶
,儀器b的名稱是
分液漏斗
分液漏斗
.裝置甲中主要反應(yīng)的化學(xué)方程式為
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.
(2)裝置丙盛有足量的飽和NaHCO
3溶液,目的是除去
氯化氫氣體
氯化氫氣體
.裝置丙中主要反應(yīng)的化學(xué)方程式為
NaHCO3+HCl=NaCl+H2O+CO2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
.裝置乙中盛有的物質(zhì)是
CuSO4
CuSO4
溶液.現(xiàn)象:
出現(xiàn)黑褐色沉淀
出現(xiàn)黑褐色沉淀
.
(3)利用圖2干燥裝置干燥氣體,常見干燥劑有①濃硫酸②無水氯化鈣③堿石灰④生石灰若選用A裝置,則A裝置中放入藥品
①
①
(選擇序號);若選用B裝置,則B裝置中放入藥品
②
②
(選擇序號).
(4)小明同學(xué)為了計(jì)算這種大理石中含碳酸鈣質(zhì)量分?jǐn)?shù),進(jìn)行了如下定量實(shí)驗(yàn):
| 實(shí)驗(yàn)步驟 |
I將適量鹽酸加入燒杯中并稱量 |
II稱取少量大理石樣品加入燒杯中,使之與過量稀鹽酸反應(yīng) |
III待反應(yīng)完全后,稱重 |
| 實(shí)驗(yàn)圖示 |
 |
| 實(shí)驗(yàn)數(shù)據(jù) |
燒杯和鹽酸的質(zhì)量為100.0g |
大理石樣的質(zhì)量為12.0g |
燒杯和其中混合物的質(zhì)量為107.6g |
小明同學(xué)通過分析計(jì)算,得出結(jié)論:該實(shí)驗(yàn)中生成的二氧化碳的質(zhì)量是4.4g.大理石樣品純度為83.3%.請你評價(jià)他的結(jié)論是否正確
錯(cuò)誤
錯(cuò)誤
,并簡述理由
大理石中含有硫化物,硫化物與鹽酸反應(yīng)會(huì)生成硫化氫氣體逸出,把生成的氣體全部作為二氧化碳,使碳酸鈣質(zhì)量偏大,造成碳酸鈣的質(zhì)量分?jǐn)?shù)偏大
大理石中含有硫化物,硫化物與鹽酸反應(yīng)會(huì)生成硫化氫氣體逸出,把生成的氣體全部作為二氧化碳,使碳酸鈣質(zhì)量偏大,造成碳酸鈣的質(zhì)量分?jǐn)?shù)偏大
.