【答案】
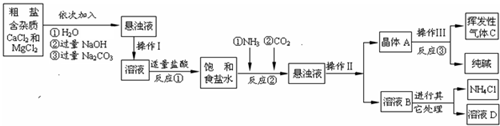
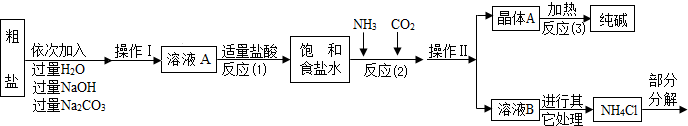
分析:(1)①根據氫氧化鈉和碳酸鈉都是過量,再結合生成物寫出溶質的化學式;
②根據過濾是分離不溶于液體的固體和液體的方法考慮;
③根據氫氧化鎂是沉淀考慮;
④根據碳酸鈉溶液可與氯化鈣溶液反應生成碳酸鈣沉淀書寫方程式;
(2)根據流程圖,反應物與生成物中的共同物質考慮;
(3)①根據充分受熱,碳酸氫鈉即可分解制得純堿及兩種常見的氧化物來考慮生成物和反應物,進而寫出方程式;
②根據碳酸氫鈉受熱易分解,碳酸鈉受熱不易分解,設計實驗檢驗其產物;二氧化碳可用澄清的石灰水檢驗,無水硫酸銅遇水變藍,可用來檢驗水;
(4)氯化鈉與硝酸銀反應可生成不溶于硝酸的氯化銀沉淀;
(5)①根據氯化鋇與碳酸鈉反應可生成碳酸鋇沉淀分析;
②判斷濾渣是否洗滌干凈,實際上是檢驗過量的氯化鋇溶液是否洗凈;然后根據氯化鋇可與稀硫酸和碳酸鈉溶液反應生成沉淀進行分析解答;
③根據白色固體是碳酸鋇,據其質量結合方程式計算碳酸鈉的質量,進而計算樣品中碳酸鈉的質量分數.
解答:解:(1)①氯化鈣能與碳酸鈉反應生成碳酸鈣沉淀和氯化鈉,所以A中的溶質主要是氯化鈉,由于氫氧化鈉和碳酸鈉過量,溶液A中也有氫氧化鈉和碳酸鈉;
故答案為:NaOH(氫氧化鈉)、Na
2CO
3(碳酸鈉);
②過濾是把固體與液體分開的操作,操作Ⅱ將混合物分成了晶體與溶液,正是通過過濾操作;
故答案為:過濾;
③粗鹽中含有少量可溶性雜質(MgCl
2和CaCl
2),氯化鎂能與氫氧化鈉反應生成氫氧化鎂沉淀和氯化鈉,所以加入氫氧化鈉溶液是除去粗鹽中的氯化鎂;
故答案為:MgCl
2(氯化鎂);
④碳酸鈉溶液與氯化鈣溶液反應生成碳酸鈣沉淀和氯化鈉,方程式是CaCl
2+Na
2CO
3═CaCO
3↓+2NaCl;
故答案為:CaCl
2+Na
2CO
3═CaCO
3↓+2NaCl;
(2)根據生產流程中涉及的方程式和流程圖,發現二氧化碳、氨氣、氯化氫、碳酸鈉為重復使用的物質;
故選ABC;
(3)①由題意知:晶體A充分受熱,可分解制得純堿及兩種常見的氧化物;依據反應流程圖可知A是碳酸氫鈉,化學反應前后元素的種類不變,從而推測出碳酸氫鈉分解生成碳酸鈉、水和二氧化碳;
故答案為:2NaHCO
3
Na
2CO
3+H
2O+CO
2↑;
②碳酸鈉化學性質穩定,碳酸氫鈉受熱易分解生成碳酸鈉、水、二氧化碳;而二氧化碳能使澄清的石灰水變渾濁,無水硫酸銅遇水變藍,可用來檢驗水,據此可設計實驗;
故答案為:
| 選擇的裝置 | 實驗現象 | 實驗結論 |
| AB”或“AC”或“ACB | “B不變渾濁”或“C不變藍”或“C不變藍、B不變渾” | 樣品不含晶體A |
(4)取純堿樣品加水溶解,向該溶液中加入過量稀HNO
3,反應掉碳酸鈉,再滴加AgNO
3溶液,仍有白色沉淀,說明一定含有氯化鈉,反應的方程式為AgNO
3+NaCl═AgCl↓+NaNO
3故答案為:AgNO
3+NaCl═AgCl↓+NaNO
3;
(5)①判斷加入氯化鋇溶液是否過量的合適方法是:靜置混合物X,向上層清液中再滴少許氯化鋇溶液,如有沉淀生成,說明氯化鋇溶液不足;
故選A;
②判斷濾渣是否洗滌干凈,實際上是檢驗過量的氯化鋇溶液是否洗凈;氯化鋇可與稀硫酸和碳酸鈉溶液反應生成硫酸鋇和碳酸鋇沉淀,通過觀察是否有沉淀生成可判斷氯化鋇溶液是否洗凈;
故選BC;
③設樣品中碳酸鈉的質量是X
BaCl
2+Na
2CO
3═BaCO
3↓+2NaCl
106 197
X 19.7g
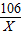
=

X=10.6g
所以樣品中碳酸鈉的質量分數是:
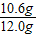
×100%=88.3%
答:樣品中碳酸鈉的質量分數是88.3%.
點評:本題充分考查利用課本知識解決新問題能力,能加深學生對課本知識的理解,訓練學生的思維能力、分析解決問題的能力,難度稍大.

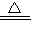 NH3↑+HCl↑.
NH3↑+HCl↑.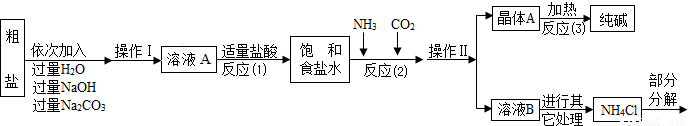


 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;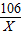 =
=
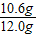 ×100%=88.3%
×100%=88.3%

 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案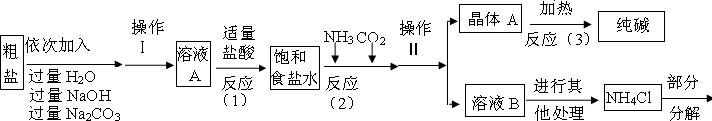
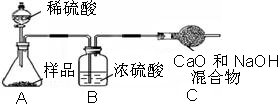 小心蒸發,并將所得物質干燥、冷卻至室溫后稱得固體質量為13.1g.樣品中碳酸鈉的質量分數為
小心蒸發,并將所得物質干燥、冷卻至室溫后稱得固體質量為13.1g.樣品中碳酸鈉的質量分數為