
【題目】用乙烯與甲苯為主要原料,按下列路線合成一種香料W:

(1)乙烯的電子式為__________________。
(2)乙炔到氯乙烯的反應類型為___________,氯乙烯到聚氯乙烯的反應化學方程式為________________________。
(3)芳香烴 ![]() 的名稱是_________________。
的名稱是_________________。
(4)實現反應①的試劑及條件______________;C中官能團名稱是________________。
(5)反應④的化學方程式為_______________________。
(6)驗證反應③已發生的操作及現象是___________________。
(7)寫出滿足下列條件的![]() 的一種同分異構體的結構簡式_________。
的一種同分異構體的結構簡式_________。
a.苯環上只有兩個取代基 b.能發生銀鏡反應
c.苯環上的一溴代物有兩種 d.能發生酯化反應
【答案】 ![]() 加成 n
加成 n![]() 鄰甲(基)乙苯或2-甲基乙苯 氯氣、光照 羥基
鄰甲(基)乙苯或2-甲基乙苯 氯氣、光照 羥基 ![]() 取樣,滴加新制氫氧化銅懸濁液,加熱,有磚紅色沉淀生成,可證明反應③已經發生。(合理即給分)
取樣,滴加新制氫氧化銅懸濁液,加熱,有磚紅色沉淀生成,可證明反應③已經發生。(合理即給分) 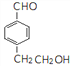 、
、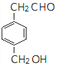 、
、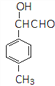 、……(合理即給分)
、……(合理即給分)
【解析】(1)乙烯分子中碳碳以雙鍵相連,碳剩余價鍵被H飽和,由此寫出電子式為![]() ;(2)乙炔與HCl發生加成反應生成氯乙烯,氯乙烯制取聚氯乙烯發生了加聚反應,化學方程式: n
;(2)乙炔與HCl發生加成反應生成氯乙烯,氯乙烯制取聚氯乙烯發生了加聚反應,化學方程式: n![]() ;(3)芳香烴
;(3)芳香烴![]() 的名稱是2-甲基乙苯;(4)甲苯在光照條件下與氯氣發生的是取代反應,則試劑及條件氯氣、光照;C為
的名稱是2-甲基乙苯;(4)甲苯在光照條件下與氯氣發生的是取代反應,則試劑及條件氯氣、光照;C為![]() ,官能團名稱是羥基;(5)反應④為A和C發生的酯化反應,化學方程式為
,官能團名稱是羥基;(5)反應④為A和C發生的酯化反應,化學方程式為![]() ;(6)反應③已發生說明有醛基生成,則檢驗的操作及現象是取樣,滴加新制的氫氧化銅溶液,加熱,如果看到有磚紅色沉淀生成,則說明反應③已發生;(7)a.苯環上只有兩個取代基。c.苯環上的一溴代物有兩種,說明對位結構;又b.能發生銀鏡反應,d.能發生酯化反應,說明含有醛基和羥基;則符合條件的 有
;(6)反應③已發生說明有醛基生成,則檢驗的操作及現象是取樣,滴加新制的氫氧化銅溶液,加熱,如果看到有磚紅色沉淀生成,則說明反應③已發生;(7)a.苯環上只有兩個取代基。c.苯環上的一溴代物有兩種,說明對位結構;又b.能發生銀鏡反應,d.能發生酯化反應,說明含有醛基和羥基;則符合條件的 有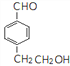 、
、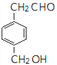 、
、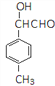 。
。


科目:高中化學 來源: 題型:
【題目】迷迭香酸是從蜂花屬植物中提取到的酸性物質,其結構如下圖所示.下列敘述正確的是( )
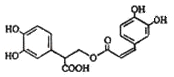
A. 迷迭香酸的分子式為C18H14O8
B. 該物質能使溴水或高錳酸鉀溶液褪色,不能與FeCl3溶液發生顯色反應
C. 1mol迷迭香酸跟H2反應,最多消耗9molH2
D. 1mol迷迭香酸與足量NaOH溶液反應,最多消耗6molNaOH
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4反應中,被氧化的P原子與被還原的P原子個數比是
A. 6:5 B. 5:6 C. 11:5 D. 11:6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pH相同的醋酸溶液和鹽酸,分別用蒸餾水稀釋到原溶液的m倍和n倍,稀釋后兩溶液的pH仍相同,則m和n的關系量是
A.m=n B.m>n C.m<n D.無法判斷
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了強化安全管理,某油庫引進了一臺空氣中汽油含量的測量儀,其工作原理如圖所示(用強酸性溶液作電解質溶液)。下列說法中不正確的是
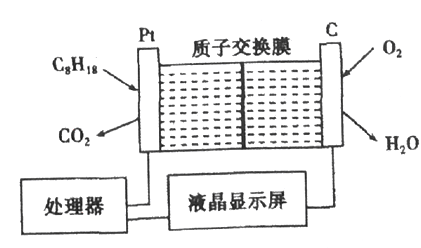
A. 石墨電極作正極,發生還原反應
B. 鉑電極的電極反應式為:C8H18+16H2O-50e-=8CO2+50H+
C. H+由質子交換膜左側向右側遷移
D. 每消耗標準狀況下5.6 L O2溶液中通過lmol 電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是用濃硝酸、銅片、水等試劑探究濃、稀硝酸的強氧化性并觀察還原產物的實驗裝置。
Ⅰ.濃硝酸的強氧化性實驗
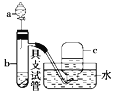
將銅片置于具支試管的底部,在分液漏斗中加入約5 mL濃硝酸,往具支試管中放入約2 mL濃硝酸,用排水法收集產生的氣體。
(1)具支試管中發生反應的化學方程式:___________________________________________。
(2)實驗中觀察到能證明濃硝酸具有強氧化性的現象_________________。
Ⅱ.稀硝酸的強氧化性實驗
(3)上述反應完成后,欲進一步證明稀硝酸也具有強氧化性,緊接的簡便、合理的實驗操作是________________________________________________________________________。
(4)能證明稀硝酸與銅反應產生NO的實驗現象是____________________(填寫序號)。
A.c中收集到無色氣體
B.c中收集到的無色氣體接觸空氣后變為紅棕色
C.b中產生的無色氣體接觸空氣后變為紅棕色
Ⅲ.實驗反思
(5)利用該裝置先進行銅與濃硝酸反應,再進行銅與稀硝酸反應的實驗,其好處是________________________________________________________________________。
Ⅳ.問題討論
用等質量的銅片與等體積的濃硝酸、稀硝酸(硝酸均過量)反應時,發現反應后所得溶液前者呈綠色,后者呈藍色。對此有兩種看法:
①兩者顏色不同的原因是因為Cu2+濃度差異引起的。
②前者溶液呈綠色,是因為生成的紅棕色NO2溶解于溶液中引起的。
(6)你認為上述看法________(填“①”或“②”)合理。若是①合理,說明理由,若是②合理,設計一個簡單實驗證明:______________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com