
��500mLNH4HCO3��Na2CO3�Ļ����Һ�ֳ���ȷݣ�ȡһ�ݼ��뺬amol�������c����Һǡ�÷�����ȫ����ȡһ�ݼ��뺬b mol HCl���}��ǡ�÷�����ȫ���tԓ�����Һ��c(Na+)�飨 ��
A����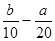 ��mol/L ��mol/L | B��(2b��a)mol/L | C��(l0b - 5a) mol/L | D����5bһ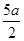 ��mol/L ��mol/L |
C
����ԇ�}����������NaOH�cNH4HCO3������2NaOH+NH4HCO3=Na2CO3+NH3?H2O+H2O���tn(NH4HCO3)=1/2n(NaOH)=1/2amol�������}���HCl�cNH4HCO3��Na2CO3��������HCl+ NH4HCO3=NH4Cl+CO2��+H2O����֪�cNH4HCO3������HCl�����|������1/2amol���t�cNa2CO3������HCl�����|�����飺��b-1/2a��mol������(j��)Na2CO3+2HCl=2NaCl+CO2��+H2O����֪Na+�飨b-1/2a��mol��������Һ���w�e0.1L�ɵ��c�x�ӝ�Ȟ飺(l0b - 5a) mol?L?1����C����_��
���c�����}�������(j��)���W����ʽ��Ӌ�㡣



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
�������P���W���Z��ʾ���_����
A���������c�����ʽ��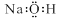 |
B��Cl���ĽY��ʾ��D�� |
C��2�������ĽY����ʽ��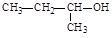 |
| D��̼�����x����ʽ��H2CO3=2H+��CO32�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
ijϡ�����ϡ����Ļ����Һ200 mL��ƽ���ֳɃɷݡ�������һ������u�����~�ۣ�������ܽ�19.2 g(��֪����ֻ��߀ԭ��NO���w)������һ������u�����F�ۣ��a�����w�����S�F���|�����ӵ�׃����D��ʾ�����з�����Y�������_����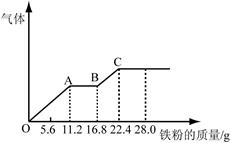
| A���������HNO3���|������Ȟ�2 mol��L��1 |
| B��ԭ�������H2SO4���|������0.4 mol |
| C��OA�ήa������NO��AB�εķ�����Fe+2Fe3+��3Fe2+��BC�ήa����� |
| D���ڶ�����Һ����K���|��FeSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
��NA��ʾ�����ӵ��_����(sh��)��ֵ�����Д������_����
| A��1molFeCl3�c��ˮ���������z�w����NA��Fe(OH)3�z�� |
| B���˜ʠ�r�£�1.12 L��HCHO������ԭ�Ӕ�(sh��)��0.2NA |
| C��1 L0.5mol��L-1Na2CO3��Һ�к��е�CO32����(sh��)Ŀ��0.5NA |
| D��0.1 mol Na2O2���������r�D�Ƶ���Ӕ�(sh��)Ŀ��0.2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
�ONA�鰢���ӵ��_����(sh��)��ֵ�����Д������_����
| A��1 molCl2�c����Fe�����D����Ӕ�(sh��)һ����3NA |
| B���˜ʠ�r�£�2.24 L NH3�к��й��r�I�Ĕ�(sh��)Ŀ��NA |
| C��1 mol Na2O��Na2O2������к��е�ꎡ���x�ӿ���(sh��)��3 NA |
| D���˜ʠ�r�£�11.2 L SO3�����ķ��Ӕ�(sh��)Ŀ��0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
��9��7 g Cu��Zn�ĺϽ��c������ϡHNO3������߀ԭ�a��ֻ��NO���w�����w�e�ژ˜ʠ�r��2�� 24 L������Һϡጞ�IL���y����Һ��pH=l���˕r��Һ��NO��3�ĝ�Ȟ�
| A��0��3 mol/L | B��0��4 mol/L | C��0��5 mol/L | D��0��6 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
��mg�V���X�Ļ�����м����m����ϡ���ᣬǡ����ȫ�������ɘ˜ʠ�r�µĚ��wbL���������Һ�м���cmol/L���������ҺVmL��ʹ�����x�ӄ��ó�����ȫ���õ��ij����|����ng���ٌ��õ��ij����Ɵ����|�����ٸ�׃?y��u)�ֹ���õ����wpg���t�����Pϵ�����_����
| A��c��1000b/11.2V | B��p��m+Vc/125 | C��n��m+17Vc | D��5/3m��p��17/9m |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
�������P���W���Z��ʾ���_����
A����ȩ�����ʽ��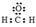 |
B���������ӵĽY����ʽ��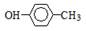 |
C��3��3-����-1-��ϩ���I��ʽ��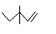 |
D���Ҵ����ӵı���ģ�ͣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
���|̼�������~��һ���ض��·����r�������~�ɱ�߀ԭ��Cu2O��Cu���F(xi��n)��2.00g C�c16.0g CuO�Ļ������^�՚�ӟ�һ�Εr�g��,�����ɵĚ��wͨ�^�����ijΜ[ʯ��ˮ�����ռ���1.12 L���w(�˜ʠ�r��,���ɳ������|����5.00 g�������f���e�`����
| A��������Ĺ��w�������߀����̼ |
| B����������w�������Cu���|����12.8 g |
| C��������Ĺ��w����ᅡ�|�F��14.4 g |
| D����������w�����������������|������0.05mol |
�鿴�𰸺ͽ���>>
���H�WУ��(y��u)�x - �������б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com