
【題目】以MnO2為原料制得的MnCl2溶液中常含有Cu2+、Pb2+等金屬離子,通過(guò)添加過(guò)量難溶電解質(zhì)MnS,可使這些金屬離子形成硫化物沉淀,經(jīng)過(guò)濾除去包括MnS在內(nèi)的沉淀。根據(jù)上述實(shí)驗(yàn)事實(shí),下列說(shuō)法中,不正確的是
A.溶解度 MnS<PbS
B.MnS存在沉淀溶解平衡 MnS(s)![]() Mn2+(aq) + S2-(aq)
Mn2+(aq) + S2-(aq)
C.Cu2+轉(zhuǎn)化為沉淀的原理為 MnS(s) + Cu2+(aq)=CuS(s) + Mn2+(aq)
D.沉淀轉(zhuǎn)化能用于除去溶液中的某些雜質(zhì)離子
【答案】A
【解析】
試題分析:A.根據(jù)題意,含有Cu2+、Pb2+等金屬離子的溶液中添加過(guò)量難溶電解質(zhì)MnS,可使這些金屬離子形成硫化物沉淀,說(shuō)明溶解度PbS <MnS,錯(cuò)誤;B.MnS存在沉淀溶解平衡,平衡方程式為MnS(s)![]() Mn2+(aq) + S2-(aq),正確;C.Cu2+轉(zhuǎn)化為沉淀的原理為MnS(s)
Mn2+(aq) + S2-(aq),正確;C.Cu2+轉(zhuǎn)化為沉淀的原理為MnS(s)![]() Mn2+(aq) + S2-(aq),與Cu2+形成CuS后,平衡正向移動(dòng),促進(jìn)MnS溶解,反應(yīng)方程式為MnS(s) + Cu2+(aq)=CuS(s) + Mn2+(aq),正確;D.根據(jù)題意,可以利用沉淀轉(zhuǎn)化的原理除去溶液中的某些雜質(zhì)離子,正確;故選A。
Mn2+(aq) + S2-(aq),與Cu2+形成CuS后,平衡正向移動(dòng),促進(jìn)MnS溶解,反應(yīng)方程式為MnS(s) + Cu2+(aq)=CuS(s) + Mn2+(aq),正確;D.根據(jù)題意,可以利用沉淀轉(zhuǎn)化的原理除去溶液中的某些雜質(zhì)離子,正確;故選A。


 目標(biāo)測(cè)試系列答案
目標(biāo)測(cè)試系列答案
| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:
【題目】實(shí)驗(yàn)室制備氨基甲酸銨(NH2COONH4)的反應(yīng)如下:2NH3(g)+CO2(g)![]() NH2COONH4(s)該反應(yīng)在干燥條件下僅生成氨基甲酸銨,若有水存在則生成碳酸銨或碳酸氫氨。
NH2COONH4(s)該反應(yīng)在干燥條件下僅生成氨基甲酸銨,若有水存在則生成碳酸銨或碳酸氫氨。
(1)該反應(yīng)在一定條件下能夠白發(fā)進(jìn)行,則反應(yīng)的△H_____________0(填“>”、“<”或“一”)。
(2)寫(xiě)出生成碳酸氫氨的化學(xué)方程式:______________。
(3)實(shí)驗(yàn)步驟如下:
步驟1:按圖所示組裝儀器,檢查裝置的氣密性。

步驟2:在相應(yīng)儀器中裝入藥品,其中在三頸燒瓶中加入氫氧化鈉固體,恒壓滴液漏斗中裝入濃氨水。
步驟3:滴加濃氨水并攪拌,調(diào)節(jié)反應(yīng)速率,在反應(yīng)器中得到產(chǎn)品。
干燥管中盛放的藥品是___________。
對(duì)比碳酸鹽和酸反應(yīng)制CO2,該實(shí)驗(yàn)利用干冰升華產(chǎn)生CO2氣體的優(yōu)點(diǎn)是__________________。
③以恒壓滴液漏斗代替分液漏斗的目的是______________________。
(4)該實(shí)驗(yàn)裝置可能存在的安全問(wèn)題是__________________。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】有A、B兩個(gè)完全相同的裝置,某學(xué)生分別在它們的側(cè)管中裝入一定量的Na2CO3和NaHCO3,A、B中分別裝有足量的鹽酸,將兩個(gè)側(cè)管中的物質(zhì)同時(shí)倒入各自的試管中,下列敘述正確的是
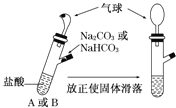
A. 側(cè)管中裝入Na2CO3的氣球膨脹速率大
B. 若加入等質(zhì)量的Na2CO3和NaHCO3 ,最終兩氣球體積不同
C. 最終兩試管中Na+、Cl-的物質(zhì)的量一定相同
D. 熱穩(wěn)定性:Na2CO3 < NaHCO3
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】草酸晶體的組成可用H2C2O4·xH2O表示,為了測(cè)定x值,進(jìn)行如下實(shí)驗(yàn):稱(chēng)取Wg草酸晶體,配成100.00mL水溶液。將25.00mL所配制的草酸溶液置于錐形瓶?jī)?nèi),加入適量稀H2SO4后,用濃度為amol·L-1的KMnO4溶液滴定到KMnO4不再褪色為止。
試回答:
(1)實(shí)驗(yàn)中不考慮鐵架臺(tái)等夾持儀器外,不需要的儀器有(填序號(hào)) ,還缺少的儀器有(填名稱(chēng))_ 。
A托盤(pán)天平(帶砝碼,鑷子) B滴定管 C 100mL容量瓶 D燒杯
e.漏斗 f.錐形瓶 g.玻璃棒 h.燒瓶
(2)實(shí)驗(yàn)中,標(biāo)準(zhǔn)液KMnO4溶液應(yīng)裝在______________式滴定管中。
(3)若在滴定前沒(méi)有用amol·L-1的KMnO4溶液對(duì)滴定管進(jìn)行潤(rùn)洗,則所測(cè)得的x值會(huì)___________(偏大、偏小、無(wú)影響)。
(4)在滴定過(guò)程中若用amol·L-1的KMnO4溶液VmL,則所配制的草酸溶液的物質(zhì)的量濃度為_(kāi)_________mol·L-1,由此可計(jì)算x的值是____________。
(5)寫(xiě)出酸性高錳酸鉀溶液滴定草酸溶液過(guò)程中反應(yīng)的離子方程式_______________。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】Ⅰ.某化學(xué)興趣小組為探究SO2的性質(zhì),按下圖所示裝置進(jìn)行實(shí)驗(yàn)。
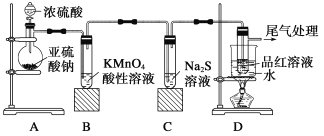
請(qǐng)回答:
(1)裝置A中蒸餾燒瓶生成SO2的化學(xué)方程式為: 。
(2)實(shí)驗(yàn)過(guò)程中,裝置B、C中發(fā)生的現(xiàn)象分別是 、 ,這些現(xiàn)象分別說(shuō)明SO2具有的性質(zhì)是 和 ;裝置B中發(fā)生反應(yīng)的離子方程式為: 。
(3)裝置D的目的是探究SO2與品紅作用的可逆性,請(qǐng)寫(xiě)出實(shí)驗(yàn)操作及現(xiàn)象: 。
Ⅱ.某化學(xué)興趣小組為探究銅跟濃硫酸的反應(yīng),用圖所示裝置進(jìn)行有關(guān)實(shí)驗(yàn)。請(qǐng)回答:
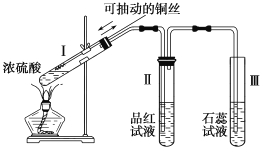
(4)試管Ⅰ中發(fā)生反應(yīng)的化學(xué)方程式為:: 。
(5)下列實(shí)驗(yàn)不合理的是 。
A.上下移動(dòng)Ⅰ中銅絲可控制生成SO2的量
B.Ⅱ中選用品紅溶液驗(yàn)證SO2的生成
C.Ⅲ中可選用NaOH溶液吸收多余的SO2
D.為確認(rèn)CuSO4生成,向Ⅰ加水,觀察溶液顏色
(6)實(shí)驗(yàn)中,用ag銅片和VmL18.4mol·L-1的濃硫酸(98%)放在試管中共熱,直到反應(yīng)完畢,發(fā)現(xiàn)試管中還有銅片剩余,該小組學(xué)生認(rèn)為還有一定量的硫酸剩余。
①有一定量的硫酸剩余但未能使銅片完全溶解,你認(rèn)為原因是 。
②下列藥品中能用來(lái)證明反應(yīng)結(jié)束后的試管中確有硫酸剩余的是 (填序號(hào))。
a.鐵粉 b.BaCl2溶液 c.Ba(NO3)2溶液 d.Na2CO3溶液
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
【題目】如圖a、b、c、d均為鉑電極,供選擇的電解質(zhì)溶液如下表( )
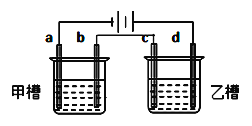
要滿(mǎn)足的條件是:①工作一段時(shí)間后,甲槽電解液pH上升,而乙槽電解液pH下降;
②b、c兩極放電離子的物質(zhì)的量相等。則應(yīng)選用的電解液是
組 | A | B | C | D |
甲槽 | NaOH | Cu(NO3)2 | KCl | Na2SO4 |
乙槽 | CuSO4 | NaCl | AgNO3 | NaNO3 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
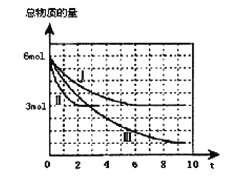
【題目】甲醇是一種可再生的清潔能源,一定條件下用CO和H2合成CH3OH:CO(g)+2H2 (g)![]() CH3OH(g)H =a kJ·mol-1。向體積為2 L的密閉容器中充入2mol CO和4mol H2,測(cè)得不同溫度下容器內(nèi)氣體總物質(zhì)的量隨時(shí)間(min)的變化關(guān)系如下左圖中Ⅰ、Ⅱ、Ⅲ曲線所示:
CH3OH(g)H =a kJ·mol-1。向體積為2 L的密閉容器中充入2mol CO和4mol H2,測(cè)得不同溫度下容器內(nèi)氣體總物質(zhì)的量隨時(shí)間(min)的變化關(guān)系如下左圖中Ⅰ、Ⅱ、Ⅲ曲線所示:
(1)能判斷反應(yīng)達(dá)到化學(xué)平衡狀態(tài)的是 (填字母)。
A.c(CO)與c(H2)的比值保持不變
B.容器中氣體壓強(qiáng)保持不變
C.容器中氣體密度保持不變
D.單位時(shí)間內(nèi)有1molCO消耗的同時(shí)有1mol CH3OH生成
E.v正(H2)=2 v逆(CH3OH)
(2)①Ⅱ和Ⅰ相比,Ⅱ改變的反應(yīng)條件是 。
②反應(yīng)Ⅲ在9min時(shí)達(dá)到平衡,比較反應(yīng)Ⅰ的溫度(T1)和反應(yīng)Ⅲ的溫度(T3)的高低:T1 T3(填“>”“<”“=”),此正反應(yīng)是________反應(yīng)(填“放熱或吸熱”)。
(3)①反應(yīng)Ⅰ在6 min時(shí)達(dá)到平衡,從反應(yīng)開(kāi)始到達(dá)到平衡時(shí)v (CH3OH) = mol/(L·min)。
②反應(yīng)Ⅱ在2 min時(shí)達(dá)到平衡,計(jì)算該溫度下的平衡常數(shù)K= 。在體積和溫度不變的條件下,在上述反應(yīng)達(dá)到平衡Ⅱ時(shí),再往容器中加入1 mol CO和3 mol CH3OH后,平衡將向_________(填“正反應(yīng)、逆反應(yīng)和不移動(dòng)”),原因是______________。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
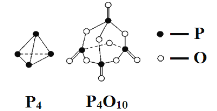
【題目】白磷與氧氣可發(fā)生如下反應(yīng):P4+5O2 = P4O10。已知斷裂下列化學(xué)鍵需要吸收的能量分別為:E(P—P) = a kJ·mol-1、E(P—O) = b kJ·mol-1、E(P=O) = c kJ·mol-1、E(O=O) = d kJ·mol-1。根據(jù)圖示的分子結(jié)構(gòu)和有關(guān)數(shù)據(jù)估算該反應(yīng)的ΔH,其中正確的是( )
A.-(6a-12b-4c+5d)kJ·mol-1
B.-(-6a+12b+4c-5d)kJ·mol-1
C.-(-4a+6b+4c-5d)kJ·mol-1
D.-(4a-6b-4c+5d)kJ·mol-1
查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專(zhuān)區(qū) | 電信詐騙舉報(bào)專(zhuān)區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專(zhuān)區(qū) | 涉企侵權(quán)舉報(bào)專(zhuān)區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com