
【題目】已知NO2與N2O4相互轉化:2NO2(g)N2O4(g);△H=﹣24.2kJ/mol 在恒溫下,將一定量NO2和N2O4(g)的混合氣體充入體積為2L的密閉容器中,其中物質的濃度隨時間變化的關系如圖.下列推理分析合理的是( )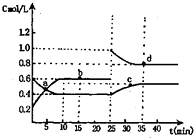
A.a,b,c,d四點中c正與v逆均相等
B.反應進行到10min時,體系吸收的熱量為9.68kJ
C.前10min內,用v(NO2)表示的該反應速率為0.02mol/Lmin
D.25min時,導致平衡移動的原因是升溫
【答案】B
【解析】解:由圖可知10﹣25min平衡狀態時,bd點所在曲線的濃度增加量為(0.6﹣0.2)mol/L=0.4mol/L,c點所在曲線的濃度減少量為(0.6﹣0.4)mol/L=0.2mol/L,bd點所在曲線表示的生成物的濃度變化量是c點所在曲線表示的反應物的濃度變化量的2倍,所以bd點所在曲線表示NO2濃度隨時間的變化曲線,c點所在曲線表示N2O4濃度隨時間的變化曲線;反應時NO2濃度增大,N2O4濃度減小,說明反應逆向進行, A.由圖可知,10﹣25min及35min之后NO2和N2O4的物質的量不發生變化,則相應時間段內的點處于化學平衡狀態,即b、d處于化學平衡狀態,故A錯誤;
B.由圖可知10﹣25min平衡狀態時,反應消耗的N2O4濃度為0.2mol/L,則其物質的量為0.2mol/L×2L=0.4mol,反應逆向進行,要吸收熱量,則反應吸收的熱量為0.4mol×24.2kJ/mol=9.68kJ,故B正確;
C.由圖象可知,10 min內用NO2的濃度變化量為(0.6﹣0.2)mol/L=0.4mol/L,故v(NO2)= ![]() =0.04mol/(Lmin),故C錯誤;
=0.04mol/(Lmin),故C錯誤;
D.25min時,X的濃度增大,Y的濃度不變,只能是增大X的濃度,所以曲線發生變化的原因是增加NO2濃度,故D錯誤;
故選B.
由圖可知10﹣25min平衡狀態時,bd點所在曲線的濃度增加量為(0.6﹣0.2)mol/L=0.4mol/L,c點所在曲線的濃度減少量為(0.6﹣0.4)mol/L=0.2mol/L,bd點所在曲線表示的生成物的濃度變化量是c點所在曲線表示的反應物的濃度變化量的2倍,所以bd點所在曲線表示NO2濃度隨時間的變化曲線,c點所在曲線表示N2O4濃度隨時間的變化曲線;反應時NO2濃度增大,N2O4濃度減小,說明反應逆向進行,
A.物質的濃度不發生變化時表示化學反應處于平衡狀態;
B.根據反應中物質的量之比等于熱量比來計算;
C.由圖象可知,10 min內用NO2的濃度變化量為(0.6﹣0.2)mol/L=0.4mol/L,根據v= ![]() 計算v(NO2);
計算v(NO2);
D.25min時,X的濃度增大,Y的濃度不變,只能是增大X的濃度.


科目:高中化學 來源: 題型:
【題目】下列應用或事實與膠體的性質沒有關系的是
A.使用微波手術刀進行外科手術,可使開刀處的血液迅速凝固而減少失血
B.在飽和氯化鐵溶液中逐滴加入NaOH溶液,產生紅褐色沉淀
C.清晨的陽光穿過茂密的林木枝葉所產生的美麗景象(光線)
D.用石膏或鹽鹵點制豆腐
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于常見有機化合物的說法中正確的是
A.分子式為C4H10的物質具有三種分子結構
B.甲烷、苯、乙酸在一定條件下都能發生取代反應
C.絲綢和棉花的組成元素相同,分子結構不同,因而性質不同
D.用氫氧化鈉溶液與乙酸乙酯充分混合并振蕩,以除去其中的乙酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據題意填空
(1)常溫下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子發生電離,則溶液的pH=;可以使0.10molL﹣1 CH3COOH的電離程度增大的是
a.加入少量0.10molL﹣1的稀鹽酸 b.加熱CH3COOH溶液 c.加水稀釋至0.010molL﹣1 d.加入少量冰醋酸 e.加入少量氯化鈉固體 f.加入少量0.10molL﹣1的NaOH溶液
(2)將等質量的鋅投入等體積且pH均等于3的醋酸和鹽酸溶液中,經過充分反應后,發現只在一種溶液中有鋅粉剩余,則生成氫氣的體積:V(鹽酸)V(醋酸)(填“>”、“<”或“=”).
(3)0.1mol/L的某酸H2A的pH=4,則H2A的電離方程式為
(4)25℃時,將pH=9的NaOH溶液與pH=4的鹽酸溶液混合,若所得混合溶液的pH=6,則NaOH溶液與鹽酸溶液的體積比為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,用鉑電極電解CuSO4溶液,當陰極產生12.8g銅時,陽極放出的氣體是
A. 1.12L H2 B. 1.12L O2 C. 2.24L H2 D. 2.24L O2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com