
 為減小CO2對環境的影響,在限制其排放量的同時,應加強對CO2創新利用的研究.
為減小CO2對環境的影響,在限制其排放量的同時,應加強對CO2創新利用的研究.| 1 |
| 2 |
| 溶解度(S)/g | 溶度積(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
| △c |
| △t |
| ||
| ||
| 0.8mol/L |
| 10min |
| 4.8mol |
| 6mol |
| 1 |
| 2 |


 中考利劍中考試卷匯編系列答案
中考利劍中考試卷匯編系列答案科目:高中化學 來源: 題型:閱讀理解
 (2013?紅橋區二模)為減小CO2對環境的影響,在限制其排放量的同時,應加強對CO2創新利用的研究.
(2013?紅橋區二模)為減小CO2對環境的影響,在限制其排放量的同時,應加強對CO2創新利用的研究.
| ||
| ||
| 溶解度(S)/g | 溶度積(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
查看答案和解析>>
科目:高中化學 來源: 題型:
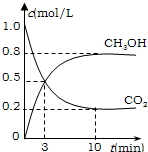
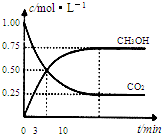 為減小CO2對環境的影響,在倡導“低碳”的同時,還需加強對CO2創新利用的研究.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.T1℃時,向體積為1L的恒容密閉容器中充入1molCO2和3molH2,測得CO2和CH3OH(g)的濃度隨時間變化曲線如圖所示,且平衡時體系壓強為P1.下列敘述中不正確的是( )
為減小CO2對環境的影響,在倡導“低碳”的同時,還需加強對CO2創新利用的研究.已知:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ/mol.T1℃時,向體積為1L的恒容密閉容器中充入1molCO2和3molH2,測得CO2和CH3OH(g)的濃度隨時間變化曲線如圖所示,且平衡時體系壓強為P1.下列敘述中不正確的是( )| A、0~3min內,v(CO2)正=v (CH3OH)正 | B、其他條件不變,若向平衡后的體系中充入1mol氦氣,體系壓強增大平衡將向正方向移動 | C、在T1℃時,若起始時向容器中充入2molCO2和6mol H2,測得平衡時容器內壓強為P2,則 P2<2P1 | D、T2℃時,上述反應平衡常數為4.2,則T2>T1 |
查看答案和解析>>
科目:高中化學 來源:2012屆杭師大附中普通高校招生適應性考試理綜試卷(化學部分) 題型:填空題
為減小CO2對環境的影響,在限制其排放量的同時,應加強對CO2創新利用的研究。
(1)① 把含有較高濃度CO2的空氣通入飽和K2CO3溶液。
② 在①的吸收液中通高溫水蒸氣得到高濃度的CO2氣體。
寫出②中反應的化學方程式________。
(2)如將CO2與H2以1:3的體積比混合。
①適當條件下合成某烴和水,該烴是_______(填序號)。
| A.烷烴 | B.烯烴 | C.炔烴 | D.苯的同系物 |
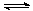 CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol。
 CO2(g)+ 2H2O(l) ΔH1=― 890.3 kJ/mol
CO2(g)+ 2H2O(l) ΔH1=― 890.3 kJ/mol H2O(l) ΔH2=-285.8 kJ/mol
H2O(l) ΔH2=-285.8 kJ/mol| 溶解度(S)/g | 溶度積(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
查看答案和解析>>
科目:高中化學 來源:2011-2012學年杭師大附中普通高校招生適應性考試理綜試卷(化學部分) 題型:綜合題
為減小CO2對環境的影響,在限制其排放量的同時,應加強對CO2創新利用的研究。
(1)① 把含有較高濃度CO2的空氣通入飽和K2CO3溶液。
② 在①的吸收液中通高溫水蒸氣得到高濃度的CO2氣體。
寫出②中反應的化學方程式________。
(2)如將CO2與H2 以1:3的體積比混合。
①適當條件下合成某烴和水,該烴是_______(填序號)。
A.烷烴 B.烯烴 C.炔烴 D.苯的同系物
② 適當條件下合成燃料甲醇和水。在體積為2L的密閉容器中,充入2 mol CO2和6 mol H2,一定條件下發生反應:CO2(g)+3H2(g)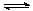 CH3OH(g)+H2O(g)
△H=-49.0 kJ/mol。
CH3OH(g)+H2O(g)
△H=-49.0 kJ/mol。
測得CO2(g)和CH3OH(g)的濃度隨時間變化如圖所示。
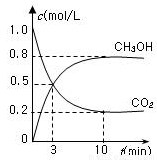
從反應開始到平衡,v(H2)=______;氫氣的轉化率=_______;能使平衡體系中n(CH3OH)增大的措施有______。
(3)如將CO2與H2 以1:4的體積比混合,在適當的條件下可制得CH4。
已知:
CH4 (g) + 2O2(g)  CO2(g)+
2H2O(l) ΔH1=― 890.3 kJ/mol
CO2(g)+
2H2O(l) ΔH1=― 890.3 kJ/mol
H2(g) + 1/2O2(g)  H2O(l)
ΔH2=-285.8 kJ/mol
H2O(l)
ΔH2=-285.8 kJ/mol
則CO2(g)與H2(g)反應生成CH4(g)與液態水的熱化學方程式是________。
(4)某同學用沉淀法測定含有較高濃度CO2的空氣中CO2的含量,經查得一些物質在20℃的數據如下表。
|
溶解度(S)/g |
溶度積(Ksp) |
||
|
Ca(OH)2 |
Ba(OH)2 |
CaCO3 |
BaCO3 |
|
0.16 |
3.89 |
2.9×10-9 |
2.6×10-9 |
(說明:Ksp越小,表示該物質在水溶液中越易沉淀)
吸收CO2最合適的試劑是_________[填“Ca(OH)2”或“Ba(OH)2”]溶液,實驗時除需要測定工業廢氣的體積(折算成標準狀況)外,還需要測定__________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com