
【題目】有研究表明,內(nèi)源性H2S作為氣體信號分子家族新成員,在抗炎、舒張血管等方面具有重要的生理作用,而籠狀COS(羰基硫)分子可作為H2S的新型供體(釋放劑)。試回答下列有關(guān)問題
(1)COS的分子結(jié)構(gòu)與CO2相似,COS的結(jié)構(gòu)式為______。
(2)已知:①COS(g)+H2(g)H2S(g)+CO(g)△H1=-15kJmol-1,②COS(g)+H2(g)H2S(g)+CO2(g)△H2=-36kJmol-1,③CO(g)+H2O(g)H2(g)+CO2(g)△H3,則△H=______。
(3)COS可由CO和H2S在一定條件下反應(yīng)制得。在恒容的密閉容器中發(fā)生反應(yīng)并達(dá)到平衡:CO(g)+H2S(g)COS(g)+H2(g),數(shù)據(jù)如表所示、據(jù)此填空
實(shí)驗 | 溫度/℃ | 起始時 | 平衡時 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | x |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
①該反應(yīng)為______(選填“吸熱反應(yīng)”或“放熱反應(yīng)”)。
②實(shí)驗2達(dá)到平衡時,x______7.0(選填“>”、“<”或“=”)
③實(shí)驗3達(dá)到平衡時,CO的轉(zhuǎn)化率α=______
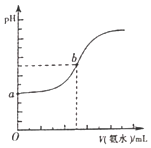
(4)已知常溫下,H2S和NH3H2O的電離常數(shù)分別為向pH=a的氫硫酸中滴加等濃度的氨水,加入氨水的體積(V)與溶液pH的關(guān)系如圖所示:
酸/堿 | 電離常數(shù) | |
H2S | Ka1=1.0×10-7 | Ka2=7.0×10-15 |
NH3H2O | Kb=1.0×10-5 | |
①若c(H2S)為0.1mol/L,則a=______
②若b點(diǎn)溶液pH=7,則b點(diǎn)溶液中所有離子濃度大小關(guān)系是______。
(5)將H2S通入裝有固體FeCl2的真空密閉燒瓶內(nèi),恒溫至300℃,反應(yīng)達(dá)到平衡時,燒瓶中固體只有FeCl2和FeSx(x并非整數(shù)),另有H2S、HCl和H2三種氣體,其分壓依次為0.30P0、0.80P0和0.04P0(P0表示標(biāo)準(zhǔn)大氣壓)。當(dāng)化學(xué)方程式中FeCl2的計量數(shù)為1時,該反應(yīng)的氣體壓強(qiáng)平衡常數(shù)記為Kp。計算:
①x=______(保留兩位有效數(shù)字)。
②Kp=______(數(shù)字用指數(shù)式表示)。
【答案】O=C=S 21kJmol-1 放熱反應(yīng) < 20% 4 c(NH4+)>c(HS-)>c(H+)=c(OH-)>c(S2-) 1.1 ![]()
【解析】
(1)CO2和COS是等電子體,等電子體結(jié)構(gòu)相似,根據(jù)二氧化碳的分子的結(jié)構(gòu)式可知COS結(jié)構(gòu)式;
(2)根據(jù)蓋斯定律計算可得;
(3)①分別建立三段式計算實(shí)驗1和實(shí)驗3的化學(xué)平衡常數(shù),依據(jù)平衡常數(shù)的大小判斷反應(yīng)時放熱還是吸熱;
②通過濃度熵與平衡常數(shù)的大小判斷平衡移動方向;
③依據(jù)三段式和轉(zhuǎn)化率公式計算;
(4)①依據(jù)電離常數(shù)公式計算;
②依據(jù)電離程度和水解程度的相對大小判斷;
(5)依據(jù)題給信息寫出反應(yīng)的化學(xué)方程式,由題給數(shù)據(jù)和公式計算即可。
(1)由二氧化碳分子的結(jié)構(gòu)式可知:COS分子中C與O、C與S均形成兩對共有電子對,所以COS結(jié)構(gòu)式為:O=C=S,故答案為:O=C=S;
(2)蓋斯定律②-①得到CO(g)+H2O(g)H2(g)+CO2(g)的焓變△H3=-36kJmol-1-(-15kJmol-1)=-21kJmol-1,故答案為:-21kJmol-1;
(3)設(shè)容器體積為1L。
①由題意可建立實(shí)驗1反應(yīng)的三段式為:
CO(g)+H2S(g)COS(g)+H2(g)
開始(mol/L)10.010.000
反應(yīng)(mol/L)3.0 3.0 3.0 3.0
平衡(mol/L)7.0 7.0 3.0 3.0
化學(xué)平衡常數(shù)=![]() =
=![]() =0.18;
=0.18;
由題意可建立實(shí)驗3反應(yīng)的三段式為:
CO(g)+H2S(g)COS(g)+H2(g)
開始(mol/L) 20.0 20.0 0 0
反應(yīng)(mol/L) 4.04.04.0 4.0
平衡(mol/L) 16.016.0 4.0 4.0
化學(xué)平衡常數(shù)=![]() =
=![]() =0.0625<0.18,所以升高溫度,平衡常數(shù)k減小,即平衡逆向移動,正向即放熱反應(yīng),故答案為:放熱反應(yīng);
=0.0625<0.18,所以升高溫度,平衡常數(shù)k減小,即平衡逆向移動,正向即放熱反應(yīng),故答案為:放熱反應(yīng);
②150℃,濃度熵Qc=![]() =
=![]() ≈0.16<k=0.18,則反應(yīng)向正反應(yīng)方向移動,所以實(shí)驗2達(dá)平衡時,n(CO)減小,x<7.0,故答案為:<;
≈0.16<k=0.18,則反應(yīng)向正反應(yīng)方向移動,所以實(shí)驗2達(dá)平衡時,n(CO)減小,x<7.0,故答案為:<;
③實(shí)驗3達(dá)平衡時,CO的轉(zhuǎn)化率=![]() ×100%=
×100%=![]() ×100%=20%,故答案為:20%;
×100%=20%,故答案為:20%;
(4)①c(H+)=![]() =
=![]() mol/L=10-4mol/L,a=pH=-lg10-4=4,故答案為:4;
mol/L=10-4mol/L,a=pH=-lg10-4=4,故答案為:4;
②b點(diǎn)呈中性,則c(H+)=c(OH-),溶液中電荷關(guān)系為c(NH4+)+c(H+)=c(HS-)+2c(S2-)+c(OH-),所以c(NH4+)>c(HS-),由于HS-的電離程度很小、主要以電離為主,同時促進(jìn)水的電離,所以c(H+)>c(S2-),即b點(diǎn)時溶液中所有離子濃度大小關(guān)系是c(NH4+)>c(HS-)>c(H+)=c(OH-)>c(S2-),故答案為:c(NH4+)>c(HS-)>c(H+)=c(OH-)>c(S2-);
(5)H2S和FeCl2反應(yīng)的方程式為xH2S(g)+FeCl2(s)FeSx(s)+2HCl(g)+(x-1)H2(g)。
①有化學(xué)方程式可得關(guān)系式:2:(x-1)=0.80P0:0.04P0,解得x=1.1,故答案為:1.1;
②H2S和FeCl2反應(yīng)的方程式為1.1H2S(g)+FeCl2(s)FeS1.1(s)+2HCl(g)+0.1H2(g),由方程式可得p(HCl)=0.80P0,p(H2)=0.04P0,p(H2S)=0.30P0,平衡分壓常數(shù)Kp=![]()
=![]() ,故答案為:
,故答案為:![]() 。
。


 孟建平小學(xué)滾動測試系列答案
孟建平小學(xué)滾動測試系列答案 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案
| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:
【題目】一種芳綸纖的拉伸強(qiáng)度比鋼絲還高,廣泛用作防護(hù)材料。其結(jié)構(gòu)片段如下圖所示:
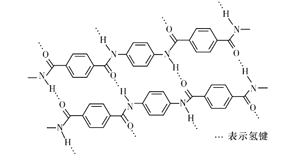
下列關(guān)于該高分子的說法不正確的是
A. 芳綸纖維可用作航天、航空、國防等高科技領(lǐng)域的重要基礎(chǔ)材料
B. 完全水解產(chǎn)物的單個分子中,含有官能團(tuán)一COOH或一NH2
C. 氫鍵對該高分子的性能有影響
D. 結(jié)構(gòu)簡式為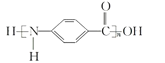
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】某研究小組擬合成醫(yī)藥中間體X和Y。
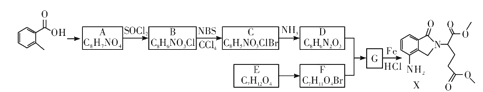
已知:①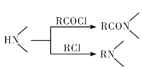 ;
;
②![]() ;
;
③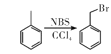 。
。
(1)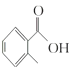 的名稱是__________
的名稱是__________
(2)G→X的反應(yīng)類型是_____________。
(3)化合物B的結(jié)構(gòu)簡式為_____________。
(4)下列說法不正確的是__________(填字母代號)
A. 化合物A能使酸性KMnO4溶液褪色
B.化合物C能發(fā)生加成、取代、消去反應(yīng)
C.化合物D能與稀鹽酸反應(yīng)
D.X的分子式是C15H16N2O5
(5)寫出D+F→G的化學(xué)方程式:____________________
(6)寫出化合物A(C8H7NO4)同時符合下列條件的兩種同分異構(gòu)體的結(jié)構(gòu)簡式_______。
①分子是苯的二取代物,1H—NMR譜表明分子中有4種化學(xué)環(huán)境不同的氧原子;
②分子中存在硝基和![]() 結(jié)構(gòu)。
結(jié)構(gòu)。
(7)參照以上合成路線設(shè)計E→![]() 的合成路線(用流程圖表示,無機(jī)試劑任選)。
的合成路線(用流程圖表示,無機(jī)試劑任選)。
____________________________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】從香莢蘭豆中提取的一種芳香化合物,其分子式為C8H8O3,遇FeCl3溶液會呈現(xiàn)特征顏色,能發(fā)生銀鏡反應(yīng)。該化合物可能的結(jié)構(gòu)簡式是( )
A.  B.
B.  C.
C.  D.
D. 
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】化學(xué)是一門以實(shí)驗為基礎(chǔ)的學(xué)科。下列實(shí)驗裝置和方案能達(dá)到相應(yīng)目的是( )
A. 圖裝置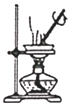 ,加熱蒸發(fā)碘水提取碘
,加熱蒸發(fā)碘水提取碘
B. 圖裝置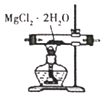 ,加熱分解制得無水Mg
,加熱分解制得無水Mg
C. 圖裝置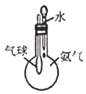 ,驗證氨氣極易溶于水
,驗證氨氣極易溶于水
D. 圖裝置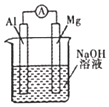 ,比較鎂、鋁的金屬性強(qiáng)弱
,比較鎂、鋁的金屬性強(qiáng)弱
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】(1)在配合物Fe(SCN)2+中,提供空軌道接受孤對電子的微粒是__,畫出配合物離子[Cu(NH3)4]2+中的配位鍵__.
(2)根據(jù)VSEPR模型,H3O+的分子立體結(jié)構(gòu)為__,BCl3的立體結(jié)構(gòu)為__.
(3)按要求寫出由第二周期元素為中心原子,通過sp3雜化形成中性分子的化學(xué)式(各寫一種)
正四面體分子__,三角錐形分子__,V形分子______。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】已知:4NH3+5O2==4NO+6H2O,若反應(yīng)速率分別用v(NH3)、v(O2)、v(NO)、v(H2O)表示,單位都為mol/(Ls),則正確的關(guān)系是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】Ⅰ、(1)某種金屬互化物具有自范性,原子在三維空間里呈周期性有序排列,該金屬互化物屬于__________(填 “晶體”或“非晶體”),可通過__________方法鑒別。
(2)基態(tài)Ni2+的核外電子排布式為__________;配合物Ni(CO)4常溫下為液態(tài),易溶于CCl4、苯等有機(jī)溶劑。固態(tài)Ni(CO)4屬于__________晶體;Ni2+和Fe2+的半徑分別為69pm和78pm,則熔點(diǎn)NiO__________FeO(填“<”或“>”)。
Ⅱ、判斷含氧酸強(qiáng)弱的一條經(jīng)驗規(guī)律是:含氧酸分子結(jié)構(gòu)中含非羥基氧原子數(shù)越多,該含氧酸的酸性越強(qiáng)。如下表所示
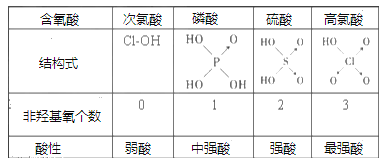
(1)亞磷酸(H3PO3)和亞砷酸(H3AsO3)分子式相似,但它們的酸性差別很大,H3PO3是中強(qiáng)酸,H3AsO3只有弱酸性。由此可推出亞磷酸的結(jié)構(gòu)式為___________。從分子結(jié)構(gòu)角度,簡述二者酸性強(qiáng)弱原因_____________________。
(2)亞磷酸與過量的氫氧化鈉溶液反應(yīng)的化學(xué)方程式為:________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】新冠病毒爆發(fā)期間,各類消毒劑大顯身手,ClO2泡騰片就是一種,使用時將其投入水中即可產(chǎn)生ClO2對水體、環(huán)境消毒。已知ClO2是一種易溶于水而難溶于有機(jī)溶劑的氣體,實(shí)驗室制備ClO2的原理是用亞氯酸鈉固體與氯氣反應(yīng):2NaClO2+Cl2=2ClO2+2NaCl。如圖是實(shí)驗室用于制備和收集一定量純凈的ClO2的裝置(某些夾持裝置和墊持用品省略)。其中E中盛有CCl4液體(用于除去ClO2中的未反應(yīng)的Cl2)。


(1)儀器P的名稱是__。
(2)寫出裝置A中燒瓶內(nèi)發(fā)生反應(yīng)的離子方程式__。
(3)B裝置中所盛試劑是__。
(4)F為ClO2收集裝置,應(yīng)選用的裝置是__(從①②③中選擇),其中與E裝置導(dǎo)管相連的導(dǎo)管口是__(填導(dǎo)管口的字母)
(5)相同條件下,ClO2的消毒能力是Cl2的__倍(以等物質(zhì)的量的消毒劑得電子的數(shù)目計算)。
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com