
| A.V正(H2O)=V正(H2) |
| B.容器中溫度不再發生改變 |
| C.消耗nmolH2同時消耗nmolCO |
| D.容器中氣體的總物質的量不隨時間改變 |
 CO(g)+H2(g)的平衡常數的數值為_________。在第5分鐘時將體系的溫發升高到T2,若在第8分鐘時達到新的平衡,請在下圖中畫出第5分鐘到9分鐘后c(H2O)濃度變化趨勢的曲線(只要求定性表示)。
CO(g)+H2(g)的平衡常數的數值為_________。在第5分鐘時將體系的溫發升高到T2,若在第8分鐘時達到新的平衡,請在下圖中畫出第5分鐘到9分鐘后c(H2O)濃度變化趨勢的曲線(只要求定性表示)。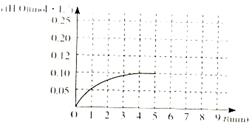
 CO(g)+H2(g) ?H=+131.6KJ/mol;(2)5C+3Fe2O3
CO(g)+H2(g) ?H=+131.6KJ/mol;(2)5C+3Fe2O3 CO2↑+4CO↑+6Fe;(3)B D (4)8.1
CO2↑+4CO↑+6Fe;(3)B D (4)8.1 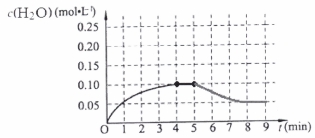
 CO(g)+H2(g) ?H=+131.6KJ/mol;(2) 赤鐵礦主要成分是Fe2O3,由于0.5mol碳完全反應得到0.6mol鐵,說明反應的Fe2O3的物質的量為0.3mol,因為同時生成2種常見氣體,則根據質量守恒定律可得該反應的化學方程式是5C+3Fe2O3
CO(g)+H2(g) ?H=+131.6KJ/mol;(2) 赤鐵礦主要成分是Fe2O3,由于0.5mol碳完全反應得到0.6mol鐵,說明反應的Fe2O3的物質的量為0.3mol,因為同時生成2種常見氣體,則根據質量守恒定律可得該反應的化學方程式是5C+3Fe2O3 CO2↑+4CO↑+6Fe;(3)A.在任何時刻都存在V正(H2O)=V正(H2)。所以不能由此確定反應達到平衡狀態。錯誤。B. 由于該反應伴隨著能量變化。如果反應未達到平衡,無論向那個方向進行,容器內的溫度必然發生改變。若容器中溫度不再發生改變,則單位時間內任何物質的濃度就不再變化,即反應達到了平衡狀態。正確。C.H2、CO都是生成物,在任何時刻都存在著消耗nmolH2同時消耗nmolCO 的關系,所以不能由此確定反應達到平衡狀態。錯誤。D.該反應是個反應前后氣體體積不等的反應,若容器中氣體的總物質的量不隨時間改變,必然反應達到了平衡狀態。正確。(4)化學平衡常數是可逆反應達到平衡狀態時個生成物濃度冪指數的乘積與各反應物濃度冪指數的乘積的比。當反應達到平衡狀態時,c(H2O)="0.10mol/L," c(H2)="c(CO)=0.9mol/L."
CO2↑+4CO↑+6Fe;(3)A.在任何時刻都存在V正(H2O)=V正(H2)。所以不能由此確定反應達到平衡狀態。錯誤。B. 由于該反應伴隨著能量變化。如果反應未達到平衡,無論向那個方向進行,容器內的溫度必然發生改變。若容器中溫度不再發生改變,則單位時間內任何物質的濃度就不再變化,即反應達到了平衡狀態。正確。C.H2、CO都是生成物,在任何時刻都存在著消耗nmolH2同時消耗nmolCO 的關系,所以不能由此確定反應達到平衡狀態。錯誤。D.該反應是個反應前后氣體體積不等的反應,若容器中氣體的總物質的量不隨時間改變,必然反應達到了平衡狀態。正確。(4)化學平衡常數是可逆反應達到平衡狀態時個生成物濃度冪指數的乘積與各反應物濃度冪指數的乘積的比。當反應達到平衡狀態時,c(H2O)="0.10mol/L," c(H2)="c(CO)=0.9mol/L." 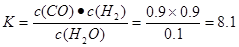 因為該反應的正反應為吸熱反應,所以升高溫度,化學平衡向正反應方向移動,當到8分鐘時達到那番話狀態。其變化曲線見答案。
因為該反應的正反應為吸熱反應,所以升高溫度,化學平衡向正反應方向移動,當到8分鐘時達到那番話狀態。其變化曲線見答案。

科目:高中化學 來源:不詳 題型:單選題
| A.將氯氣通入H2O2和NaOH的混合溶液中,發出紅光,說明反應物的總能量低于生成物的總能量,放出熱量 |
| B.1mol H2在氯氣中完全燃燒,放出180kJ熱量,則鍵能(E)的關系為E(H—H)=180kJ+2E(H—Cl)-E(Cl—Cl) |
| C.干燥的碘粉與鋁粉混合無明顯現象,滴上一滴水會冉冉升起紫色的碘蒸氣,最后得到白色AlI3。說明碘和鋁發生的反應是放熱反應 |
| D.精確實驗測得H2O在常溫下也能微弱電離:H2O??H++OH-,該過程是放熱過程 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
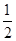 O2(g)=H2O(l)ΔH3=-285.84 kJ·mol-1
O2(g)=H2O(l)ΔH3=-285.84 kJ·mol-1查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2SO3(g)
2SO3(g) 

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| | Fe2O3 | CO | Fe | CO2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CH3OH(g) ΔH
CH3OH(g) ΔH
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 4NO(g) △H=+292.3kJ·mol—1,
4NO(g) △H=+292.3kJ·mol—1, N2(g)+2CO2(g) 的△H= ;
N2(g)+2CO2(g) 的△H= ; 2N2O5(g);已知體系中n(NO2)隨時間變化如下表:
2N2O5(g);已知體系中n(NO2)隨時間變化如下表:| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 O2(g)=H2 O(g) △H=-241.8kJ·mol-1
O2(g)=H2 O(g) △H=-241.8kJ·mol-1 O2(g)=CO(g) △H=-110.5kJ·mol-1
O2(g)=CO(g) △H=-110.5kJ·mol-1 2NO(g) △H
2NO(g) △H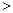 0,若1.0 mol空氣含0.80 mol N2和0.20 mol O2,1300oC時在1.0 L密閉容器內經過5s反應達到平衡,測得NO為8.0×10-4 mol。
0,若1.0 mol空氣含0.80 mol N2和0.20 mol O2,1300oC時在1.0 L密閉容器內經過5s反應達到平衡,測得NO為8.0×10-4 mol。 2CO2(g)+N2(g) 中,NO的濃度
2CO2(g)+N2(g) 中,NO的濃度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com