


 Fe3+(aq)+3OH-(aq) △H=a kJ/mol
Fe3+(aq)+3OH-(aq) △H=a kJ/mol H+(aq)+OH-(aq) △H=b kJ/mol
H+(aq)+OH-(aq) △H=b kJ/mol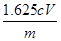 %或
%或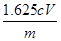 或
或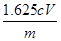 ×100% (2分,合理答案即可)
×100% (2分,合理答案即可) Fe(OH)3(aq) + 3H+(aq) △H=(3b-a)kJ·mol-1 (2分,化學式寫錯、表達式寫錯、不配平、漏寫物質狀態、漏寫單位均不得分)
Fe(OH)3(aq) + 3H+(aq) △H=(3b-a)kJ·mol-1 (2分,化學式寫錯、表達式寫錯、不配平、漏寫物質狀態、漏寫單位均不得分)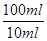 =0.01cVmol,因此氯化鐵的質量是0.01cVmol×162.5g/mol=1.625cVg,則樣品中氯化鐵的質量分數為
=0.01cVmol,因此氯化鐵的質量是0.01cVmol×162.5g/mol=1.625cVg,則樣品中氯化鐵的質量分數為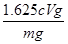 ×100%=
×100%=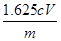 %。
%。 Fe3+(aq)+3OH-(aq) △H=a kJ/mol,②H2O(l)
Fe3+(aq)+3OH-(aq) △H=a kJ/mol,②H2O(l) H+(aq)+OH-(aq) △H=b kJ/mol,則根據蓋斯定律可知②×3-①即得到方程式)Fe3+(aq)+3H2O(l)
H+(aq)+OH-(aq) △H=b kJ/mol,則根據蓋斯定律可知②×3-①即得到方程式)Fe3+(aq)+3H2O(l) Fe(OH)3(aq) + 3H+(aq),所以該反應的反應熱△H=(3b-a)kJ·mol-1。
Fe(OH)3(aq) + 3H+(aq),所以該反應的反應熱△H=(3b-a)kJ·mol-1。

 計算高手系列答案
計算高手系列答案科目:高中化學 來源:不詳 題型:填空題
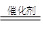 CH3OCH3+H2O
CH3OCH3+H2O CH3OCH3(g)+CO2(g) △H=-247kJ/mol
CH3OCH3(g)+CO2(g) △H=-247kJ/mol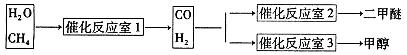
 CH3OCH3(g)+CO2(g)在密閉容器中達到平衡后,要提高CO的轉化率,可以采取的措施是
CH3OCH3(g)+CO2(g)在密閉容器中達到平衡后,要提高CO的轉化率,可以采取的措施是  CH3OH(g)+H2O (g) △H<0反應達到平衡時,改變溫度(T)和壓強(P),反應混合物CH3OH“物質的量分數”變化情況如圖所示,關于溫度(T)和壓強(P)的關系判斷正確的是 (填序號)
CH3OH(g)+H2O (g) △H<0反應達到平衡時,改變溫度(T)和壓強(P),反應混合物CH3OH“物質的量分數”變化情況如圖所示,關于溫度(T)和壓強(P)的關系判斷正確的是 (填序號)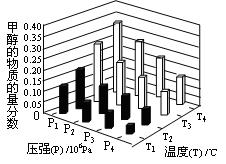
 CO(g)+3H2(g) △H>0寫出平衡常數的表達式:
CO(g)+3H2(g) △H>0寫出平衡常數的表達式: 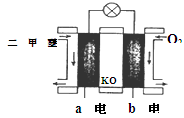
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 CO2(g) + 3H2(g) ;△H>0
CO2(g) + 3H2(g) ;△H>0
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2H2↑+O2↑
2H2↑+O2↑ 2H2↑+O2↑
2H2↑+O2↑ 2H2↑+O2↑
2H2↑+O2↑ CO+3H2
CO+3H2 CH3OH(g)+H2O(g) ΔH="-49.0" kJ/mol,測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g) ΔH="-49.0" kJ/mol,測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
 CH3OH(g)的平衡常數:
CH3OH(g)的平衡常數:| 溫度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常數 | 667 | 13 | 1.9×1 | 2.4×1 | 1×1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.-69.4 kJ·mol-1 | B.-45.2 kJ·mol-1 |
| C.+69.4 kJ·mol-1 | D.+45.2 kJ·mol-1 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.△H2-△H1 | B.△H2+△H1 | C.△H1-△H2 | D.-△H1-△H2 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.4a+4b+4c | B.2a-2b+6c |
| C.2a-2b+2c | D.2a-6b+2c |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g)
 Fe(s)+ CO2(g) ΔH=-23.5 kJ·mol-1,該反應在
Fe(s)+ CO2(g) ΔH=-23.5 kJ·mol-1,該反應在 CH3OH(g)。請根據圖示回答下列問題:
CH3OH(g)。請根據圖示回答下列問題: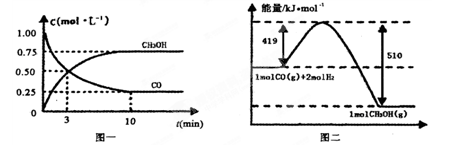
| 容器 | 反應物投入的量 | 反應物的 轉化率 | CH3OH的濃度 | 能量變化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ熱量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ熱量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ熱量 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

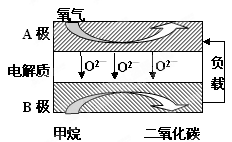
 2PbSO4+2H2O,請回答下列問題(不考慮氫、氧的氧化還原):
2PbSO4+2H2O,請回答下列問題(不考慮氫、氧的氧化還原): 
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com