
(1)常溫下,將2種一元酸分別和NaOH溶液等體積混合,實(shí)驗(yàn)數(shù)據(jù)如下:
| 組別 | 一元酸 | NaOH | pH |
| 甲 | c(HX)=0.1mol/L | c(NaOH)=0.1mol/L | pH=9 |
| 乙 | c(HY)=c1mol/L | c(NaOH)=0.1mol/L | pH=7 |
 CH3OH(g) △H
CH3OH(g) △H| 溫度 | 523K | 573K | 623K |
| 平衡常數(shù)(K) | 2.041 | 0.270 | 0.012 |
(17分)(1)①c(Na+)>c(Xˉ)>c(OHˉ)>c(H+)(2分) 10ˉ5(2分) ②=(1分)
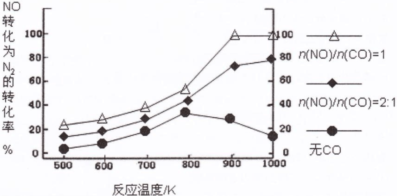
(2)①900K(1分,不寫單位或900℃不給分) n(NO)/n(CO)=1(1分,只寫1也給分)
②CH4+2NO2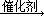 CO2+N2+2H2O(2分,化學(xué)式錯不給分,系數(shù)錯扣1分,不寫條件不扣分,用等號不扣分)
CO2+N2+2H2O(2分,化學(xué)式錯不給分,系數(shù)錯扣1分,不寫條件不扣分,用等號不扣分)
(3)①<(2分) ②523K(2分,不寫單位或523℃不給分)
③
(3分,每條曲線1分,標(biāo)注錯或坐標(biāo)數(shù)值錯不給分)
解析試題分析:(1)①HX與NaOH恰好完全中和,所得NaX溶液pH=9,說明NaX是強(qiáng)堿弱酸鹽,HX是弱酸;由于電離程度NaX>H2O,前者電離出的Xˉ部分水解,則混合溶液中c(Na+)>c(Xˉ)>c(OHˉ)>c(H+);H2O OHˉ+H+,NaX能促進(jìn)水的電離平衡右移,則水電離出的c(OHˉ)>10ˉ7mol/L,由pH=9可知溶液中c(H+)=10ˉ9mol/L<10ˉ7mol/L,由水的離子積可知,溶液中的c(OHˉ)=Kw/ c(H+)=10ˉ5mol/L>10ˉ7mol/L,所以混合溶液中水電離出的c(OHˉ)=10ˉ5mol/L;②HY是強(qiáng)酸,則NaY是強(qiáng)酸強(qiáng)堿鹽,混合溶液pH=7,說明HY與NaOH恰好完全中和,則c(HY)=c(NaOH)=0.1mol/L,所以c1=0.1;(2)①讀圖可知,相同溫度下,n(NO)/n(CO)越大,NO的轉(zhuǎn)化率越小;投料比最小時,溫度越高,NO轉(zhuǎn)化率越大,但是 900K時NO轉(zhuǎn)化率已經(jīng)接近100%,再升高溫度,需要消耗更多的能量,NO轉(zhuǎn)化率卻增加不大,得不償失,因此最佳溫度和投料比分別為900K、n(NO)/n(CO)=1;②根據(jù)題意可知反應(yīng)產(chǎn)物為CO2、N2、H2O,假設(shè)甲烷的系數(shù)為1,根據(jù)碳、氫、氧、氮原子個數(shù)守恒配平可得反應(yīng)式:CH4+2NO2
OHˉ+H+,NaX能促進(jìn)水的電離平衡右移,則水電離出的c(OHˉ)>10ˉ7mol/L,由pH=9可知溶液中c(H+)=10ˉ9mol/L<10ˉ7mol/L,由水的離子積可知,溶液中的c(OHˉ)=Kw/ c(H+)=10ˉ5mol/L>10ˉ7mol/L,所以混合溶液中水電離出的c(OHˉ)=10ˉ5mol/L;②HY是強(qiáng)酸,則NaY是強(qiáng)酸強(qiáng)堿鹽,混合溶液pH=7,說明HY與NaOH恰好完全中和,則c(HY)=c(NaOH)=0.1mol/L,所以c1=0.1;(2)①讀圖可知,相同溫度下,n(NO)/n(CO)越大,NO的轉(zhuǎn)化率越小;投料比最小時,溫度越高,NO轉(zhuǎn)化率越大,但是 900K時NO轉(zhuǎn)化率已經(jīng)接近100%,再升高溫度,需要消耗更多的能量,NO轉(zhuǎn)化率卻增加不大,得不償失,因此最佳溫度和投料比分別為900K、n(NO)/n(CO)=1;②根據(jù)題意可知反應(yīng)產(chǎn)物為CO2、N2、H2O,假設(shè)甲烷的系數(shù)為1,根據(jù)碳、氫、氧、氮原子個數(shù)守恒配平可得反應(yīng)式:CH4+2NO2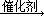 CO2+N2+2H2O;(3)①根據(jù)表中信息推斷,升高溫度平衡常數(shù)減小,前者說明平衡向吸熱方向移動,后者說明平衡向逆反應(yīng)方向移動,則逆反應(yīng)是吸熱反應(yīng),所以正反應(yīng)是△H<0的放熱反應(yīng);②根據(jù)各組分的變化濃度之比等于系數(shù)之比,可求平衡濃度:
CO2+N2+2H2O;(3)①根據(jù)表中信息推斷,升高溫度平衡常數(shù)減小,前者說明平衡向吸熱方向移動,后者說明平衡向逆反應(yīng)方向移動,則逆反應(yīng)是吸熱反應(yīng),所以正反應(yīng)是△H<0的放熱反應(yīng);②根據(jù)各組分的變化濃度之比等于系數(shù)之比,可求平衡濃度:
CO(g) + 2H2(g)  CH3OH(g)
CH3OH(g)
起始濃度/mol?Lˉ1 1 3 0
變化濃度/mol?Lˉ1 0.8 1.6 0.8
平衡濃度/mol?Lˉ1 0 .2 1.4 0.8
K=c(CH3OH)/[c(CO)?c2(H2)]=" 0.8/[0" .2×1.42]=2.041
與表中數(shù)據(jù)對比可知,平衡時溫度為523K。
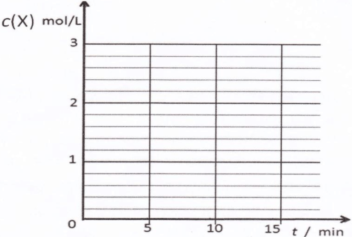
③畫圖要點(diǎn):a、起點(diǎn)時,t=0,c(CO)=1mol/L,c(H2)=3mol/L,c(CH3OH)=0;b、平衡點(diǎn)或拐點(diǎn)時,t=10min,c(CO)=0.2mol/L,c(H2)=1.4mol/L,c(CH3OH)=0.8mol/L;c、起點(diǎn)至平衡點(diǎn)或拐點(diǎn)時,反應(yīng)物濃度逐漸減小,生成物濃度逐漸增大,且各組分的變化濃度之比等于化學(xué)方程式中相應(yīng)的系數(shù)之比;平衡點(diǎn)或拐點(diǎn)之后,各組分的濃度保持不變。
考點(diǎn):考查化學(xué)反應(yīng)原理,涉及酸和堿混合溶液中離子濃度大小關(guān)系、鹽類水解、水的電離、化學(xué)平衡、化學(xué)方程式等考點(diǎn)。



| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源: 題型:填空題
一定溫度下,將3molA氣體和1molB氣體通過一密閉容器中,發(fā)生如下反應(yīng): 3A(g)+B (g) xC(g)。若容器體積固定為2L,反應(yīng)1min時測得剩余1.8molA,C的濃度為0.4mol/L。請?zhí)顚懴铝锌瞻祝?br />(1) x= ; 1min內(nèi),B的平均反應(yīng)速率為_________;
xC(g)。若容器體積固定為2L,反應(yīng)1min時測得剩余1.8molA,C的濃度為0.4mol/L。請?zhí)顚懴铝锌瞻祝?br />(1) x= ; 1min內(nèi),B的平均反應(yīng)速率為_________;
(2)若反應(yīng)經(jīng)2min達(dá)到平衡,平衡時C的濃度_________0.8mol/L(填“大于”、“等于”或“小于”);
(3)平衡混合物中,C的體積分?jǐn)?shù)為22%,若維持容器壓強(qiáng)不變,達(dá)到平衡時C的體積分?jǐn)?shù)_________22%,(填“大于”、“等于”或“小于”);
(4)若改變起始物質(zhì)加入的量,欲使反應(yīng)達(dá)到平衡時C的物質(zhì)的量分?jǐn)?shù)與原平衡相等,起始加入的三種物質(zhì)的物質(zhì)的量n(A)、n (B)、n(C)之間應(yīng)滿足的關(guān)系式__________________ 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
已知A(g)+B(g) C(g)+D(g)反應(yīng)的平衡常數(shù)和溫度的關(guān)系如下:
C(g)+D(g)反應(yīng)的平衡常數(shù)和溫度的關(guān)系如下:
| 溫度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常數(shù) | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
 A(g)+B(g)的平衡常數(shù)的值為 。
A(g)+B(g)的平衡常數(shù)的值為 。查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
(12分)工業(yè)制硫酸時,利用接觸氧化反應(yīng)將SO2轉(zhuǎn)化為SO3是一個關(guān)鍵的步驟。
(1)在接觸室中2SO2(g)+O2(g)  2SO3(g)達(dá)到平衡狀態(tài)的標(biāo)志是______。
2SO3(g)達(dá)到平衡狀態(tài)的標(biāo)志是______。
| A.υ(O2)正=2υ(SO2)逆 |
| B.容器中氣體的總質(zhì)量不隨時間而變化 |
| C.容器中氣體的顏色不隨時間而變化 |
| D.容器中氣體的壓強(qiáng)不隨時間而變化 |
 2SO3(g) ΔH<0。下列圖像中不正確的是______ (填字母序號)。
2SO3(g) ΔH<0。下列圖像中不正確的是______ (填字母序號)。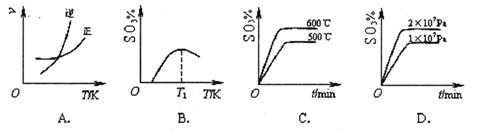
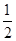 O2(g)
O2(g)  SO3(g) ΔH=-98KJ/mol
SO3(g) ΔH=-98KJ/mol查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
“潔凈煤技術(shù)”研究在世界上相當(dāng)普遍,科研人員通過向地下煤層氣化爐中交替鼓入空氣和水蒸氣的方法,連續(xù)產(chǎn)出了高熱值的煤炭氣,其主要成分是CO和H2。CO和H2可作為能源和化工原料,應(yīng)用十分廣泛。生產(chǎn)煤炭氣的反應(yīng)之一是:C(s)+H2O(g)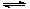 CO(g)+H2(g)?131.4 kJ。
CO(g)+H2(g)?131.4 kJ。
(1)在容積為3L的密閉容器中發(fā)生上述反應(yīng),5min后容器內(nèi)氣體的密度增大了0.12g/L,用H2O表示0~5miin的平均反應(yīng)速率為_________________________。
(2)能說明該反應(yīng)已達(dá)到平衡狀態(tài)的是________(選填編號)。
a.v正 (C)= v逆(H2O) b.容器中CO的體積分?jǐn)?shù)保持不變
c.c(H2)=c(CO) d.炭的質(zhì)量保持不變
(3)若上述反應(yīng)在t0時刻達(dá)到平衡(如圖),在t1時刻改變某一條件,請?jiān)谟覉D中繼續(xù)畫出t1時刻之后正反應(yīng)速率隨時間的變化: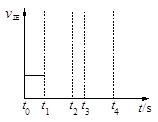
①縮小容器體積,t2時到達(dá)平衡(用實(shí)線表示);
②t3時平衡常數(shù)K值變大,t4到達(dá)平衡(用虛線表示)。
(4)在一定條件下用CO和H2經(jīng)如下兩步反應(yīng)制得甲酸甲酯:
①CO(g) + 2H2(g)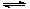 CH3OH(g) ②CO(g) + CH3OH(g)
CH3OH(g) ②CO(g) + CH3OH(g)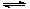 HCOOCH3(g)
HCOOCH3(g)
①反應(yīng)①中CO的平衡轉(zhuǎn)化率(α)與溫度、壓強(qiáng)的關(guān)系如圖所示。在不改變反應(yīng)物用量的情況下,為提高CO的轉(zhuǎn)化率可采取的措施是 。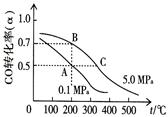
②已知反應(yīng)①中CO的轉(zhuǎn)化率為80%,反應(yīng)②中兩種反應(yīng)物的轉(zhuǎn)化率均為85%,則5.04kgCO最多可制得甲酸甲酯 kg。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
2012年冬季,我國城市空氣污染狀況受到人們的強(qiáng)烈關(guān)注,其中NOx、CO、SO2是主要污染性氣體。
I.汽車內(nèi)燃機(jī)工作時發(fā)生的反應(yīng)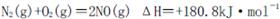 是導(dǎo)致汽車尾 氣中含有NO的重要原因之一。
是導(dǎo)致汽車尾 氣中含有NO的重要原因之一。
(1)有人欲選用合適的催化劑,使反應(yīng)2NO(g)=N2(g)+O2(g)能較快進(jìn)行以達(dá)到除去NO的目的。你認(rèn)為該反應(yīng)能否自發(fā)進(jìn)行 (填“能”或“不能”)。
(2)利用催化技術(shù)可將汽車尾氣中的NO氣體轉(zhuǎn)化成無毒氣體,相關(guān)反應(yīng)的平衡常數(shù)可表示為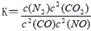 ,此反應(yīng)為放熱反應(yīng)。在一定溫度下,10L某密閉容器中發(fā)生上述反應(yīng),各物質(zhì)的物質(zhì)的量的變化情況如下表
,此反應(yīng)為放熱反應(yīng)。在一定溫度下,10L某密閉容器中發(fā)生上述反應(yīng),各物質(zhì)的物質(zhì)的量的變化情況如下表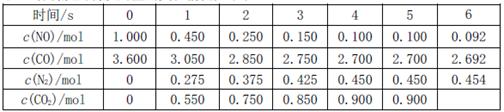
①根據(jù)土表數(shù)據(jù)計算0~4s間用NO表示的平均速率v(NO)= ;達(dá)到化學(xué)平衡時兩種反應(yīng)物的轉(zhuǎn)化率是否相等 (填“相等”或“不相等”)。
②在5~6s時,若K增大,5s后正反應(yīng)速率 (填“增大”或“減小”)
③在5~6s時,若K不變,以上各物質(zhì)的物質(zhì)的量變化原因可能是 。
A.選用更有效的催化劑 B.縮小容器的體積
C.降低CO2濃度 D.升高溫度
II為探究硫在氧氣中燃燒的產(chǎn)物里是否有SO3,某化學(xué)興趣小組在絕熱環(huán)境下進(jìn)行了定量實(shí)驗(yàn)探究。探究實(shí)驗(yàn)的相關(guān)數(shù)據(jù)如下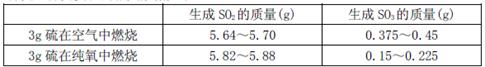
(3)對數(shù)據(jù)進(jìn)行分析可知,等質(zhì)量的硫在純氧中燃燒產(chǎn)生的SO3比在空氣中燃燒產(chǎn)生的SO3 (填“多”或“少”),原因可能是 。
A.純氧中氧氣濃度高,有利于化學(xué)平衡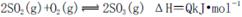 向右移動
向右移動
B.化學(xué)反應(yīng)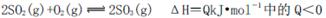
C.純氧中氧氣濃度高,單位時間內(nèi)發(fā)熱量大,致使反應(yīng)體系的溫度較高,不利于化學(xué)平衡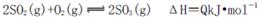 向右移動
向右移動
D.3g硫在純氧中燃燒比3g硫在空氣中燃燒放出的熱量多,不利于化學(xué)平衡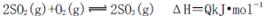 向右移動
向右移動
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
某溫度時,在3L密閉容器中,X、Y、Z三種物質(zhì)的物質(zhì)的量隨時間變化的曲線如圖所示。由圖中數(shù)據(jù)分析:
(1)該反應(yīng)的化學(xué)方程式: ;
(2)反應(yīng)開始至2min末,X的反應(yīng)速率為 ;
(3)該反應(yīng)是由 開始反應(yīng)的。(?正反應(yīng)?逆反應(yīng)?正逆反應(yīng)同時。)
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:填空題
在下列事實(shí)中,什么因素影響了化學(xué)反應(yīng)速率?
①天的食品易霉變,冬天就不易發(fā)生該現(xiàn)象 。
②熔化的氯酸鉀放出氣泡較慢,撒入少量二氧化錳很快產(chǎn)生氣體 。
③工業(yè)上常將固體燃料粉碎,以提高燃燒效率 。
④同體積、同濃度的鹽酸與同樣大小的鋅條和鎂條反應(yīng),產(chǎn)生氣體前慢后快 。
⑤同體積、同濃度的硫酸和鹽酸與同樣大小質(zhì)量相等的鋅粒反應(yīng),產(chǎn)生氣體前者快 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:問答題
氮的固定有三種途徑:生物固氮、自然固氮和工業(yè)固氮。根據(jù)最新“人工固氮”的研究報道:在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3的TiO2)表面與水發(fā)生反應(yīng),生成的主要產(chǎn)物為NH3。進(jìn)一步研究NH3生成量與溫度的關(guān)系,部分實(shí)驗(yàn)數(shù)據(jù)見下表(光照、N2壓力1.0×105 Pa、反應(yīng)時間1 h):
| T/K | 303 | 313 | 323 | 353 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 | 2.0 |
 4NH3(g)+3O2(g)ΔH=a kJ·mol-1
4NH3(g)+3O2(g)ΔH=a kJ·mol-1 2NH3(g) ΔH=-92 .4 kJ·mol-1
2NH3(g) ΔH=-92 .4 kJ·mol-1 2NH3(g) ΔH=-92 .4 kJ·mol-1,分別研究在T1、T2和T3(T1<T2<T3)三種溫度下合成氨氣的規(guī)律。下圖是上述三種溫度下不同的H2和N2的起始組成比(起始時N2的物質(zhì)的量均為1 mol)與N2平衡轉(zhuǎn)化率的關(guān)系。請回答:
2NH3(g) ΔH=-92 .4 kJ·mol-1,分別研究在T1、T2和T3(T1<T2<T3)三種溫度下合成氨氣的規(guī)律。下圖是上述三種溫度下不同的H2和N2的起始組成比(起始時N2的物質(zhì)的量均為1 mol)與N2平衡轉(zhuǎn)化率的關(guān)系。請回答: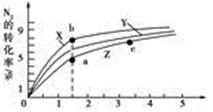
 N2(g)+3H2(g)的平衡常數(shù)為________ 。
N2(g)+3H2(g)的平衡常數(shù)為________ 。查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com