
運用化學反應原理研究氮、氧等單質及其化合物的反應有重要意義。
(1)合成氨反應N2 (g)+3H2(g)![]() 2NH3(g),若在恒溫、恒壓條件下向平衡體系中通入氬氣,則平衡 移動(填“向左”“向右”或“不”);使用催化劑,上述反應的△H________(填“增大” “減小” 或“不改變”)。
2NH3(g),若在恒溫、恒壓條件下向平衡體系中通入氬氣,則平衡 移動(填“向左”“向右”或“不”);使用催化劑,上述反應的△H________(填“增大” “減小” 或“不改變”)。
(2)甲烷在高溫下與水蒸氣反應的方程式為:CH4+H2O=CO+3H2。已知部分物質燃燒的熱化學方程式如下:
2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H=-566kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ·mol-1
又知1molH2O(g)轉變為1mol H2O(l)時放出44.0kJ熱量。寫出CH4和H2O在高溫下反應的熱化學方程式 。
(3)在25℃下,向濃度均為0.1 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化學式),生成該沉淀的離子方程式為_____ _______。已知25℃時Ksp[Mg(OH)2]=1.8×10-11,KsP [Cu(OH)2]=2.2×10-20。
(4)有人設想尋求合適的催化劑和電極材料,以N2、H2為電極反應物,以HCl—NH4Cl為電解質溶液制造新型燃燒電池。請寫出該電池的正極反應式 。
(5)某溫度(t℃)時,測得0.01mol·L-1的NaOH溶液的pH=11。在此溫度下,將pH=a的H2SO4溶液VaL與pH=b的NaOH溶液VbL混合,若所得混合液為中性,且a+b=12,則Va︰Vb= 。
(6)在25℃下,將a mol·L-1的氨水![]() 與0.01 mol·L-1的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-)。則溶液顯_____________性(填“酸”“堿”或“中”);用含a的代數式表示NH3·H2O的電離常數Kb
與0.01 mol·L-1的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-)。則溶液顯_____________性(填“酸”“堿”或“中”);用含a的代數式表示NH3·H2O的電離常數Kb![]() =__________。
=__________。
(1)向左; 不改變(各2分)
(2)CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.1kJ·mol-1(2分)
(3)Cu(OH)2(2分); 2NH3·H2O+Cu2+=Cu(OH)2↓+2NH4*;(2分)
(4)N2+8H++6e-=2NH4—(2分)
(5)1 ︰ 10(2分)
(6)中(2分); mol·L-1(2分)
(1)恒溫恒壓下通入氬氣,體積增大,所以平衡向左移動;使用催化劑與反應熱無關。
(2)根據蓋斯定律即可得熱化學方程式為CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.1kJ·mol-1
(3)已知25℃時Ksp[Mg(OH)2]=1.8×10-11,KsP [Cu(OH)2]=2.2×10-20,所以先生成Cu(OH)2
(4)以N2、H2為電極反應物,則總反應為N2+3H2![]() 2NH3,由于HCl—NH4Cl為電解質溶液所以正極反應方程式為N2+8H++6e-=2NH4—
2NH3,由于HCl—NH4Cl為電解質溶液所以正極反應方程式為N2+8H++6e-=2NH4—
(5)因為0.01mol·L-1的NaOH溶液的pH=11所以此溫度下Kw=10-13,由此可得10-a×Va=10b-13×Vb,則Va:Vb=1:10
(6)由電荷守恒c(H+)+c(NH4+)= c(OH-)+c(Cl-)可得,c(H+)= c(OH-)顯中性。
K= c(NH4+) c(OH-)÷c(NH3·H2O)=0.01×10-7÷(a-0.01)= mol·L-1


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:閱讀理解
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
+ 2 |
- 6 |
+ 2 |
- 6 |
+ 4 |
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
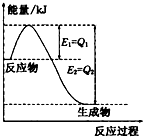 運用化學反應原理研究氮、氯、碘等單質及其化合物的反應有重要意義.
運用化學反應原理研究氮、氯、碘等單質及其化合物的反應有重要意義.
| ||
| (一定條件) |
| b×10-7 |
| a-b |
| b×10-7 |
| a-b |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| 10-7y |
| x-y |
| 10-7y |
| x-y |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com