
(9分)美國(guó)Bay等工廠使用石油熱裂解的副產(chǎn)物甲烷來(lái)制取氫氣,其生產(chǎn)流程如
下圖:
(1)此流程的第II步反應(yīng)為:CO(g)+H2O(g) H2(g)+CO2(g),該反應(yīng)的化學(xué)平衡常數(shù)表達(dá)式為K= ;反應(yīng)的平衡常數(shù)隨溫度的變化如表一,
H2(g)+CO2(g),該反應(yīng)的化學(xué)平衡常數(shù)表達(dá)式為K= ;反應(yīng)的平衡常數(shù)隨溫度的變化如表一,
| 溫度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常數(shù)K | 10 | 9 | 1 | 0.6 |
 H2(g)+CO2(g),在830℃,以表二的物質(zhì)的量(單位為mol)投入恒容反應(yīng)器發(fā)生上述反應(yīng),其中反應(yīng)開始時(shí),向正反應(yīng)方向進(jìn)行的有 (填實(shí)驗(yàn)編號(hào));
H2(g)+CO2(g),在830℃,以表二的物質(zhì)的量(單位為mol)投入恒容反應(yīng)器發(fā)生上述反應(yīng),其中反應(yīng)開始時(shí),向正反應(yīng)方向進(jìn)行的有 (填實(shí)驗(yàn)編號(hào));| 實(shí)驗(yàn)編號(hào) | N(CO) | N(H2O) | n(H2) | N(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
 達(dá)到平衡、在時(shí)刻t
達(dá)到平衡、在時(shí)刻t 分別因改變某個(gè)條件而發(fā)生變化的情況:圖中時(shí)刻t
分別因改變某個(gè)條件而發(fā)生變化的情況:圖中時(shí)刻t 發(fā)生改變的條件是_________。(寫出兩種)
發(fā)生改變的條件是_________。(寫出兩種)

| 年級(jí) | 高中課程 | 年級(jí) | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來(lái)源: 題型:閱讀理解
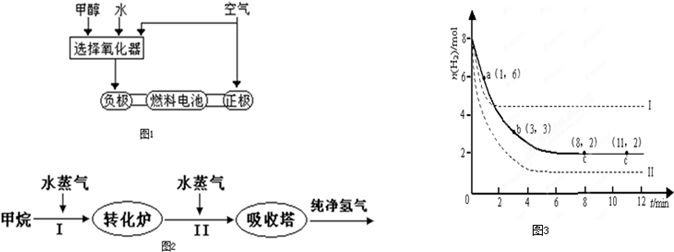
 美國(guó)Bay等工廠使用石油熱裂解的副產(chǎn)物甲烷來(lái)制取氫氣,其生產(chǎn)流程如圖1:
美國(guó)Bay等工廠使用石油熱裂解的副產(chǎn)物甲烷來(lái)制取氫氣,其生產(chǎn)流程如圖1:| c(H2)c(CO2) |
| c(CO)c(H2O) |
| c(H2)c(CO2) |
| c(CO)c(H2O) |
| 溫度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常數(shù)K | 10 | 9 | 1 | 0.6 |
| 實(shí)驗(yàn)編號(hào) | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:閱讀理解
| 高溫 |
| 溫度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常數(shù)K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:
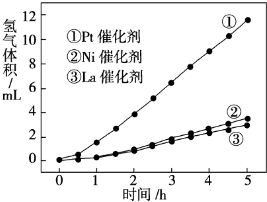
| 溫度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常數(shù)K | 10 | 9 | 1 | 0.6 |
| 實(shí)驗(yàn)編號(hào) | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:閱讀理解
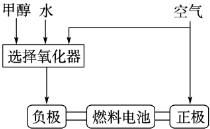
(14分)美國(guó)Bay等工廠使用石油熱裂解的副產(chǎn)物甲烷來(lái)制取氫氣,其生產(chǎn)流程如下圖:
(1)此流程的第II步反應(yīng)為:CO(g)+H2O(g)H2(g)+CO2(g),該反應(yīng)的平衡常數(shù)隨溫度的變化如下表:
| 溫度/℃ | 400 | 500 | 830 |
| 平衡常數(shù)K | 10 | 9 | 1 |
從上表可以推斷:此反應(yīng)是 (填“吸”或“放”)熱反應(yīng)。在830℃下,若開始時(shí)向恒容密閉容器中充入1mo1CO和2mo1H2O,則達(dá)到平衡后CO的轉(zhuǎn)化率為 。
(2)在500℃,以下表的物質(zhì)的量(按照CO、H2O、H2、CO2的順序)投入恒容密閉容器中進(jìn)行上述第II步反應(yīng),達(dá)到平衡后下列關(guān)系正確的是
| 實(shí)驗(yàn)編號(hào) | 反應(yīng)物投入量 | 平衡時(shí)H2濃度 | 吸收或放出的熱量 | 反應(yīng)物轉(zhuǎn)化率 |
| A | 1、1、0、0 | c1 | Q1 | α1[來(lái)源:] |
| B | 0、0、2、2 | c2 | Q2 | α2
|
| C | 2、2、0、0 | c3 | Q3 | α3 |
A.2c1= c2 =c3 B.2Q1=Q2=Q3 C.α1 =α2 =α3 D.α1 +α2 =1
(3)在一個(gè)絕熱等容容器中,不能判斷此流程的第II步反應(yīng)達(dá)到平衡的是 。
①體系的壓強(qiáng)不再發(fā)生變化 ②混合氣體的密度不變
③混合氣體的平均相對(duì)分子質(zhì)量不變 ④各組分的物質(zhì)的量濃度不再改變
⑤體系的溫度不再發(fā)生變化 ⑥v(CO2)正=v(H2O)逆
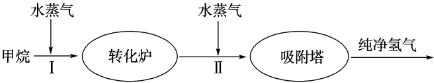
(4)下圖表示此流程的第II步反應(yīng),在t1時(shí)刻達(dá)到平衡、在t2時(shí)刻因改變某個(gè)條件濃度發(fā)生變化的情況:圖中t2時(shí)刻發(fā)生改變的條件是 、
(寫出兩種)。若t4時(shí)刻通過(guò)改變?nèi)莘e的方法將壓強(qiáng)增大為原先的兩倍,在圖中t4和t5區(qū)間內(nèi)畫出CO、CO2濃度變化曲線,并標(biāo)明物質(zhì)(假設(shè)各物質(zhì)狀態(tài)均保持不變)。
查看答案和解析>>
科目:高中化學(xué) 來(lái)源: 題型:閱讀理解
(9分)美國(guó)Bay等工廠使用石油熱裂解的副產(chǎn)物甲烷來(lái)制取氫氣,其生產(chǎn)流程如
下圖:
(1)此流程的第II步反應(yīng)為:CO(g)+H2O(g) H2(g)+CO2(g),該反應(yīng)的化學(xué)平衡常數(shù)表達(dá)式為K= ;反應(yīng)的平衡常數(shù)隨溫度的變化如表一,
| 溫度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常數(shù)K | 10 | 9 | 1 | 0.6 |
從上表可以推斷:此反應(yīng)是_______________ (填“吸”、“放”)熱反應(yīng)。在830℃下,若開始時(shí)向恒容密閉容器中充入CO與HzO均為1 mo1,則達(dá)到平衡后CO的轉(zhuǎn)化率為_____。
(2)此流程的第II步反應(yīng)CO(g)+H2O(g) H2(g)+CO2(g),在830℃,以表二的物質(zhì)的量(單位為mol)投入恒容反應(yīng)器發(fā)生上述反應(yīng),其中反應(yīng)開始時(shí),向正反應(yīng)方向進(jìn)行的有 (填實(shí)驗(yàn)編號(hào));
| 實(shí)驗(yàn)編號(hào) | N(CO) | N(H2O) | n(H2) | N(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |
(3)在一個(gè)不傳熱的固定容積的容器中,判斷此流程的第II步反應(yīng)達(dá)到平衡的標(biāo)志是
① 體系的壓強(qiáng)不再發(fā)生變化 ②混合氣體的密度不變 ③混合氣體的平均相對(duì)分子質(zhì)量不變 ④ 各組分的物質(zhì)的量濃度不再改變 ⑤ 體系的溫度不再發(fā)生變化 ⑥ v(CO2正)= v(H2O逆)
(4) 圖表示該反應(yīng)此流程的第II步反應(yīng)在時(shí)刻t![]() 達(dá)到平衡、在時(shí)刻t
達(dá)到平衡、在時(shí)刻t![]() 分別因改變某個(gè)條件而發(fā)生變化的情況:圖中時(shí)刻t
分別因改變某個(gè)條件而發(fā)生變化的情況:圖中時(shí)刻t![]() 發(fā)生改變的條件是_________。(寫出兩種)
發(fā)生改變的條件是_________。(寫出兩種)
(5)若400℃時(shí),第Ⅱ步反應(yīng)生成l mol氫氣的熱量數(shù)值為 33.2(單位為kJ),第Ⅰ步反應(yīng)的熱化學(xué)方程式為: CH4(g)+H2O(g)=3H2(g)+CO(g)△H=-103.3kJ·mol-1。則400℃時(shí),甲烷和水蒸氣反應(yīng)生成二氧化碳和氫氣的熱化學(xué)方程式為 。
查看答案和解析>>
國(guó)際學(xué)校優(yōu)選 - 練習(xí)冊(cè)列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺(tái) | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無(wú)主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com