
【題目】設NA表示阿伏加德羅常數的值。下列說法正確的是
A.15g 14CO與15N2的混合氣體所含質子數為7.5NA
B.11.2L Cl2與NaOH溶液反應,轉移電子數為0.5NA
C.2mol SO2與1mol O2反應生成SO3的分子數為2NA
D.6g MgSO4與NaHSO4的混合物所含氧原子數為0.2NA
【答案】D
【解析】
A.14CO與15N2的摩爾質量都是30g·mol 1,并且1個14CO分子與1個15N2分子所含的質子數都是14,所以15 g 14CO與15N2的混合氣體的物質的量為![]() =0.5mol,所含的質子數為7NA,A錯誤;
=0.5mol,所含的質子數為7NA,A錯誤;
B.未指明標況, 11.2L Cl2的物質的量無法確定,B錯誤;
C.SO2與 O2在一定條件下反應生成SO3的反應是一個可逆反應,反應物的轉化率小于100%,故2mol SO2與1mol O2反應生成SO3的分子數小于2NA,C錯誤;
D.MgSO4與NaHSO4的摩爾質量都是120g·mol 1,6g MgSO4與NaHSO4的混合物的物質的量為![]() =0.05mol,所含氧原子數為4×0.05mol×NA=0.2NA,D正確;
=0.05mol,所含氧原子數為4×0.05mol×NA=0.2NA,D正確;
答案選D。


科目:高中化學 來源: 題型:
【題目】反應4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),H=-akJmol-1,在5L密閉容器投入1molNH3和1mol的O2,2分鐘后NO的物質的量增加了0.4mol,下列說法正確的是( )
4NO(g)+6H2O(g),H=-akJmol-1,在5L密閉容器投入1molNH3和1mol的O2,2分鐘后NO的物質的量增加了0.4mol,下列說法正確的是( )
A.2分鐘反應放出的熱量值小于0.1akJ
B.用氧氣表示0~2min的反應速率:v(O2)=0.05mol·L-1·min-1
C.2分鐘內NH3的轉化率是50%
D.2分鐘末c(H2O)=0.6mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為驗證鹵素單質氧化性的相對強弱,某學習小組用如圖所示裝置進行實驗(夾持儀器已略去,氣密性已檢驗).

實驗過程:
Ⅰ.打開彈簧夾,打開活塞a,滴加濃鹽酸.
Ⅱ.當B和C中的溶液都變為黃色時,夾緊彈簧夾.
Ⅲ.當B中溶液由黃色變為棕紅色時,關閉活塞a.
Ⅳ.
(1)A中產生黃綠色氣體,其電子式是 ______;A中使用KMnO4可以在不加熱的情況下與濃鹽酸發生反應。如果改用二氧化錳,則在加熱條件下發生的化學反應方程式為______。
(2)驗證氯氣的氧化性強于碘的實驗現象是 ______ 。
(3)B中溶液發生反應的離子方程式是 ______ 。
(4)為驗證溴的氧化性強于碘,過程Ⅳ的操作和現象是 ______。
(5)過程Ⅲ實驗的目的是 ______ 。
(6)實驗結論:氯、溴、碘單質的氧化性逐漸 ______ ,原因是:同主族元素從上到下 ______ ,得電子能力逐漸 ______ 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下,向1L恒容密閉容器中通入2mol CO2和8mol H2發生反應:CO2(g) +4H2(g)![]() CH4(g) +2H2O(g) ,5min后,測得CO2的物質的量為1.2mol ,則0~5min內用H2表示的化學反應速率是
CH4(g) +2H2O(g) ,5min后,測得CO2的物質的量為1.2mol ,則0~5min內用H2表示的化學反應速率是
A.0.16mol·L-1·min -1B.0.24mol·L-1·min -1C.0.64mol·L-1·min -1D.0.96mol·L-1·min -1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表是打開物質世界奧秘之門的一把金鑰匙 ,1869年,門捷列夫發現了元素周期律并發表了元素周期表。下圖為元素周期表的一部分,回答下列問題。

(1).上述元素中化學性質最穩定的是________(填元素符號,下同) ,非金屬性最強的是_____。
(2)c的最高價氧化物對應水化物的化學式為__________。
(3)h元素的原子結構示意圖為__________,寫出h單質的一種用途:__________。
(4)b、d、f三種元素原子半徑由大到小的順序是__________(用元素符號表示)。
(5)a、g、j的氫氧化物中堿性最強的是__________(填化學式),寫出其溶液與g的氧化物反應的離子方程式:___________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸鋁主要用作造紙工業中的沉淀劑和飲用水的絮凝劑。用鋁灰(Al2O3、SiO2和少量鐵的氧化物)制備硫酸鋁晶體[Al2(SO4)3·18H2O]的工藝流程如圖所示:
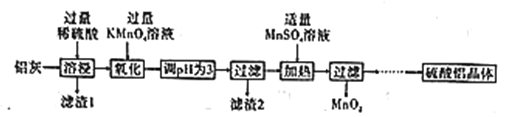
(1)濾渣1的化學式為____。
(2)“氧化”步驟的離子方程式為____。
(3)已知:相關離子生成氫氧化物沉淀的pH范圍如表:
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
開始沉淀時 | 3.4 | 6.3 | 1.5 |
完全沉淀時 | 4.7 | 8.3 | 2.8 |
根據表中數據解釋調節pH為3的目的是________。
(4)“加熱”步驟中反應的生成物中氧化產物與還原產物的物質的量之比為_____。
(5)“…”中一系列操作是___、冷卻結晶、過濾、___、干燥。
(6)硫酸鋁晶體加熱發生分解的失重曲線如圖所示,主要分為三個階段:第一階段失重40.54%,第二階段失重48.65%,第三階段失重84.68%,以后不再失重。
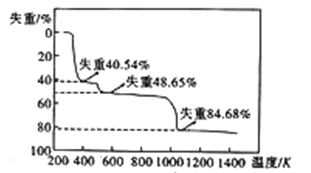
①失重第一階段殘留固體的化學式為_________。
②失重第三階段反應的化學方程式為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】取 1LFeCl3 溶液腐蝕銅板制作電路板,反應后在此殘留液中慢慢加入鐵粉,溶液中 Fe2+的濃度變化如圖所示(加入固體引起的體積變化忽略不計),下列說法不正確的是

A. 當n(Fe)=0.5mol 時,發生的離子反應為 Fe+2Fe3+=3Fe2+
B. 當 n(Fe)=1.5mol 時,溶液中發生的總反應離子方程式為4Fe3++Cu2++3Fe=7Fe2++Cu
C. 當n(Fe)=1mol 時,溶液中 c(Fe2+)=5 mol·L-1
D. 腐蝕之前原溶液中 c(Fe3+)=4 mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】脂環烴分子中兩個或兩個以上碳環共有兩個以上碳原子的烴稱為橋環烴,二環[4.1.0]庚烷(![]() )是一種典型的橋環烴,下列關于二環[4.1.0]庚烷的說法錯誤的是( )
)是一種典型的橋環烴,下列關于二環[4.1.0]庚烷的說法錯誤的是( )
A. 與環庚烯互為同分異構體
B. 所有的碳原子均在同一平面上
C. 一氯代物有4種(不考慮立體異構)
D. 1mol二環[4.1.0]庚烷完全燃燒時消耗10molO2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com