(1)由表可知,溫度越高,平衡常數越小,反應進行程度越小,平衡向逆反應移動,升高溫度平衡向吸熱方向移動,故正反應為放熱反應,故答案為:放熱;
(2)A、加入催化劑只改變反應速率不改變化學平衡,故A錯誤;
B、增大CO的物質的量以提高體系的壓強,CO(g)+H
2O(g)?H
2(g)+CO
2(g)反應是氣體物質的量不變的反應,增大一氧化碳物質的量平衡正向進行,容器內氣體物質的量增大,壓強增大,故B正確;
C、反應是放熱反應,降溫,速率減小平衡正向進行,故C錯誤;
D、減小氫氣濃度,平衡正向進行,但速率減小,故D錯誤;
故選ACD.
(3)向某密閉容器中充入2molCO和4molH
2O(g),CO(g)+H
2O(g)?H
2(g)+CO
2(g),當反應達平衡時,CO的體積分數為X;
A、采用極限分析法,1molCO(g)+4molH
2O+2molCO
2(g)+2molH
2(g),假如反應完全轉化為CO和H
2O物質的量為:3mol:6mol=1:2,反應前后氣體體積不變,平衡相同,CO的體積分數為x,故A不符合;
B、采用極限分析法,2molCO(g)+2molH
2O+2molCO
2(g)+2molH
2(g),假如反應完全轉化為CO和H
2O物質的量為:3mol:3mol=1:1,反應前后氣體體積不變,平衡正向進行,CO的體積分數大于x,故B符合;
C、采用極限分析法,1molCO(g)+3molH
2O+0.8molCO
2(g)+0.8molH
2(g),假如反應完全轉化為CO和H
2O物質的量為:1.8mol:3.8mol=9:19,反應前后氣體體積不變,平衡正向進行,CO的體積分數小于x,故C符合;
D、采用極限分析法,1molCO(g)+3molH
2O+1molCO
2(g)+1molH
2(g),假如反應完全轉化為CO和H
2O物質的量為2mol:4mol=1:2,當反應達到平衡時,CO的體積分數為x.故D不符合;
故選BC.
(4)因800℃時反應平衡常數為1.
CO(g)+H
2O(g)?H
2(g)+CO
2(g),
起始:5(1-x) 5x 0 0
轉化:5(1-x)y 5(1-x)y 5(1-x)y 5(1-x)y
平衡:5(1-x)(1-y)5(x-y+xy) 5(1-x)y 5(1-x)y
所以平衡常數k=
=
| 5(1-x)y×5(1-x)y |
| 5(1-x)(1-y)×5(x-y+xy) |
=1,解得y=x,
故答案為:y=x;
(5)由方程式CO(g)+H
2O(g)?H
2(g)+CO
2(g)可知,有1molCO反應則生成1molH
2,開始通入10molCO,所以平衡時,CO、H
2的物質的量共為10mol.則平均燃燒熱為
=284.5kJ/mol,
利用平均值法計算CO、H
2的物質的量之比,設CO、H
2物質的量為x、y;
x+y=10
283x+286y=2845
計算得到x=y=5mol;
利用三段式法求出平衡時各組分的物質的量,
CO(g)+H
2O(g)?H
2(g)+CO
2(g),
起始:10mol 10mol 0 0
轉化:5mol 5 mol 5mol 5mol
平衡:5mol 5mol 5mol 5mol
所以常數平衡常數為K=
=
=1;
圖表分析可知溫度為800°C,T=273+800=1073K
故答案為:1;1073;



 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案 H2(g)+CO2(g)的平衡常數隨溫度的變化如表:
H2(g)+CO2(g)的平衡常數隨溫度的變化如表: 2CO(g)平衡常數K;
2CO(g)平衡常數K; CO(g)+H2(g) 平衡常數K1;
CO(g)+H2(g) 平衡常數K1; H2(g)+CO2(g) 平衡常數K2,
H2(g)+CO2(g) 平衡常數K2,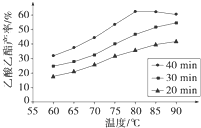 Ⅰ工業上常利用醋酸和乙醇合成有機溶劑乙酸乙酯:CH3COOH(l)+C2H5OH(l)
Ⅰ工業上常利用醋酸和乙醇合成有機溶劑乙酸乙酯:CH3COOH(l)+C2H5OH(l)