Ⅰ.某研究性學(xué)習(xí)小組用10g膽礬制取CuO,并證明CuO可以催化H
2O
2的分解反應(yīng).
(1)首先制備CuO,實驗步驟如下,請完成缺少的步驟:
①稱取10g膽礬,放入小燒杯中,再加水溶解;②向小燒杯中滴加NaOH溶液,至產(chǎn)生大量沉淀;③用酒精燈在石棉網(wǎng)上加熱小燒杯,至沉淀物完全黑色;④將以上混合物過濾,洗滌,
干燥
干燥
,然后研細(xì);⑤檢查④中洗滌是否完全的操作是
取最后幾滴洗滌液,加入BaCl2溶液,若無渾濁,證明沉淀已洗凈
取最后幾滴洗滌液,加入BaCl2溶液,若無渾濁,證明沉淀已洗凈
.
(2)用圖1所示,按表中設(shè)計實驗方法,證明CuO能催化7%H
2O
2溶液的分解,并與MnO
2的催化效果進(jìn)行比較.
| 實驗序號 |
雙氧水體積 |
催化劑 |
待測數(shù)據(jù) |
| a |
15mL |
無 |
|
| b |
15mL |
0.5g CuO |
|
| c |
15mL |
0.5g MnO2 |
|
①從設(shè)計原理看,實驗中的待測數(shù)據(jù)是
相同時間內(nèi)產(chǎn)生氣體的體積(或產(chǎn)生相同體積氣體所需要的時間)
相同時間內(nèi)產(chǎn)生氣體的體積(或產(chǎn)生相同體積氣體所需要的時間)
.
②為探究CuO在實驗b中是否起催化作用,除與
a比較外,還應(yīng)補充以下實驗(不必寫具體操作):
A.證明CuO化學(xué)性質(zhì)在反應(yīng)前后是否改變;
B.
CuO的質(zhì)量在反應(yīng)前后是否發(fā)生改變
CuO的質(zhì)量在反應(yīng)前后是否發(fā)生改變
.
Ⅱ.摩爾鹽[(NH
4)
2SO
4?FeSO
4?6H
2O]
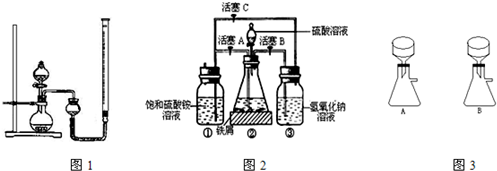
在空氣中比一般亞鐵鹽穩(wěn)定,是化學(xué)分析中常用的還原劑.某研究性學(xué)習(xí)小組用圖2所示的實驗裝置來制取摩爾鹽,實驗步驟如下,回答下列問題:
(1)用30%的NaOH溶液和廢鐵屑(含少量油污、鐵銹、FeS等)混合、煮沸、冷卻、分離,將分離出的NaOH溶液裝入③中.
(2)利用容器②的反應(yīng),向容器①中通入氫氣,應(yīng)關(guān)閉活塞
A
A
,打開活塞
B、C
B、C
(填字母).向容器①中通入氫氣的目的是
趕走硫酸銨溶液中的溶解O2和容器①液面上部的O2,防止Fe2+被氧化為Fe3+
趕走硫酸銨溶液中的溶解O2和容器①液面上部的O2,防止Fe2+被氧化為Fe3+
.
(3)待錐形瓶中的鐵屑快反應(yīng)完時,關(guān)閉活塞B、C,打開活塞A,繼續(xù)產(chǎn)生的氫氣會將錐形瓶中的硫酸亞鐵(含極少部分未反應(yīng)的稀硫酸)壓到飽和硫酸銨溶液的底部.在常溫下放置一段時間,試劑瓶底部將結(jié)晶出硫酸亞鐵銨,抽濾,制得硫酸亞鐵銨晶體.圖3是抽濾裝置的一部分,其中正確的是
A
A
.(填A(yù)或B)
(4)為了確定產(chǎn)品中亞鐵離子的含量,研究小組用滴定法來測定.若取產(chǎn)品24.50g配成100mL溶液,取出10.00mL用0.1000mol?L
-1KMnO
4酸性溶液滴定,消耗KMnO
4溶液10.00mL.
已知高錳酸鉀與Fe
2+的離子方程式為:MnO
+5Fe
2++8H
+=Mn
2++5Fe
3++4H
2O
試求產(chǎn)品中摩爾鹽的質(zhì)量分?jǐn)?shù)
80%
80%
.(NH
4)
2SO
4?FeSO
4?6H
2O的相對分子質(zhì)量為392.




 全能練考卷系列答案
全能練考卷系列答案