
已知甲為恒壓容器、乙為恒容容器。相同條件下充入等物質的量的NO2氣體,且起始時體積相同。發生反應:2NO2(g)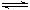 N2O4 (g) △H<0。一段時間后相繼達到平衡狀態。下列說法中正確的是
N2O4 (g) △H<0。一段時間后相繼達到平衡狀態。下列說法中正確的是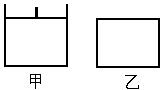
| A.平衡時NO2體積分數:甲<乙 |
| B.達到平衡所需時間,甲與乙相等 |
| C.該反應的平衡常數表達式K=c(N2O4)/c(NO2) |
| D.若兩容器內氣體的壓強保持不變,均說明反應已達到平衡狀態 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:單選題
已知:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O,下列各組實驗中,反應速率最快的是
| 組號 | 反應溫 度/℃ | Na2S2O3 | H2SO4 | H2O體積/mL | ||
| 體積/mL | 濃度/mol·L-1 | 體積/mL | 濃度/mol·L-1 | |||
| A | 10 | 5 | 0.2 | 5 | 0.1 | 10 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一定條件下,對于A2(g)+3B2(g) 2AB3(g)反應來說,下列所表示的化學反應速率中最大的是
2AB3(g)反應來說,下列所表示的化學反應速率中最大的是
| A.v(A2)=0.8mol·L-1·s-1 | B.v(A2)=40mol·L-1·min-1 |
| C.v(AB3)=1.0mol·L-1·s-1 | D.v(B2)=1.2mol·L-1·s-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
C+CO2 2CO △H 1>0,反應速率v1 ,N2+3H2
2CO △H 1>0,反應速率v1 ,N2+3H2 2NH3 △H 2<0,反應速率v2 。若升高溫度,v1和v2的變化是
2NH3 △H 2<0,反應速率v2 。若升高溫度,v1和v2的變化是
| A.同時增大 | B.同時減少 | C.v1增大,v2減少 | D.v1減少,v2增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在一密閉容器中進行如下反應:2SO2(氣)+O2(氣) 2SO3(氣),已知反應過程中某一時刻SO2、O2、SO3的濃度分別為0.2mol/L、0.1mol/L、0.2mol/L,當反應達平衡時,可能存在的數據是
2SO3(氣),已知反應過程中某一時刻SO2、O2、SO3的濃度分別為0.2mol/L、0.1mol/L、0.2mol/L,當反應達平衡時,可能存在的數據是
| A.SO2為0.4mol/L、O2為0.2mol/L |
| B.SO2為0.25mol/L |
| C.SO2、SO3均為0.15mol/L |
| D.SO3為0.4mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
一定量的鹽酸跟過量的鐵粉反應時,為了減緩反應速率,且不影響生成氫氣的總量,可向鹽酸中加入適量的
①NaOH固體 ②KNO3溶液 ③硫酸鉀溶液 ④CH3COONa固體
| A.①③ | B.③④ | C.②③ | D.②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
在密閉容器中,將1.0 mol CO與1.0 mol H2O混合加熱到800℃,發生下列反應:CO(g)+H2O(g) CO2(g)+H2(g)。一段時間后該反應達到平衡,測得CO的物質的量為0.5 mol。則下列說法正確的是
CO2(g)+H2(g)。一段時間后該反應達到平衡,測得CO的物質的量為0.5 mol。則下列說法正確的是
| A.800℃下,該反應的化學平衡常數為0.25 |
| B.427℃時該反應的平衡常數為9.4,則該反應的△H>0 |
| C.800℃下,若繼續向該平衡體系中通入1.0 mol的CO(g),則平衡時CO物質的量分數為33.3% |
| D.800℃下,若繼續向該平衡體系中通入1.0 mol的H2O(g),則平衡時CO轉化率為66.7% |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
某可逆反應aA + bB cC + Q在某溫度下的平衡常數為K(K≠1),反應熱為Q。保持溫度不變,將方程式的書寫作如下改變,則Q和K數值的相應變化為( )
cC + Q在某溫度下的平衡常數為K(K≠1),反應熱為Q。保持溫度不變,將方程式的書寫作如下改變,則Q和K數值的相應變化為( )
A.寫成2aA + 2bB 2cC,Q值、K值均擴大了一倍 2cC,Q值、K值均擴大了一倍 |
B.寫成2aA + 2bB 2cC,Q值擴大了一倍,K值保持不變 2cC,Q值擴大了一倍,K值保持不變 |
C.寫成cC aA + bB,Q值、K值變為原來的相反數 aA + bB,Q值、K值變為原來的相反數 |
D.寫成cC aA + bB,Q值變為原來的相反數,K值變為倒數 aA + bB,Q值變為原來的相反數,K值變為倒數 |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列有關說法正確的是
| A.CaCO3(s)=CaO(s)+CO2(g)室溫下不能自發進行,說明該反應的△H<0 |
| B.鍍鋅鐵制品鍍層受損后,鐵制品比受損前更容易生銹 |
| C.生鐵中含有碳,抗腐蝕能力比純鐵強 |
| D.Zn具有還原性和導電性,可用作堿性鋅錳干電池的負極材料 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com