

 ,它所對應反應的化學方程式為 。
,它所對應反應的化學方程式為 。 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1 CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1 CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1| 物質 | CH3OH | CH3OCH3 | H2O |
| c(mol/L) | 0.8 | 1.24 | 1.24 |
 CO(g)+H2(g) (1分)
CO(g)+H2(g) (1分) CH3OCH3(g) +CO2(g) △H1=-246.1kJ·mol-1 > (1分)
CH3OCH3(g) +CO2(g) △H1=-246.1kJ·mol-1 > (1分) CO(g)+H2(g);II.(1)根據蓋斯定律,①×2+②+③得催化反應室中總反應的熱化學方程式為3CO(g)+3H2(g)
CO(g)+H2(g);II.(1)根據蓋斯定律,①×2+②+③得催化反應室中總反應的熱化學方程式為3CO(g)+3H2(g)  CH3OCH3(g) +CO2(g) △H1=-246.1kJ·mol-1;該反應放熱,降溫平衡向正向移動,K增大,故在催化反應室中反應③的K>1.0;(2)根據v=△c/△t,將題給數據代入計算,v(CO)= 0.1mol/(L·min);根據平衡計算——三行式計算。
CH3OCH3(g) +CO2(g) △H1=-246.1kJ·mol-1;該反應放熱,降溫平衡向正向移動,K增大,故在催化反應室中反應③的K>1.0;(2)根據v=△c/△t,將題給數據代入計算,v(CO)= 0.1mol/(L·min);根據平衡計算——三行式計算。 CH3OH(g) CO(g)+2H2(g)
CH3OH(g) CO(g)+2H2(g) CH3OH(g)
CH3OH(g)

科目:高中化學 來源:不詳 題型:填空題

 CO(NH2)2(l)+H2O(g)。
CO(NH2)2(l)+H2O(g)。| A.提高NH3的濃度 | B.增大壓強 |
| C.及時轉移生成的尿素 | D.使用更高效的催化劑 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

A.反應處于平衡狀態時, |
B.反應達到平衡后, |
| C.體系的總壓強不變,說明反應已達平衡 |
| D.混合氣體的密度保持不變,說明反應已達平衡 |
 ①
①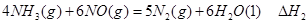 ②
② ③
③ 、
、 、
、 三者之間關系的表達式,
三者之間關系的表達式, =_________。
=_________。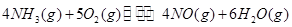
 =
=


| 時間/濃度 |   |   |   |   |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 H= -221.0kJ/mmol
H= -221.0kJ/mmol H= -483.6kJ/ol。
H= -483.6kJ/ol。 H為
H為| A.+262.6kJ/mol | B.-131.3kJ/mol | C.-352.3kJ/mol | D.+131.3kJ/mol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 和
和 。實驗測得N-N鍵鍵能為167kJ·mol-1, NO2中氮氧鍵的平均鍵能為466 kJ·mol-1,N2O4中氮氧鍵的平均鍵能為438.5 kJ·mol-1。
。實驗測得N-N鍵鍵能為167kJ·mol-1, NO2中氮氧鍵的平均鍵能為466 kJ·mol-1,N2O4中氮氧鍵的平均鍵能為438.5 kJ·mol-1。 2NO2(g),在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。下列說法正確的是
2NO2(g),在溫度為T1、T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。下列說法正確的是 
| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.050 | n2 | 0.080 | 0.080 |
 N2O4的平衡常數K將 (填“增大”、“減小”或“不變”)。
N2O4的平衡常數K將 (填“增大”、“減小”或“不變”)。查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
 2Fe(s)+3CO2(g) ΔH =" a" kJ mol-1
2Fe(s)+3CO2(g) ΔH =" a" kJ mol-1| | Fe2O3 | CO | Fe | CO2 |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 2.0 | 1.0 | 1.0 |

查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.Q1 +Q2 +Q3 | B.0.5(Q1 +Q2 +Q3) |
| C.0.5Q1 –0.5Q2 +0.5Q3 | D.1.5Q1 –0.5Q2 +0.5Q 3 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題


查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com