
【題目】下列元素中,原子半徑最大的是
A.LiB.NaC.FD.Cl
科目:高中化學 來源: 題型:
【題目】如圖是某同學利用注射器設計的簡易實驗裝置。甲管中吸入10 mL CH4,同溫同壓下乙管中吸入50 mL Cl2,將乙管氣體推入甲管中,將注射器用日光照射一段時間。
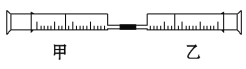
(1)下列是某同學預測的實驗現象:
①氣體最終變為無色;
②實驗過程中,甲管活塞向內移動;
③甲管內壁有油珠;
④產生火花。
其中正確的是 。
(2)甲管中發生的化學反應類型為 。
(3)反應后,甲管中剩余氣體最好用下列的 吸收。
A.水 B.氫氧化鈉溶液
C.硝酸銀溶液 D.飽和食鹽水
(4)反應后,若將甲管中的物質推入盛有適量AgNO3溶液的小試管中會觀察到 ,若用pH試紙測量甲管中溶液的酸堿性,可觀察到pH試紙變 色。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2 L容積不變的容器中,發生N2+3H2 ![]() 2NH3的反應。現通入4 mol H2和4 mol N2,10 s內用H2表示的反應速率為0.12 mol/(L·s),則10 s后容器中N2的物質的量是
2NH3的反應。現通入4 mol H2和4 mol N2,10 s內用H2表示的反應速率為0.12 mol/(L·s),則10 s后容器中N2的物質的量是
A. 1.6 mol B. 2.8 mol
C. 3.2 mol D. 3.6 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】隨著核電荷數的遞增,氧化性逐漸減弱的一組是( )
A.I2、Br2、Cl2、F2B.F2、Cl2、Br2、I2C.F-、Cl-、Br-、I-D.Li、Na、K、Rb
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎂鋁堿式碳酸鹽MgaAlb(OH)c(CO3)d·xH2O是一種不溶于水的新型無機阻燃劑,其受熱分解產物中的MgO、Al2O3熔點較高且都不燃燒,有阻燃作用。完成下列填空:
(1)組成鎂鋁堿式碳酸鹽的三種非金屬元素的原子半徑從小到大的順序是______________。碳原子最外層電子排布式是________________,鋁原子核外有_________種能量不同的電子。
(2)將MgaAlb(OH)c (CO3)d·x H2O表示成氧化物的形式:2aMgO·bAl2O3·2dCO2·(________)H2O;
(3)焦炭與石英高溫下在氮氣流中發生如下反應,工業上可由此制得一種新型陶瓷材料氮化硅(Si3N4):3SiO2(s)+6C(s)+2N2(g)![]() Si3N4(s)+6CO(g) + Q (Q>0)。
Si3N4(s)+6CO(g) + Q (Q>0)。
①該反應中,氧化產物是________________________。若測得反應生成4.48 L CO氣體(標準狀況下),則轉移的電子的物質的量為_____________。
②該反應的平衡常數表達式K=_____________________________;若升高溫度,K值____________(填“增大”、“減小”或“不變”)。
③該反應的速率與反應時間的關系如右圖所示,t4時刻引起正逆反應速率變化的原因是___________________________(寫出一種即可)。
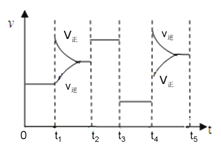
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,將0.1 mol/L NaOH溶液滴入20.00 mL 0.1 mol/L HA溶液,溶液pH隨加入NaOH溶液體積的變化曲線如圖所示。
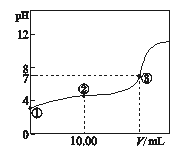
其中不正確的是 ( )
A. ①點:由水電離出的c(H+)=1×10-3mol/L
B. ②點:c(A-)>c(Na+)>c(H+)>c(OH-)
C. ③點:c(Na+)=c(A-)>c(H+)=c(OH-)
D. ③點加入NaOH溶液的體積小于20.00mL
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將3.2 g Cu投入100 mL稀硫酸中加熱,沒有明顯變化,若邊加熱邊緩緩加入一定量H2O2,金屬Cu逐漸溶解,則下列說法正確的是( )
A. 反應過程中有刺激性氣味的氣體生成
B. H2O2對Cu和稀硫酸的反應起催化作用
C. 若Cu和硫酸恰好完全反應,則稀硫酸的物質的量濃度為0.5 mol·L-1
D. 反應中硫酸既表現出酸性又表現出氧化性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含硫化合物的種類很多,現有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4這7種常見的含硫化合物。回答下列問題:
(1)H2SO3轉化為硫酸是酸雨形成的重要過程之一,寫出其反應的化學方程式,并標明電子轉移的方向和數目:_______________________________________。
(2)常溫下,將鐵棒置于濃硫酸中,無明顯現象,課本上解釋為發生了鈍化,但有人認為未發生反應。為驗證此過程,某同學經過思考,設計了如下實驗:將經濃硫酸處理過的鐵棒洗凈后置于CuSO4溶液中,若鐵棒表面_______________________,則發生了鈍化;若鐵棒表面____________________,則未發生反應。
(3)用Na2SO3吸收法是治理SO2污染的一種方法,其原理為(用化學方程式表示): _______________________________________________________________。
(4)減少SO2的污染并變廢為寶,我國正在探索在一定條件下用CO還原SO2得到單質硫的方法來除去SO2,該反應的化學方程式:______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在一容積可變的容器中,反應2X(g)![]() Y(g)+2Z(g)達到平衡時,X、Y和Z的物質的量分別為6mol、3mol和6mol。保持溫度和壓強不變,對平衡混合物中三者的物質的量做如下調整,可使平衡向右移動的是
Y(g)+2Z(g)達到平衡時,X、Y和Z的物質的量分別為6mol、3mol和6mol。保持溫度和壓強不變,對平衡混合物中三者的物質的量做如下調整,可使平衡向右移動的是
A. 均減少1mol B. 均增加1mol C. 均減半 D. 均加倍
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com