
過度排放CO2會造成“溫室效應”,為了減少煤燃燒對環境造成的污染,煤的氣化是高效、清潔利用煤炭的重要途徑。煤綜合利用的一種途徑如圖所示。

(1)已知①C(s) + H2O(g) = CO(g)+H2(g) ΔH1=+131.3 kJ·mol-1
②C(s) + 2H2O(g) = CO2(g) + 2H2(g) ΔH2=+90 kJ·mol-1
則一氧化碳與水蒸氣反應生成二氧化碳和氫氣的熱化學方程式是 ________________________,
(2)用下圖原電池裝置可以完成過程⑤的轉化,該裝置b電極的電極反應式是_______________________。

(3)在壓強為0.1 MPa條件下,容積為V L的密閉容器中a mol CO與2a mol H2在催化劑作用下反應生成甲醇:
CO(g)+2H2(g)  CH3OH(g),CO的平衡轉化率與溫度、壓強的關系如下圖所示,則:
CH3OH(g),CO的平衡轉化率與溫度、壓強的關系如下圖所示,則:
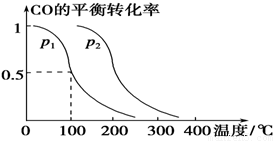
①p1________p2(填“>”、“<”或“=”)。
②在其他條件不變的情況下,向容器中再增加a mol CO與2a mol H2,達到新平衡時,CO的平衡轉化率________(填“增大”、“減小”或“不變”)。
③在p1下,100 ℃時,CO(g)+2H2(g)
 CH3OH(g)反應的平衡常數為________(用含a、V的代數式表示)。
CH3OH(g)反應的平衡常數為________(用含a、V的代數式表示)。
(4)如圖表示CO2與H2反應生成CH3OH和H2O的過程中能量(單位為kJ·mol-1)的變化:

關于該反應的下列說法中,正確的是________(填編號)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0 D.ΔH<0,ΔS>0
(5)為探究反應原理,現進行如下實驗,在體積為1 L的密閉容器中,充入1 mol
CO2和3 mol H2,一定條件下發生反應:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),測得CO2(g)和CH3OH(g)的濃度隨時間變化的曲線如圖所示:
CH3OH(g)+H2O(g),測得CO2(g)和CH3OH(g)的濃度隨時間變化的曲線如圖所示:

①從反應開始到平衡,CO2的平均反應速率v(CO2)=________。
②下列措施中能使化學平衡向正反應方向移動的是________(填編號)。
A.升高溫度 B.將CH3OH(g)及時液化移出
C.選擇高效催化劑 D.再充入1 mol CO2和3 mol H2
(1) CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1 (2) O2 +4e- +2H2O = 4OH— (3)①<② V 2 / a2 ③增大 (4)C (5)①0.075 mol/( L·min). ②BD
【解析】
試題分析:(1)②-①可得:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.3 kJ/mol.. (2)在燃料電池中,通入燃料的電極作負極,通入氧氣的電極作正極。a電極是負極,b電極是正極。b電極的電極反應式是O2 +4e-
+2H2O = 4OH— (3)
①由圖可以看出:在溫度相同時,轉化率P2>P1。根據平衡移動原理:在其它條件不變的情況下。增大壓強,化學平衡向氣體體積減小的方向移動。即向正反應方向移動。這時反應物的轉化率提高。所以P1<P2. ②在其他條件不變的情況下,向容器中再增加a mol CO與2a mol H2。即增大了體系的壓強,這時化學平衡向正反應方向移動。故達到新平衡時,CO的平衡轉化率增大。③在p1下,100 ℃時,CO(g)+2H2(g)
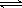 CH3OH(g)反應的平衡常數為K=C (CH3OH)/ { C(CO)·C2(H2)}
=( a/2V):{(a/2V) ·(a/V)}2= V 2
/ a2.(4)CO2(g)+3H2(g)
CH3OH(g)反應的平衡常數為K=C (CH3OH)/ { C(CO)·C2(H2)}
=( a/2V):{(a/2V) ·(a/V)}2= V 2
/ a2.(4)CO2(g)+3H2(g)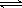 CH3OH(g)+CO(g).由圖可看出該反應的正反應是放熱反應。該反應的正反應是個氣體體積減小的放熱反應。所以△H<0;△S<0。選項為:C。(5)①從反應開始到平衡,CO2的平均反應速率v(CO2)=(1-0.25)mol/L÷10min=0.075 mol/(
L·min). ②A升高溫度化學平衡向吸熱方向移動。由于該反應的正反應是放熱反應所以升高溫度化學平衡向逆反應方向移動。B.減小生成物的濃度,化學平衡向正反應方向移動。故將CH3OH(g)及時液化移出可使平衡向正反應方向移動,C.催化劑 對化學平衡無影響。D.達到平衡時若再充入1 mol CO2和3 mol
H2 ,即增大了壓強,化學平衡向氣體體積減小的方向及正反應方向移動。所以能使化學平衡向正反應方向移動的措施是BD。
CH3OH(g)+CO(g).由圖可看出該反應的正反應是放熱反應。該反應的正反應是個氣體體積減小的放熱反應。所以△H<0;△S<0。選項為:C。(5)①從反應開始到平衡,CO2的平均反應速率v(CO2)=(1-0.25)mol/L÷10min=0.075 mol/(
L·min). ②A升高溫度化學平衡向吸熱方向移動。由于該反應的正反應是放熱反應所以升高溫度化學平衡向逆反應方向移動。B.減小生成物的濃度,化學平衡向正反應方向移動。故將CH3OH(g)及時液化移出可使平衡向正反應方向移動,C.催化劑 對化學平衡無影響。D.達到平衡時若再充入1 mol CO2和3 mol
H2 ,即增大了壓強,化學平衡向氣體體積減小的方向及正反應方向移動。所以能使化學平衡向正反應方向移動的措施是BD。
考點:考查熱化學方程式的書寫、化學平衡常數的計算及外界條件對化學平衡的影響等知識。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:閱讀理解
過度排放CO2會造成溫室效應,最近科學家提出“綠色自由”構想:把空氣吹入碳酸鉀溶液,然后再把CO2從溶液中提取出來,經化學反應后使空氣中的CO2轉變為可再生燃料甲醇。“綠色自由”構想技術流程如下:
(1)寫出吸收池中主要反應的離子方程式 ;
在合成塔中,若有2.2kgCO2與足量H2恰好完全反應,生成氣態的水和甲醇,可放出2473.5kJ的熱量,試寫出合成塔中發生反應的熱化學方程式 。
(2)“綠色自由”構想技術流程中常包括物質和能量的“循環利用”,上述流程中能體現“循環利用”的除碳酸鉀溶液外,還包括 。
(3)甲醇可制作燃料電池。寫出以氫氧化鉀為電解質的甲醇燃料電池負極反應式 。當電子轉移的物質的量為 時,參加反應的氧氣的體積是6.72L(標準狀況下)。
(4)工業上常以CO和H2為主要原料,生產甲醇。
某密閉容器中充有10mol CO與20mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g)CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
①若A、B兩點表示在某時刻達到的平 衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tA tC(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高 CO轉化率可采取的措施是 (答出兩點即可)。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖南省“五市十校”高三12月聯合檢測化學試卷(解析版) 題型:填空題
過度排放CO2會造成“溫室效應”,為了減少煤燃燒對環境造成的污染,煤的氣化是高效、清潔利用煤炭的重要途徑。煤綜合利用的一種途徑如圖所示。

(1)已知①C(s) + H2O(g) = CO(g)+H2(g) ΔH1=+131.3 kJ·mol-1
②C(s) + 2H2O(g) = CO2(g) + 2H2(g) ΔH2=+90 kJ·mol-1
則一氧化碳與水蒸氣反應生成二氧化碳和氫氣的熱化學方程式是 ________________________,
(2)用下圖原電池裝置可以完成過程⑤的轉化,該裝置b電極的電極反應式是_______________________。

(3)在壓強為0.1 MPa條件下,容積為V L的密閉容器中a mol CO與2a mol H2在催化劑作用下反應生成甲醇:
CO(g)+2H2(g)  CH3OH(g),CO的平衡轉化率與溫度、壓強的關系如下圖所示,則:
CH3OH(g),CO的平衡轉化率與溫度、壓強的關系如下圖所示,則:

①p1________p2(填“>”、“<”或“=”)。
②在其他條件不變的情況下,向容器中再增加a mol CO與2a mol H2,達到新平衡時,CO的平衡轉化率________(填“增大”、“減小”或“不變”)。
③在p1下,100 ℃時,CO(g)+2H2(g)
 CH3OH(g)反應的平衡常數為________(用含a、V的代數式表示)。
CH3OH(g)反應的平衡常數為________(用含a、V的代數式表示)。
(4)如圖表示CO2與H2反應生成CH3OH和H2O的過程中能量(單位為kJ·mol-1)的變化:

關于該反應的下列說法中,正確的是________(填編號)。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS<0 D.ΔH<0,ΔS>0
(5)為探究反應原理,現進行如下實驗,在體積為1 L的密閉容器中,充入1 mol
CO2和3 mol H2,一定條件下發生反應:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),測得CO2(g)和CH3OH(g)的濃度隨時間變化的曲線如圖所示:
CH3OH(g)+H2O(g),測得CO2(g)和CH3OH(g)的濃度隨時間變化的曲線如圖所示:

①從反應開始到平衡,CO2的平均反應速率v(CO2)=________。
②下列措施中能使化學平衡向正反應方向移動的是________(填編號)。
A.升高溫度 B.將CH3OH(g)及時液化移出
C.選擇高效催化劑 D.再充入1 mol CO2和3 mol H2
查看答案和解析>>
科目:高中化學 來源:2014屆江蘇南京學大教育專修學校高二3月月考化學試卷(解析版) 題型:填空題
過度排放CO2會造成“溫室效應”,科學家正在研究如何將CO2轉化為可利用的
資源。目前工業上有一種方法是用CO2來生產燃料甲醇。為探究反應原理,現進行如下實驗,
在1 L固定體積的密閉容器中,充入1 mol CO2和3 mol H2,一定條件下發生反應:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
ΔH>0,經測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g)
ΔH>0,經測得CO2和CH3OH(g)的濃度隨時間變化如圖所示。

(1)從反應開始到平衡,CO2的平均反應速率v(CO2)= ;
(2)該反應的平衡常數表達式K= ;
(3)能判斷該反應是否達到化學平衡狀態的依據是 (多選扣分);
a.容器中壓強不變 b.v正(H2)=v逆(H2O)
c.混合氣體中c(H2O)不變 d.c(CO2)=c(CH3OH)
(4)下列措施中能使化學平衡向正反應方向移動的是 (填字母)。
a.升高溫度 b.將CH3OH(g)及時液化抽出
c.選擇高效催化劑 d.再充入H2O(g)
查看答案和解析>>
科目:高中化學 來源:2010-2011學年山東省高三第三次模擬考試(理綜)化學部分 題型:填空題
過度排放CO2會造成溫室效應,最近科學家提出“綠色自由”構想:把空氣吹入碳酸鉀溶液,然后再把CO2從溶液中提取出來,經化學反應后使空氣中的CO2轉變為可再生燃料甲醇。“綠色自由”構想技術流程如下:

(1)寫出吸收池中主要反應的離子方程式 ;
在合成塔中,若有2.2kgCO2與足量H2恰好完全反應,生成氣態的水和甲醇,可放出2473.5kJ的熱量,試寫出合成塔中發生反應的熱化學方程式 。
(2)“綠色自由”構想技術流程中常包括物質和能量的“循環利用”,上述流程中能體現“循環利用”的除碳酸鉀溶液外,還包括 。
(3)甲醇可制作燃料電池。寫出以氫氧化鉀為電解質的甲醇燃料電池負極反應式 。當電子轉移的物質的量為 時,參加反應的氧氣的體積是6.72L(標準狀況下)。
(4)工業上常以CO和H2為主要原料,生產甲醇。
某密閉容器中充有10
mol CO與20mol H2,在催化劑作用下反應生成甲醇:CO(g)+2H2(g) CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。
CH3OH(g);CO的轉化率(α)與溫度、壓強的關系如下圖所示。

①若A、B兩點表示在某時刻達到的平 衡狀態,此時在A點時容器的體積為10L,則該溫度下的平衡常數K= ;此時在B點時容器的體積VB 10L(填“大于”、“小于”或“等于”)。
②若A、C兩點都表示達到的平衡狀態,則自反應開始到達平衡狀態所需的時間tA tC(填“大于”、“小于”或“等于”)。
③在不改變反應物用量情況下,為提高 CO轉化率可采取的措施是 (答出兩點即可)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com