
【題目】氣體的體積主要由以下什么因素決定:( )
①氣體的分子多少 ②氣體分子的大小
③氣體分子間的平均距離 ④氣體分子的相對分子質量.
A. ①②B. ①③C. ②③D. ②④
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】已知:Pb的化合價只有+2、+4,且+4價的Pb具有強氧化性,能氧化濃HCl生成Cl2;PbO2不穩定,隨溫度升高按下列順序逐步分PbO2→Pb2O3→Pb3O4→PbO.現將a mol PbO2加熱分解,收集產生的O2;向加熱后所得固體中加入足量的濃鹽酸,收集產生的Cl2 . 加熱反應后所得固體中,Pb2+占Pb元素的物質的量分數為x;兩步反應中收集的O2和Cl2的物質的量之和為y mol.試回答下列問題:
(1)試寫出Pb2O3與濃鹽酸反應的化學方程式 .
(2)用含x與a的表達式表示產生的O2、Cl2的物質的量n(O2)= , n(Cl2)= .
(3)寫出y與a、x的函數關系式: .
(4)若兩步反應中O2和Cl2的物質的量之比為5:3,則剩余固體中含有的物質為;其物質的量之比為 .
(5)PbO2和Pb經常作制造蓄電池的原材料,鉛蓄電池的工作原理:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O.現有一種生產NH4NO3的新工藝,電解NO制備NH4NO3 , 其工作原理如圖所示,為使電解產物全部轉化為NH4NO3 , 需補充物質A,A是 , 說明理由: . 生產1噸硝酸銨需消耗Pb的物質的量是kg(保留到整數).
2PbSO4+2H2O.現有一種生產NH4NO3的新工藝,電解NO制備NH4NO3 , 其工作原理如圖所示,為使電解產物全部轉化為NH4NO3 , 需補充物質A,A是 , 說明理由: . 生產1噸硝酸銨需消耗Pb的物質的量是kg(保留到整數).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某同學組裝了如圖所示的電化學裝置,則下列說法正確的是( ) 
A.圖中甲池為原電池裝置,Cu電極發生還原反應
B.實驗過程中,甲池左側燒杯中NO ![]() 的濃度不變
的濃度不變
C.若甲池中Ag電極質量增加5.4g時,乙池某電極析出1.6g金屬,則乙中的某鹽溶液可能是足量AgNO3溶液
D.若用銅制U形物代替“鹽橋”,工作一段時間后取出U形物稱量,質量不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.NA代表阿伏加德羅常數,1molC4H10中含共價鍵數目為14NA
B.某反應的△H=﹣88kJ?mol﹣1 , 則正反應活化能一定小于88kJ?mol﹣1
C.已知某溫度下,Kw=l×10﹣13 , 若將pH=8的NaOH溶液與pH=5的H2SO4溶液混合保持溫度不變,欲使混合溶液pH=7,則NaOH溶液與H2SO4溶液的體積比為11:9
D.將濃度為0.1 mol?L﹣1 HF溶液加水不斷稀釋過程中,電離度和Ka(HF)保持不變, ![]() 始終保持增大
始終保持增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋅銅原電池裝置如圖所示,其中陽離子交換膜只允許陽離子和水分子通過,下列有關敘述正確的是( )
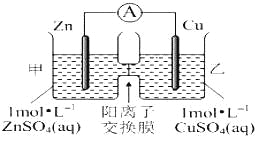
A. 銅電極上發生氧化反應
B. 電池工作一段時間后,甲池的C(SO42-)減小
C. 電池工作一段時間后,乙池溶液的總質量增加
D. 陽離子通過交換膜向正極移動,陰離子通過交換膜向負極移動,保持溶液中電荷平衡
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuCl廣泛應用于化工和印染等行業。某研究性學習小組擬熱分解結晶水合物CuCl·2H2O制備CuCl,并進行相關探究。
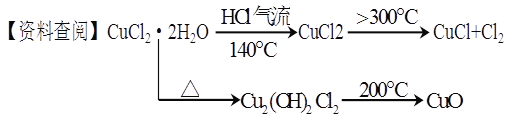
【實驗探究】該小組用下圖所示裝置進行實驗(夾持儀器略)。

請回答下列問題:
(1)儀器X的名稱是 。
(2)實驗操作的先后順序是![]()
![]() (填操作的編號)。
(填操作的編號)。
a.檢查裝置的氣密性后加入藥品
b.熄滅酒精燈,冷卻
c.在“氣體入口”處通入干燥HCl
d.點燃酒精燈,加熱
e.停止通入HCl,然后通入N2
(3)在實驗過程中,觀察到B中物質由白色變為藍色,C中試紙的顏色變化是 。
(4)裝置D中發生的氧化還原反應的離子方程式是 。
【探究反思】
(5)反應結束后,取出CuCl產品進行實驗,發現其中含有少量的CuCl2或CuO雜質,根據資料信息分析:
①若雜質是CuCl2,則產生的原因是 。
②若雜質是CuO,則產生的原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各選項有機物數目,與分子式為ClC4H7O2且能與碳酸氫鈉反應生成氣體的有機物數目相同的是(不含立體異構)( )
A.分子式為C5H10的烯烴
B.分子式為C4H8O2的酯
C.甲苯( ![]() )的一氯代物
)的一氯代物
D.立體烷( ![]() )的二氯代物
)的二氯代物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A. 直徑介于1~100 nm之間的粒子稱為膠體
B. 通過觀察外觀的方法可以區別膠體和溶液
C. 利用丁達爾效應可以區別溶液與膠體
D. 膠體區別于其他分散系的本質特征是丁達爾效應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com