
甲醇是一種很好的燃料,工業上用CH4和H2O為原料,通過反應Ⅰ和Ⅱ來制備甲醇。
(1)將1.0 mol CH4和2.0 mol H2O(g)通入反應室(容積為100 L),在一定條件下發生反應:CH4(g)+H2O(g) CO(g)+3H2(g)……Ⅰ。CH4的轉化率與溫度、壓強的關系如下圖。
CO(g)+3H2(g)……Ⅰ。CH4的轉化率與溫度、壓強的關系如下圖。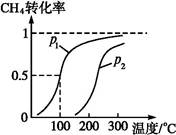
①已知100 ℃壓強為p1時達到平衡所需的時間為5 min,則用H2表示的平均反應速率為 。
②圖中的p1 p2(填“<”“>”或“="”),100" ℃壓強為p2時平衡常數為 。
③該反應的ΔH 0(填“<”“>”或“=”)。
(2)在一定條件下,將a mol CO與3a mol H2的混合氣體在催化劑作用下能自發反應生成甲醇: CO(g)+2H2(g) CH3OH(g) ΔH<0 ……Ⅱ
CH3OH(g) ΔH<0 ……Ⅱ
①若容器容積不變,下列措施可增加甲醇產率的是( )
A.升高溫度
B.將CH3OH(g)從體系中分離
C.充入He,使體系總壓強增大
D.再充入1 mol CO和3 mol H2
②為了尋找合成甲醇的溫度和壓強的適宜條件,某同學設計了三組實驗,部分實驗條件已經填在下面實驗表格中。
A.下表中剩余的實驗條件數據:a= ;b= 。
。
B.根據反應Ⅱ的特點,下圖是在壓強分別為0.1 MPa和5 MPa下CO的轉化率隨溫度變化的曲線圖,請指明圖中的壓強px= MPa。
| 實驗編號 | T/℃ | n(CO)/n(H2) | p/MPa |
| 1 | 150 | 1/3 | 0.1 |
| 2 | a | 1/3 | 5 |
| 3 | 350 | b | 5 |

 手拉手全優練考卷系列答案
手拉手全優練考卷系列答案科目:高中化學 來源: 題型:填空題
在某一容積為5 L的密閉容器內,加入0.2mol 的CO和0.2mol的H2O(g),在催化劑存在的條件下高溫加熱,發生如下反應:CO(g)+H2O(g) CO2(g)+H2(g),反應放出熱量。反應中CO2的濃度隨時間變化的情況如下圖所示。
CO2(g)+H2(g),反應放出熱量。反應中CO2的濃度隨時間變化的情況如下圖所示。
(1)根據圖中數據,從反應開始至達到平衡時,CO的化學反應速率為________;反應平衡時c(H2)=________。
(2)判斷該反應達到平衡的依據是________(填序號)。
| A.CO減少的化學反應速率和CO2減少的化學反應速率相等 |
| B.CO、H2O、CO2、H2的濃度都相等 |
| C.CO、H2O、CO2、H2的濃度都不再發生變化 |
| D.正、逆反應速率都為零 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
超音速飛機在平流層飛行時,尾氣中的NO會破壞臭氧層。科學家正在研究利用催化技術將尾氣中的NO和CO轉變成CO2和N2 , 化學方程式如下:2NO + 2 CO 2CO2 + N2 ,為了測定在某種催化劑作用下的反應速率,在某溫度下,用氣體傳感器測得不同時間的NO和CO濃度如下表:
2CO2 + N2 ,為了測定在某種催化劑作用下的反應速率,在某溫度下,用氣體傳感器測得不同時間的NO和CO濃度如下表:
| 時間 /s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol·L—1 | 1.00×10—3 | 4.50×10—4 | 2.50×10—4 | 1.50×10—4 | 1.00×10—4 | 1.00×10—4 |
| c(CO)/mol·L—1 | 3.60×10—3 | 3.05×10—3 | 2.85×10—3 | 2.75×10—3 | 2.70×10—3 | 2.70×10—3 |
| 實驗編號 | T / ℃ | NO初始濃度 ( mol·L—1 ) | CO初始濃度 ( mol·L—1 ) | 催化劑的比表面積 ( m2·g—1 ) |
| Ⅰ | 280 | 1.20 × 10—3 | 5.80 × 10—3 | 82 |
| Ⅱ | | | | 124 |
| Ⅲ | 350 | | | 124 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
一定條件下,在體積為5 L的密閉容器中,氣態物質A、B、C的物質的量n(mol)隨時間t的變化如圖1所示。已知達平衡后,降低溫度,A的體積百分含量將減小。
(1)根據上圖數據,寫出反應的化學方程式 ;
從反應開始到平衡時的平均速率v(C)= 。
(2)該反應的ΔH 0(填“>”、“<”或“=”)。
(3)此反應平衡常數的表達式為K= 。
(4)該反應的反應速率v和時間t的關系如圖2所示:
①根據上圖判斷,在t3時刻改變的外界條件是 。
②A的轉化率最大的一段時間是 。
③各階段的平衡常數如表所示:
K1、K2、K3之間的關系為: (用“>”、“<”或“=”連接)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
金屬鎂及其化合物不僅在國防上有重要應用,在化學研究中也有廣泛應用。
(1)某同學研究反應速率時用如下方法:取一段鎂條,用砂紙擦去表面的氧化膜,使足量鎂條與一定量鹽酸反應生成H2的量與反應時間的關系曲線如圖所示。鎂與鹽酸反應的離子方程式為 ;在前4min內,鎂條與鹽酸的反應速率逐漸加快,在4 min之后,反應速率逐漸減慢,請簡述其原因:_____________。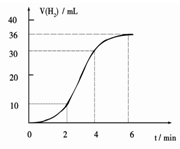
(2)向少量的Mg(OH)2懸濁液中加入適量的飽和氯化銨溶液,固體完全溶解,寫出NH4Cl飽和溶液使Mg(OH)2懸濁液溶解的離子方程式 。
(3)Mg Al可形成原電池:
| 編號 | 電極材料 | 電解質溶液 | 電子流動方向 |
| 1 | Mg Al | 稀鹽酸 | Mg流向Al |
| 2 | Mg Al | NaOH溶液 | |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
甲醇汽油是由10%一25%的甲醇與其他化工原料、添加劑合成的新型車用燃料,可達到國標汽油的性能和指標。甲醇是一種可再生能源,具有廣泛的開發和應用前景。
Ⅰ、工業上合成甲醇一般采用下列反應:CO(g)+2 H2(g) CH3 OH(g) △H="a" kJ/mol,
CH3 OH(g) △H="a" kJ/mol,
下表是該反應在不同溫度下的化學平衡常數(K):
| 溫度/0C | 250 | 310 | 350 |
| K | 2.041 | 0.250 | 0.012 |
| 濃度mol/L 時間/min | c(CO) | c(H2) | c(CH3OH) |
| 0 | 0.8 | 1.6 | 0 |
| 2 | 0.6 | 1.2 | 0.2 |
| 4 | 0.3 | 0.6 | 0.5 |
| 6 | 0.3 | 0.6 | 0.5 |
 CH3 OH(g)△H="a" kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中CO的百分含量分別為w1和w2;已知T1<T2,則
CH3 OH(g)△H="a" kJ/mol。恒溫恒容下反應相同時間后,分別測得體系中CO的百分含量分別為w1和w2;已知T1<T2,則查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業制硫酸的過程中利用反應2SO2(g)+O2(g)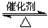 2SO3(g);△H<0,將SO2轉化為SO3,尾氣SO2可用NaOH溶液進行吸收。請回答下列問題:
2SO3(g);△H<0,將SO2轉化為SO3,尾氣SO2可用NaOH溶液進行吸收。請回答下列問題:
(1)一定條件下,向一帶活塞的密閉容器中充入2molSO2和1molO2發生反應,則下列說法正確的是 。
A.若反應速率v(SO2)=v(SO3),則可以說明該可逆反應已達到平衡狀態
B.保持溫度和容器體積不變,充入2 mol N2,化學反應速率加快
C.平衡后僅增大反應物濃度,則平衡一定右移,各反應物的轉化率一定都增大
D.平衡后移動活塞壓縮氣體,平衡時SO2、O2的百分含量減小,SO3的百分含量增大
E.保持溫度和容器體積不變,平衡后再充入2molSO3,再次平衡時各組分濃度均比原平衡時的濃度大
F.平衡后升高溫度,平衡常數K增大
(2)將一定量的SO2(g)和O2(g)分別通入到體積為2L的恒容密閉容器中,在不同溫度下進行反應得到如下表中的兩組數據:
| 實驗編號 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
鐵及其化合物在生產、生活中有廣泛應用。請回答下列問題:
(1)水熱法制備Fe3O4納米顆粒的反應是:3Fe2++2S2O32-+O2+xOH-→Fe3O4↓+S4O32-+2H2O
①上述離子方程式中x=________;
②每生成1 mol Fe3O4,反應轉移的電子為________mol;
(2)某高效凈水劑可由Fe(OH)SO4聚合得到。工業上以FeSO4、NaNO2和稀硫酸為原料來制備Fe(OH)SO4,反應中有NO生成,化學方程式為 。
高爐煉鐵過程中發生的主要反應為: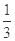 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g) 
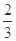 Fe(s)+CO2(g)+Q
Fe(s)+CO2(g)+Q
已知該反應在不同溫度下的平衡常數如下:
| 溫度/℃ | 1000 | 1115 | 1300 |
| 平衡常數 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)二氧化硫的催化氧化的過程如圖所示,其中a、c二步的化學方程式可表示為: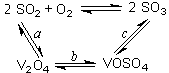
SO2+V2O5 SO3+ V2O4
SO3+ V2O4
4VOSO4+O2 2V2O5+4SO3。
2V2O5+4SO3。
該反應的催化劑是 (寫化學式)
(2) 550 ℃時,SO2轉化為SO3的平衡轉化率(α)與體系總壓強(p)的關系如圖所示。將2.0 mol SO2和1.0 mol O2置于5 L密閉容器中,反應達平衡后,體系總壓強為0.10 M Pa。試計算反應2SO3 2SO2+O2在550 ℃時的平衡常數K= 。
2SO2+O2在550 ℃時的平衡常數K= 。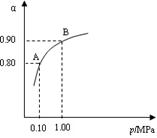
(3)550 ℃時,將2.0 mol SO2和1.0 mol O2置于5 L密閉容器中,反應 達平衡后,下列措施中能使n(SO3)/n(SO2)增大的是
A.升高溫度
B.充入He(g),使體系總壓強增大
C.再充入2 mol SO2和1 mol O2
D.再充入1 mol SO2和1 mol O2
(4)維持溫度不變條件下使之發生如下反應:2SO2+O2 2SO3,有兩只密閉容器A和B。A容器有一個可以移動的活塞能使容器內保持恒壓,B容器能保持恒容。起始時向這兩個容器中分別充入等物質的量的體積比為2∶1的SO2和O2的混合氣體,并使A和B容積相等(如下圖所示)。
2SO3,有兩只密閉容器A和B。A容器有一個可以移動的活塞能使容器內保持恒壓,B容器能保持恒容。起始時向這兩個容器中分別充入等物質的量的體積比為2∶1的SO2和O2的混合氣體,并使A和B容積相等(如下圖所示)。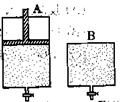
試填寫下列空格:
A容器達到平衡時所需的時間比B容器__________(填:“短或長”);平衡時A容器中SO2的轉化率比B容器_______(填:“大或小”);達到所述平衡后,若向兩容器中通入等物質的量的原反應氣體,達到平衡時,A容器的混合氣體中SO3的體積分數_________(填“增大”、“減小”或“不變”,下同);B容器的混合氣體中SO3的體積分數_________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com