
【題目】向盛有KI溶液的試管中加入少許CCl4后滴加氯水,CCl4層變成紫色。如果繼續向試管中滴加氯水,振蕩,CCl4層會逐漸變淺,最后變成無色。完成下列填空:
(1)寫出并配平CCl4層由紫色變成無色的化學反應方程式,標出電子轉移的方向和數目:
![]()
_______________________________________
(2)整個反應過程中的還原劑是__________、___________。
(3)把KI換成KBr,則CCl4層變為橙紅色:繼續滴加氯水,CCl4層的顏色沒有變化。Cl2、HIO3、HBrO3氧化性由強到弱的順序是________________。據此請判斷下列反應能否進行:HBrO3 +HCl → Br2 + Cl2 + H2O(未配平)_________(填“能”或“否”)
【答案】 I2+5Cl2+6H2O=2HIO3+10HCl(電子轉移方向略) KI I2 HBrO3>Cl2>HIO3 能
【解析】(1)氯氣具有強氧化性,向盛有KI溶液的試管中加入少許CCl4后滴加氯水,CCl4層變成紫色,說明生成I2,繼續向試管中滴加氯水,振蕩,CCl4層會逐漸變淺,最后變成無色,說明I2被進一步氧化,生成HIO3,同時氯氣被還原為HCl,反應的方程式為5Cl2+I2+6H20=2HIO3+10HCl,其中Cl2為氧化劑,反應中轉移電子的方向和數目為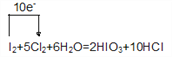 ;
;
(2)在Cl2+2KI=I2+2KCl的反應中KI被氧化,為還原劑;在Cl2+I2+H20→HIO3+HCl反應,I元素的化合價升高,被氧化,I2在反應中做還原劑;
(3)氯氣的氧化性比溴強,將KI換成KBr,則生成Br2,則CCl4層變為棕色,繼續滴加氯水,CCl4層的顏色沒有變化,說明氧化性HBrO3>Cl2,根據氧化劑和還原劑反應生成氧化產物和還原產物,氧化劑氧化性大于氧化產物的氧化性,則有Cl2>HIO3,所以氧化性順序為HBrO3>Cl2>HIO3,氧化性HBrO3>Cl2,所以HBrO3+HCl→Br2+Cl2+H2O能進行。


科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是( )
A. NaHS溶于水: NaHS = Na+ + H+ + S2-
B. Al(OH)3電離: H2O+AlO2-+H+=Al(OH)3=Al3++3OH-
C. NaHSO4溶于水:NaHSO4=Na++ HSO4-
D. HF溶于水:HF+H2O![]() H3O++F-
H3O++F-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(多選)如圖所示,A處通入干燥Cl2 , 關閉B閥時,C處的紅色布條看不到明顯現象,打開B閥后,C處紅色布條逐漸褪色,則D瓶中裝的是( ) 
A.濃H2SO4
B.NaOH溶液
C.濃鹽酸
D.飽和NaCl溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗中,溶液顏色有明顯變化的是( )
A.少量明礬溶液加入到過量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固體加入到過量NaHSO4溶液中
D.往酸性高錳酸鉀溶液中滴入少量Fe2(SO4)3稀溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容積的容器中進行反應:2SO2(g)+O2(g) ![]() 2SO3(g)。已知反應過程中某一時刻SO2、O2、SO3的濃度分別為0.2 molL-1、0.1 molL-1、0.2 molL-1。當反應達平衡時,可能存在的數據是( )
2SO3(g)。已知反應過程中某一時刻SO2、O2、SO3的濃度分別為0.2 molL-1、0.1 molL-1、0.2 molL-1。當反應達平衡時,可能存在的數據是( )
A. SO2為0.4 molL-1,O2為0.2 molL-1 B. SO2為0.25 molL-1
C. SO2、SO3均為0.15 molL-1 D. SO3為0.4 molL-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述不科學的是( )
A.含氟牙膏可預防齲齒B.誤食重金屬鹽后,可喝鮮牛奶急救
C.維生素可以調節人體的新陳代謝D.可用聚乙烯或聚氯乙烯塑料包裝食品
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某烴A的分子式為C6H12
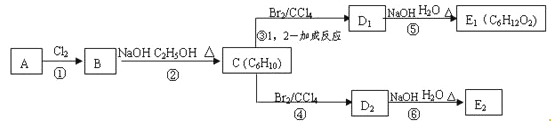
(1)若烴A能使溴水褪色,在一定條件下能與氯氣發生取代反應,其一氯取代物只有一種,則烴A的結構簡式為_____。
(2)④、⑥的反應類型依次________、__________。
(3)反應②的化學方程式為________________。
(4)寫出E1與金屬鈉反應的化學方程式___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com