
下列說法正確的是( )
| A.根據反應5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O可知:用酸性KMnO4溶液可檢驗綠礬(FeSO4·7H2O)是否變質 |
| B.根據反應H3PO3+2NaOH(足量)===Na2HPO3+2H2O可知:H3PO3屬于三元酸 |
| C.根據反應3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O可知:反應中HNO3表現酸性和氧化性 |
| D.根據反應CuSO4+H2S===CuS↓+H2SO4可知:H2S的酸性比H2SO4強 |
 黃岡小狀元滿分沖刺微測驗系列答案
黃岡小狀元滿分沖刺微測驗系列答案 新輔教導學系列答案
新輔教導學系列答案 陽光同學一線名師全優好卷系列答案
陽光同學一線名師全優好卷系列答案科目:高中化學 來源: 題型:單選題
常溫下,下列各組離子在指定溶液中一定能大量共存的是( )
A.c(H+)/c(OH-)=1×1014的溶液:Fe2+、K+、HSO 、ClO- 、ClO- |
B.0.1 mol·L-1FeCl3溶液:NH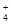 、H+、I-、SCN- 、H+、I-、SCN- |
C.0.1 mol·L-1Na2CO3溶液:K+、Ca2+、HCO 、SO 、SO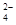 |
D.使酚酞變紅色的溶液:Na+、Ba2+、NO 、Cl- 、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列反應的離子方程式正確的是( )
| A.向AgNO3溶液中滴加氨水至過量:Ag++NH3·H2O=AgOH↓+NH4+ |
| B.向Mg(OH)2懸濁液中滴加FeCl3溶液:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| C.向Na2S2O3溶液中加入足量稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O |
D.向苯酚鈉溶液中通入少量CO2氣體: |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,下列各組離子在指定溶液中一定能大量共存的是
| A.0.1 mol/L的NaOH溶液:K+、AlO2-、SO42-、CO32- |
| B.0.1 mol/LFeCl3溶液:K+、NH4+、I-、SCN- |
| C.0.1 mol/L的Na2CO3溶液:K+、Ba2+、NO3-、Cl- |
| D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、I-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,下列各組離子在指定溶液中一定能大量共存的是
| A.能溶解Al2O3的溶液:Na+、K+、HCO3-、NO3- |
| B.0.1mol·L-1Ca(ClO)2溶液:K+、Na+、I-、Cl- |
| C.能使甲基橙顯紅色的溶液:K+、Fe2+、Cl-、NO3- |
| D.加入KSCN顯紅色的溶液:Na+、Mg2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
能正確表示下列化學反應的離子方程式是
| A.碳酸鈣與醋酸反應:CaCO3 + 2H+ = Ca2+ + CO2↑ + H2O |
| B.利用腐蝕法制作印刷線路板:Fe3+ + Cu = Fe2+ + Cu2+ |
C.工業制備氯氣:2NaCl + 2H2O 2Na+ + 2OH一+ H2↑ + Cl2↑ 2Na+ + 2OH一+ H2↑ + Cl2↑ |
| D.過量二氧化碳與石灰水反應:CO2 + 2OH一= CO32一+ H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列反應的離子方程式中,正確的是
| A.NH4HCO3溶液與過量NaOH溶液反應:NH4+ + OH- = NH3·H2O |
| B.在苯酚的乳濁溶液中滴加碳酸鈉溶液變澄清:2C6H5OH + CO32- → CO2↑+ 2C6H5O- + H2O |
C.用兩根銅棒作電極電解鹽酸:2H+ + 2Cl-  H2↑ + Cl2↑ H2↑ + Cl2↑ |
| D.SO2通入次氯酸鈉溶液中:SO2 + ClO-+ H2O = SO42- + Cl-+ 2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
常溫下,下列各組粒子在指定溶液中可能大量共存的是( )
| A.氨水中:Al3+、Cl-、I-、SO42- | B.pH=2的溶液中:K+、Cu2+、Cl-、NO3- |
| C.食鹽水中:Mg2+、Fe(OH)2、Br-、CO32- | D.無色溶液:NO3-、SO2、NH4+、Na+ |
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
根據表中信息,判斷下列敘述中正確的是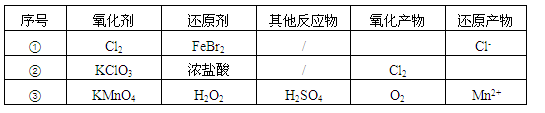
| A.表中①組的反應只可能有一種元素被氧化和一種元素被還原 |
| B.氧化性強弱的比較: KClO3>Fe3+>Cl2>Br2 |
| C.由表中①②組反應推測:ClO3-、Br-、H+、Fe2+不能在濃溶液中大量共存 |
| D.表中③組反應的離子方程式為:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com