
| 實驗序號 | FeSO4溶液的體積讀數/mL | |
| 滴定前 | 滴定后 | |
| 1 | 0.10 | 16.20 |
| 2 | 0.30 | 15.31 |
| 3 | 0.20 | 15.19 |
| 1.56×10-10 |
| 3 | 2×1.10×10 -12 |


科目:高中化學 來源: 題型:
A.實驗室制備乙烯時必須將溫度計水銀球插入反應液中,測定反應液溫度
B.取少量蔗糖溶液加稀硫酸水浴加熱幾分鐘后加新制的氫氧化銅濁液加熱,觀察現象,判斷蔗糖水解的產物中是否含有葡萄糖
C.在苯中加入溴水充分振蕩、靜置,觀察現象,判斷苯環中是否存在碳碳雙鍵
D.實驗室制備乙酸乙酯時,先將乙醇、乙酸混合,再把混合液加入到濃硫酸中
E.除去蛋白質溶液中少量的NaCl,可將裝有混合液的半透膜袋放入流水中滲析
F.中和滴定時,酸式滴定管用蒸餾水清洗幾次后,即加入標準鹽酸進行滴定
G.實驗室用潔凈的試管做銀鏡反應時不能將試管直接放在酒精燈火焰上加熱
Ⅱ.儲氫納米碳管研究成功體現了科技的進步。但用電弧法合成的碳納米管常伴有大量的雜質——碳納米顆粒,這種碳納米顆粒可用氧化氣化法提純。其反應式為:
![]()
![]()
(1)此反應的氧化劑是______________,氧化產物是______________。
(2)H2SO4在上述反應中表現出來的性質是______________(填選項編號)。
A.酸性 B.氧化性 C.吸水性 D.脫水性
(3)配平的化學計量數為_________________。
(4)上述反應中若產生0.1 mol CO2氣體,則轉移電子的物質的量是____________mol。
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
(14分)二氧化氯(ClO2)作為一種高效強氧化劑已被聯合國世界衛生組織(WHO)列為AI級安全消毒劑。常溫下二氧化氯為黃綠色或橘黃色氣體,性質非常不穩定,溫度過高或水溶液中ClO2的質量分數高于30%等均有可能引起爆炸,易與堿液反應生成鹽和水。
(1)某研究小組設計如圖所示實驗制備ClO2溶液,其反應的化學方程式為
①在反應開始之前將燒杯中的水加熱到80℃,然后停止加熱,并使其溫度保持在60~80℃之間。控制溫度的目的是 ,圖示裝置中缺少的一種必須的玻璃儀器是
②裝置A用于溶解產生的二氧化氯氣體,其中最好盛放 (填字母)。
A.20mL 60℃的溫水 B.100mL冰水
C.100mL飽和食鹽水 D.100mL沸水
③在燒瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加熱,反應后生成ClO2的質量為
(2)用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子()。飲用水中ClO2、
的含量可用連續碘量法進行測定,實驗步驟如下:
步驟1:準確量取一定體積的水樣加入錐形瓶中;
步驟2:調節水樣的pH至7.0~8.0;
步驟3:加入足量的KI晶體;
步驟4:加入少量指示劑,用一定濃度的Na2S2O3溶液滴定至終點;
步驟5:再調節溶液的pH≤2.0;
步驟6:繼續用相同濃度的Na2S2O3溶液滴定至終點。
①步驟1中若要量取20.00mL水樣,則應選用的儀器是
②步驟1~4的目的是測定水樣中ClO2的含量,其反應的化學方程式為:
,則步驟4中加入的指示劑為 ,滴定達到終點時溶液的顏色變化為
③步驟5的目的是使將溶液中的
還原為
以測定其含量,該反應的離子方程式為:
④若飲用水中的含量超標,可向其中加入適量的
將
還原為
,則該反應的氧化產物為 (填化學式)
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省高三上學期第一次月考化學試卷 題型:實驗題
(16分)二氧化氯(ClO2)作為一種高效強氧化劑已被聯合國世界衛生組織(WHO)列為AI級安全消毒劑。常溫下二氧化氯為黃綠色或橘黃色氣體,性質非常不穩定,溫度過高或水溶液中ClO2的質量分數高于30%等均有可能引起爆炸,易與堿液反應生成鹽和水。
(1)某研究小組設計如圖所示實驗制備ClO2溶液,其反應的化學方程式為

 。
。
①在反應開始之前將燒杯中的水加熱到80℃,然后停止加熱,并使其溫度保持在60~80℃之間。控制溫度的目的是_ __,圖示裝置中缺少的一種必須的玻璃儀器是_____________。

②裝置A用于溶解產生的二氧化氯氣體,其中最好盛放_______(填字母)。
a.20mL 60℃的溫水 b.100mL冰水
c.100mL飽和食鹽水 d.100mL沸水
③在燒瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加熱,反應后生成ClO2的質量為______________________
(2)用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子( )。飲用水中ClO2、
)。飲用水中ClO2、 的含量可用連續碘量法進行測定,實驗步驟如下:
的含量可用連續碘量法進行測定,實驗步驟如下:
步驟1:準確量取一定體積的水樣加入錐形瓶中;
步驟2:調節水樣的pH至7.0~8.0;
步驟3:加入足量的KI晶體;
步驟4:加入少量指示劑,用一定濃度的Na2S2O3溶液滴定至終點;
步驟5:再調節溶液的pH≤2.0;
步驟6:繼續用相同濃度的Na2S2O3溶液滴定至終點。
①步驟1中若要量取20.00mL水樣,則應選用的儀器是____________________________。
②步驟1~4的目的是測定水樣中ClO2的含量,其反應的化學方程式為:

 ,則步驟4中加入的指示劑為_________,滴定達到終點時溶液的顏色變化為___________________________。
,則步驟4中加入的指示劑為_________,滴定達到終點時溶液的顏色變化為___________________________。
③步驟5的目的是使 將溶液中的
將溶液中的 還原為
還原為 以測定其含量,該反應的離子方程式為_________________
_____________。
以測定其含量,該反應的離子方程式為_________________
_____________。
查看答案和解析>>
科目:高中化學 來源:2010年河南省唐河三高高二下學期期末考試化學試題 題型:實驗題
(14分)二氧化氯(ClO2)作為一種高效強氧化劑已被聯合國世界衛生組織(WHO)列為AI級安全消毒劑。常溫下二氧化氯為黃綠色或橘黃色氣體,性質非常不穩定,溫度過高或水溶液中ClO2的質量分數高于30%等均有可能引起爆炸,易與堿液反應生成鹽和水。
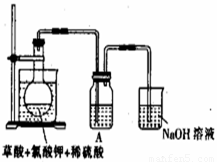
(1)某研究小組設計如圖所示實驗制備ClO2溶液,其反應的化學方程式為
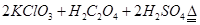
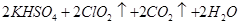
①在反應開始之前將燒杯中的水加熱到80℃,然后停止加熱,并使其溫度保持在60~80℃之間。控制溫度的目的是 ,圖示裝置中缺少的一種必須的玻璃儀器是
②裝置A用于溶解產生的二氧化氯氣體,其中最好盛放 (填字母)。
A.20mL 60℃的溫水 B.100mL冰水
C.100mL飽和食鹽水 D.100mL沸水
③在燒瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加熱,反應后生成ClO2的質量為
(2)用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子(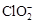 )。飲用水中ClO2、
)。飲用水中ClO2、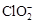 的含量可用連續碘量法進行測定,實驗步驟如下:
的含量可用連續碘量法進行測定,實驗步驟如下:
步驟1:準確量取一定體積的水樣加入錐形瓶中;
步驟2:調節水樣的pH至7.0~8.0;
步驟3:加入足量的KI晶體;
步驟4:加入少量指示劑,用一定濃度的Na2S2O3溶液滴定至終點;
步驟5:再調節溶液的pH≤2.0;
步驟6:繼續用相同濃度的Na2S2O3溶液滴定至終點。
①步驟1中若要量取20.00mL水樣,則應選用的儀器是
②步驟1~4的目的是測定水樣中ClO2的含量,其反應的化學方程式為:

 ,則步驟4中加入的指示劑為
,滴定達到終點時溶液的顏色變化為
,則步驟4中加入的指示劑為
,滴定達到終點時溶液的顏色變化為
③步驟5的目的是使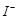 將溶液中的
將溶液中的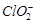 還原為
還原為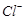 以測定其含量,該反應的離子方程式為:
以測定其含量,該反應的離子方程式為:
④若飲用水中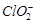 的含量超標,可向其中加入適量的
的含量超標,可向其中加入適量的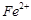 將
將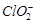 還原為
還原為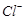 ,則該反應的氧化產物為
(填化學式)
,則該反應的氧化產物為
(填化學式)
查看答案和解析>>
科目:高中化學 來源:09-10年新余一中高二下學期第二次段考化學卷 題型:實驗題
(14分)二氧化氯(ClO2)作為一種高效強氧化劑已被聯合國世界衛生組織(WHO)列為AI級安全消毒劑。常溫下二氧化氯為黃綠色或橘黃色氣體,性質非常不穩定,溫度過高或水溶液中ClO2的質量分數高于30%等均有可能引起爆炸,易與堿液反應生成鹽和水。

(1)某研究小組設計如圖所示實驗制備ClO2溶液,其反應的化學方程式為


①在反應開始之前將燒杯中的水加熱到80℃,然后停止加熱,并使其溫度保持在60~80℃之間。控制溫度的目的是 ,圖示裝置中缺少的一種必須的玻璃儀器是
②裝置A用于溶解產生的二氧化氯氣體,其中最好盛放 (填字母)。
A.20mL 60℃的溫水 B.100mL冰水
C.100mL飽和食鹽水 D.100mL沸水
③在燒瓶中加入12.25g KClO3和9g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加熱,反應后生成ClO2的質量為
(2)用ClO2處理過的飲用水(pH為5.5~6.5)常含有一定量對人體不利的亞氯酸根離子(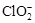 )。飲用水中ClO2、
)。飲用水中ClO2、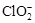 的含量可用連續碘量法進行測定,實驗步驟如下:
的含量可用連續碘量法進行測定,實驗步驟如下:
步驟1:準確量取一定體積的水樣加入錐形瓶中;
步驟2:調節水樣的pH至7.0~8.0;
步驟3:加入足量的KI晶體;
步驟4:加入少量指示劑,用一定濃度的Na2S2O3溶液滴定至終點;
步驟5:再調節溶液的pH≤2.0;
步驟6:繼續用相同濃度的Na2S2O3溶液滴定至終點。
①步驟1中若要量取20.00mL水樣,則應選用的儀器是
②步驟1~4的目的是測定水樣中ClO2的含量,其反應的化學方程式為:

 ,則步驟4中加入的指示劑為
,滴定達到終點時溶液的顏色變化為
,則步驟4中加入的指示劑為
,滴定達到終點時溶液的顏色變化為
③步驟5的目的是使 將溶液中的
將溶液中的 還原為
還原為 以測定其含量,該反應的離子方程式為:
以測定其含量,該反應的離子方程式為:
④若飲用水中 的含量超標,可向其中加入適量的
的含量超標,可向其中加入適量的 將
將 還原為
還原為 ,則該反應的氧化產物為
(填化學式)
,則該反應的氧化產物為
(填化學式)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com