

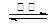 4CO(g) + BaS(s) ΔH1 = +571.2 kJ·mol-1 ①
4CO(g) + BaS(s) ΔH1 = +571.2 kJ·mol-1 ①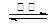 2CO2(g) + BaS(s) ΔH2= +226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) ΔH2= +226.2 kJ·mol-1 ②| A.Na2S溶液的pH比NaHS溶液pH小 |
| B.兩溶液中含有的離子種類不同 |
| C.兩溶液中滴入同體積同濃度的鹽酸,產(chǎn)生氣體速率相等 |
| D.兩溶液中加入NaOH固體,c(S2-)都增大 |
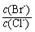 = 。 【已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10】
= 。 【已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10】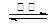 2CO(g)的ΔH =
2CO(g)的ΔH =  HS-+OH-;D、E;(2)2.7×10-3;(3)+172.5KJ/mol;(4)炭過量使BaSO4充分還原
HS-+OH-;D、E;(2)2.7×10-3;(3)+172.5KJ/mol;(4)炭過量使BaSO4充分還原 HS-+OH-。②A.NaHS是H2S 的一級電離產(chǎn)生的,Na2S是H2S 的二級電離產(chǎn)生的,對于多元弱酸來說,一級電離>>二級電離。溶液的酸性主要一級電離決定。根據(jù)鹽的水解規(guī)律:有弱才水解,誰弱誰水解,,越弱越水解,誰強(qiáng)顯誰性。所以溶液的堿性Na2S>NaHS。即Na2S溶液的pH比NaHS溶液pH大。錯(cuò)誤。B.在兩種物質(zhì)的溶液中都含有Na+、S2-、HS-、H2S、H+、OH-。離子種類相同。錯(cuò)誤。C.當(dāng)向Na2S溶液中加入鹽酸時(shí),首先發(fā)生S2-+H+=HS-,沒有氣體產(chǎn)生;然后發(fā)生HS-+H+=H2S↑,放出氣體。而向NaHS溶液中加入鹽酸時(shí)立即發(fā)生HS-+H+=H2S↑,放出氣體。所以兩溶液中滴入同體積同濃度的鹽酸,產(chǎn)生氣體速率不相等。錯(cuò)誤。D.當(dāng)向Na2S和NaHS的溶液中分別加入NaOH溶液時(shí)由于增大了OH-離子的濃度,所以水解平衡:S2-+H2O
HS-+OH-。②A.NaHS是H2S 的一級電離產(chǎn)生的,Na2S是H2S 的二級電離產(chǎn)生的,對于多元弱酸來說,一級電離>>二級電離。溶液的酸性主要一級電離決定。根據(jù)鹽的水解規(guī)律:有弱才水解,誰弱誰水解,,越弱越水解,誰強(qiáng)顯誰性。所以溶液的堿性Na2S>NaHS。即Na2S溶液的pH比NaHS溶液pH大。錯(cuò)誤。B.在兩種物質(zhì)的溶液中都含有Na+、S2-、HS-、H2S、H+、OH-。離子種類相同。錯(cuò)誤。C.當(dāng)向Na2S溶液中加入鹽酸時(shí),首先發(fā)生S2-+H+=HS-,沒有氣體產(chǎn)生;然后發(fā)生HS-+H+=H2S↑,放出氣體。而向NaHS溶液中加入鹽酸時(shí)立即發(fā)生HS-+H+=H2S↑,放出氣體。所以兩溶液中滴入同體積同濃度的鹽酸,產(chǎn)生氣體速率不相等。錯(cuò)誤。D.當(dāng)向Na2S和NaHS的溶液中分別加入NaOH溶液時(shí)由于增大了OH-離子的濃度,所以水解平衡:S2-+H2O HS-+OH-、HS-+H2O
HS-+OH-、HS-+H2O H2S+OH-逆向移動。使c(S2-)都增大。所以正確。E.NaHS=Na++ HS-; HS-發(fā)生水解反應(yīng) HS-+H2O
H2S+OH-逆向移動。使c(S2-)都增大。所以正確。E.NaHS=Na++ HS-; HS-發(fā)生水解反應(yīng) HS-+H2O H2S+OH-要消耗,所以c(Na+) >c(HS-);HS-水解消耗了水電離產(chǎn)生的H+,使H+的濃度減小,最終當(dāng)達(dá)到水的電離平衡時(shí)c(OH-) >c (H+) 。鹽的電離遠(yuǎn)大于弱電解質(zhì)水的電離,所以c(HS-) >c(OH-)。因此E.NaHS溶液中:c(Na+) >c(HS-) >c(OH-) >c (H+) 。正確。(2)向BaCl2溶液中加入AgNO3和KBr,發(fā)生反應(yīng):Ag++Cl-="AgCl↓;" Ag++Br-=AgBr↓.Ksp(AgBr)= C(Ag+)·C(Br-) =5.4×10-13; Ksp(AgCl)= C(Ag+)·C(Cl-)=2.0×10-10當(dāng)兩種沉淀共存時(shí),C(Ag+)相同。
H2S+OH-要消耗,所以c(Na+) >c(HS-);HS-水解消耗了水電離產(chǎn)生的H+,使H+的濃度減小,最終當(dāng)達(dá)到水的電離平衡時(shí)c(OH-) >c (H+) 。鹽的電離遠(yuǎn)大于弱電解質(zhì)水的電離,所以c(HS-) >c(OH-)。因此E.NaHS溶液中:c(Na+) >c(HS-) >c(OH-) >c (H+) 。正確。(2)向BaCl2溶液中加入AgNO3和KBr,發(fā)生反應(yīng):Ag++Cl-="AgCl↓;" Ag++Br-=AgBr↓.Ksp(AgBr)= C(Ag+)·C(Br-) =5.4×10-13; Ksp(AgCl)= C(Ag+)·C(Cl-)=2.0×10-10當(dāng)兩種沉淀共存時(shí),C(Ag+)相同。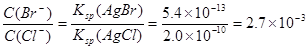 。(3) (①-②)÷2可得:反應(yīng)C(s) + CO2(g)
。(3) (①-②)÷2可得:反應(yīng)C(s) + CO2(g) 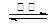 2CO(g)的ΔH =+172.5KJ/mol;(4)實(shí)際生產(chǎn)中必須加入過量的炭,同時(shí)還要通入空氣,其目的是使BaSO4充分還原得到BaS。4的用途、Na2S和NaHS溶液的比較、溶度積常數(shù)的應(yīng)用及熱化學(xué)方程式的書寫等知識。
2CO(g)的ΔH =+172.5KJ/mol;(4)實(shí)際生產(chǎn)中必須加入過量的炭,同時(shí)還要通入空氣,其目的是使BaSO4充分還原得到BaS。4的用途、Na2S和NaHS溶液的比較、溶度積常數(shù)的應(yīng)用及熱化學(xué)方程式的書寫等知識。


| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源:不詳 題型:單選題
| A.-1641.0kJ/mol | B.+3081kJ/mol |
| C.+663.5kJ/mol | D.-2507.0kJ/mol |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
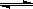 N2(g)+ CO2(g);△H= Q kJ?mol-1。在T1℃時(shí),反應(yīng)進(jìn)行到不同時(shí)間測得各物質(zhì)的濃度如下:
N2(g)+ CO2(g);△H= Q kJ?mol-1。在T1℃時(shí),反應(yīng)進(jìn)行到不同時(shí)間測得各物質(zhì)的濃度如下:| 時(shí)間(min) 濃度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
| N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
| CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
 (1)海水經(jīng)過處理后可以得到無水氯化鎂,無水氯化鎂是工業(yè)制取鎂的原料。試寫出電解熔融氯化鎂制取金屬鎂的化學(xué)反應(yīng)方程式 。
(1)海水經(jīng)過處理后可以得到無水氯化鎂,無水氯化鎂是工業(yè)制取鎂的原料。試寫出電解熔融氯化鎂制取金屬鎂的化學(xué)反應(yīng)方程式 。| 難溶電解質(zhì) | Cu(OH)2 | CuS | Pb(OH)2 | PbS |
| Ksp | 4.8×10-20 | 6.3×10-36 | 1.2×10-15 | 1.0×10-28 |

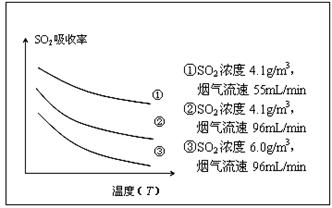
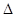 H=-570kJ/mol;
H=-570kJ/mol;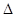 H=-242kJ/mol;
H=-242kJ/mol;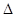 H=—110.5kJ/moL;
H=—110.5kJ/moL;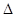 H=—393.5kJ/moL;
H=—393.5kJ/moL;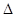 H=+890kJ/moL
H=+890kJ/moL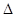 H=akJ/moL;則a= ;該反應(yīng)的熵
H=akJ/moL;則a= ;該反應(yīng)的熵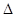 S 0(選填“>”、“=”、“<”);已知自由能
S 0(選填“>”、“=”、“<”);已知自由能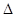 G=
G=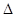 H—T
H—T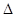 S,當(dāng)
S,當(dāng)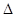 G<0時(shí)可自發(fā)進(jìn)行。則該反應(yīng)在什么條件下可自發(fā)進(jìn)行__________________。
G<0時(shí)可自發(fā)進(jìn)行。則該反應(yīng)在什么條件下可自發(fā)進(jìn)行__________________。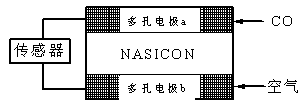
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
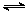 CH3OH(g) △H 1=-90.7 kJ·mol-1
CH3OH(g) △H 1=-90.7 kJ·mol-1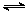 CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1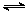 CO2(g)+H2(g) △H 3=-41.2kJ·mol-1
CO2(g)+H2(g) △H 3=-41.2kJ·mol-1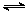 CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。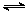 CH3OCH3(g)+H2O(g) △H,其CO的平衡轉(zhuǎn)化率隨溫度、壓強(qiáng)變化關(guān)系如圖1所示,下列說法正確的是 。
CH3OCH3(g)+H2O(g) △H,其CO的平衡轉(zhuǎn)化率隨溫度、壓強(qiáng)變化關(guān)系如圖1所示,下列說法正確的是 。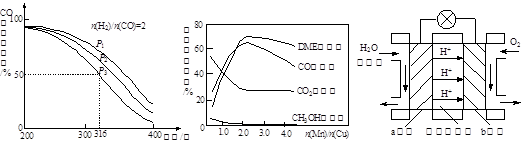
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
 CH3OH(g) ΔH <0。
CH3OH(g) ΔH <0。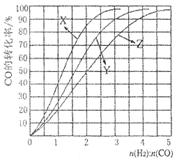
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:單選題
| A.-82kJ/mol | B.-41kJ/mol | C.-312kJ/mol | D.+82kJ/mol |
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題
 SO3(g)+NO(g)
SO3(g)+NO(g) 2SO3(g) ΔH=a kJ·mol-1
2SO3(g) ΔH=a kJ·mol-1 2NO2(g) ΔH=b kJ·mol-1
2NO2(g) ΔH=b kJ·mol-1 SO3(g)+NO(g) ΔH= kJ·mol-1。
SO3(g)+NO(g) ΔH= kJ·mol-1。 SO3(g)+NO(g)。下列事實(shí)中不能說明該反應(yīng)達(dá)到平衡狀態(tài)的是 (選填序號)。
SO3(g)+NO(g)。下列事實(shí)中不能說明該反應(yīng)達(dá)到平衡狀態(tài)的是 (選填序號)。 CH3OH(g)。今在一容積可變的密閉容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡轉(zhuǎn)化率(α)與溫度(T)、壓強(qiáng)(P)的關(guān)系如圖所示:
CH3OH(g)。今在一容積可變的密閉容器中,充有10 mol CO和20 mol H2,用于合成甲醇。CO的平衡轉(zhuǎn)化率(α)與溫度(T)、壓強(qiáng)(P)的關(guān)系如圖所示:
查看答案和解析>>
科目:高中化學(xué) 來源:不詳 題型:填空題


| A.第10min后,向該容器中再充入1molCO2和3molH2,則再次達(dá)到平衡時(shí)c(CH3OH) ="1.5" mol/L |
| B.達(dá)到平衡時(shí),氫氣的轉(zhuǎn)化率為0.75 |
| C.0~10分鐘內(nèi),氫氣的平均反應(yīng)速率為0.075mol/(L?min) |
| D.該溫度下,反應(yīng)的平衡常數(shù)的值為3/16 |
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com