
【題目】研究處理NOx、SO2,對環(huán)境保護有著重要的意義。回答下列問題:
(1)SO2的排放主要來自于煤的燃燒,工業(yè)上常用氨水吸收法處理尾氣中的SO2。已知吸收過程中相關(guān)反應(yīng)的熱化學(xué)方程式如下:① SO2(g) + NH3H2O(aq) =NH4HSO3(aq) △H1 = a kJmol-1;② NH3H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJmol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJmol-1,則反應(yīng) 2SO2(g) + 4NH3H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l) △H = ______。
(2)NOx的排放主要來自于汽車尾氣,有人利用反應(yīng)C (s) + 2NO(g)![]() N2(g) + CO2(g) △H=-34.0 kJmol-1,用活性炭對NO進行吸附。在恒壓密閉容器中加入足量的活性炭和一定量的NO氣體,測得NO的轉(zhuǎn)化率 α(NO)隨溫度的變化如圖所示:
N2(g) + CO2(g) △H=-34.0 kJmol-1,用活性炭對NO進行吸附。在恒壓密閉容器中加入足量的活性炭和一定量的NO氣體,測得NO的轉(zhuǎn)化率 α(NO)隨溫度的變化如圖所示:
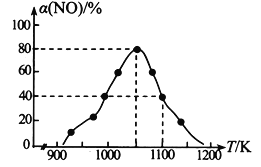
①由圖可知,1050K前反應(yīng)中NO的轉(zhuǎn)化率隨溫度升高而增大,原因是_________________________; 在1100K 時,CO2的體積分數(shù)為______。
②用某物質(zhì)的平衡分壓代替其物質(zhì)的量濃度也可以表示化學(xué)平衡常數(shù)(記作Kp)。在1050K、1.1×106Pa 時,該反應(yīng)的化學(xué)平衡常數(shù)Kp=________(已知:氣體分壓=氣體總壓×體積分數(shù))。
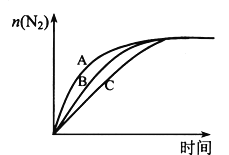
(3)在高效催化劑的作用下用CH4還原NO2,也可消除氮氧化物的污染。在相同條件下,選用A、B、C三種不同催化劑進行反應(yīng),生成 N2的物質(zhì)的量與時間變化關(guān)系如圖所示,其中活化能最小的是_________(填字母標號)。
(4)在汽車尾氣的凈化裝置中 CO和NO發(fā)生反應(yīng):2NO(g) + 2CO(g)![]() N2(g) + 2CO2(g) △H2 =-746.8 kJmol-1。實驗測得,υ正=k正c2(NO) c2(CO) ,υ逆=k逆c(N2) c2(CO2) (k正、k逆為速率常數(shù),只與溫度有關(guān))。
N2(g) + 2CO2(g) △H2 =-746.8 kJmol-1。實驗測得,υ正=k正c2(NO) c2(CO) ,υ逆=k逆c(N2) c2(CO2) (k正、k逆為速率常數(shù),只與溫度有關(guān))。
①達到平衡后,僅升高溫度,k正增大的倍數(shù)_____(填" >”、“< ”或“=”) k逆增大的倍數(shù)。
②若在1L 的密閉容器中充入1 mol CO和1 mol NO,在一定溫度下達到平衡時,CO的轉(zhuǎn)化率為40%,則![]() =_____(保留2位有效數(shù)字)。
=_____(保留2位有效數(shù)字)。
【答案】(2a+2b+c)kJmol-1 1050K前反應(yīng)未達到平衡狀態(tài),隨著溫度升高,反應(yīng)速率加快,NO轉(zhuǎn)化率增大 20% 4 A < 0.25
【解析】
(1)利用蓋斯定律解答。
(2)①在1050K前反應(yīng)未達到平衡狀態(tài),隨著溫度升高,反應(yīng)速率加快,NO轉(zhuǎn)化率增大;達到平衡后,升高溫度,平衡左移,NO的轉(zhuǎn)化率降低。恒溫恒壓下體積分數(shù)等于物質(zhì)的量分數(shù)。
②利用化學(xué)平衡常數(shù)表達式計算。
(3)A反應(yīng)速率快,先達到平衡,故活化能最小。
(4)①正反應(yīng)為放熱反應(yīng),升高溫度平衡左移,則正反應(yīng)速率增大的倍數(shù)小于逆反應(yīng)速率增大的倍數(shù)。
②當反應(yīng)達到平衡時,υ正=υ逆,故![]() =c(N2)c2(CO2)/[c2(NO)c2(CO)]=K。
=c(N2)c2(CO2)/[c2(NO)c2(CO)]=K。
(1)① SO2(g) + NH3H2O(aq) =NH4HSO3(aq) △H1 = a kJmol-1;
② NH3H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJmol-1;
③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJmol-1;
利用蓋斯定律,將①×2+②×2+③可得2SO2(g) + 4NH3H2O(aq) + O2(g) = 2(NH4)2SO4(aq) + 2H2O(l)的△H =(2a+2b+c)kJmol-1,故答案為:(2a+2b+c)kJmol-1。
(2)①在1050K前反應(yīng)未達到平衡狀態(tài),隨著溫度升高,反應(yīng)速率加快,NO轉(zhuǎn)化率增大;達到平衡后,升高溫度,平衡左移,NO的轉(zhuǎn)化率降低。根據(jù)反應(yīng)C (s) + 2NO(g)![]() N2(g) + CO2(g),假設(shè)加入1molNO,在1100K時,NO的轉(zhuǎn)化率為40%,則△n(NO)=0.4mol,故n(CO2)=0.2mol,由于反應(yīng)前后氣體的總物質(zhì)的量不變,故混合氣體中CO2的體積分數(shù)為
N2(g) + CO2(g),假設(shè)加入1molNO,在1100K時,NO的轉(zhuǎn)化率為40%,則△n(NO)=0.4mol,故n(CO2)=0.2mol,由于反應(yīng)前后氣體的總物質(zhì)的量不變,故混合氣體中CO2的體積分數(shù)為![]() %=20%,故答案為:1050K前反應(yīng)未達到平衡狀態(tài),隨著溫度升高,反應(yīng)速率加快,NO轉(zhuǎn)化率增大;20%。
%=20%,故答案為:1050K前反應(yīng)未達到平衡狀態(tài),隨著溫度升高,反應(yīng)速率加快,NO轉(zhuǎn)化率增大;20%。
②根據(jù)反應(yīng)C (s) + 2NO(g)![]() N2(g) + CO2(g),假設(shè)加入1molNO,在1050K時, α(NO)=80%,平衡時n(NO)=0.2mol,n(N2)=0.4mol,n(CO2)=0.4mol,各物質(zhì)的平衡分壓p分(NO)=
N2(g) + CO2(g),假設(shè)加入1molNO,在1050K時, α(NO)=80%,平衡時n(NO)=0.2mol,n(N2)=0.4mol,n(CO2)=0.4mol,各物質(zhì)的平衡分壓p分(NO)=![]() Pa,p分(N2)=
Pa,p分(N2)=![]() ×1.1×106Pa,p分(CO2)=
×1.1×106Pa,p分(CO2)=![]() ×1.1×106Pa,故反應(yīng)的化學(xué)平衡常數(shù)Kp=
×1.1×106Pa,故反應(yīng)的化學(xué)平衡常數(shù)Kp=![]() ×1.1×106Pa×
×1.1×106Pa×![]() ×1.1×106Pa÷(
×1.1×106Pa÷(![]() Pa)2=4,故答案為:4。
Pa)2=4,故答案為:4。
(3)A反應(yīng)速率快,先達到平衡,故活化能最小,故答案為:A。
(4)①正反應(yīng)為放熱反應(yīng),升高溫度平衡左移,則正反應(yīng)速率增大的倍數(shù)小于逆反應(yīng)速率增大的倍數(shù),故k正增大的倍數(shù)小于k逆增大的倍數(shù)。故答案為:<。
②當反應(yīng)達到平衡時,υ正=υ逆,故![]() =c(N2)c2(CO2)/c2(NO)c2(CO)=K,根據(jù)化學(xué)方程式可知,平衡時c (NO)=c(CO)=0.6molL-1,c(N2)=0.2 molL-1,c(CO2)=0.4 molL-1,故
=c(N2)c2(CO2)/c2(NO)c2(CO)=K,根據(jù)化學(xué)方程式可知,平衡時c (NO)=c(CO)=0.6molL-1,c(N2)=0.2 molL-1,c(CO2)=0.4 molL-1,故![]() = c(N2)c2(CO2)/[c2(NO)c2(CO)]=(0.2×0.42)/(0.62×0.62)=20/81≈0.25,故答案為:0.25。
= c(N2)c2(CO2)/[c2(NO)c2(CO)]=(0.2×0.42)/(0.62×0.62)=20/81≈0.25,故答案為:0.25。


 新思維假期作業(yè)寒假吉林大學(xué)出版社系列答案
新思維假期作業(yè)寒假吉林大學(xué)出版社系列答案科目:高中化學(xué) 來源: 題型:
【題目】“84消毒液”因1984年北京某醫(yī)院研制使用而得名,在日常生活中使用廣泛,其有效成分是NaClO。某化學(xué)研究性學(xué)習(xí)小組在實驗室制備NaClO溶液,并進行性質(zhì)探究和成分測定。

(1)該學(xué)習(xí)小組按上圖裝置進行實驗(部分夾持裝置省去),反應(yīng)一段時間后,分別取B、C瓶中的溶液進行實驗,實驗現(xiàn)象如下表。
已知:①飽和NaClO溶液pH為11;
②25°C時,弱酸電離常數(shù)為:H2CO3:K1=4.4×10-7,K2=4.7×10-11;HClO:K=3×10-8
實驗步驟 | 實驗現(xiàn)象 | |
B瓶 | C瓶 | |
實驗1:取樣,滴加紫色石蕊試液 | 變紅,不褪色 | 變藍,不褪色 |
實驗2:測定溶液的pH | 3 | 12 |
回答下列問題:
①儀器a的名稱___________,裝置A中發(fā)生反應(yīng)的離子方程式__________。
②C瓶溶液中的溶質(zhì)是NaCl、__________(填化學(xué)式)。
③若將C瓶溶液換成NaHCO3溶液,按上述操作步驟進行實驗,C瓶現(xiàn)象為:實驗1中紫色石蕊試液立即褪色;實驗2中溶液的pH=7.結(jié)合平衡移動原理解釋紫色石蕊試液立即褪色的原因______
(2)測定C瓶溶液中NaClO含量(單位:g/L)的實驗步驟如下:
Ⅰ.取C瓶溶液20mL于錐形瓶中,加入硫酸酸化,加入過量KI溶液,蓋緊瓶塞并在暗處充分反應(yīng)。
Ⅱ.用0.1000mol/LNa2S2O3標準溶液滴定錐形瓶中的溶液,淀粉溶液顯示終點后,重復(fù)操作2~3次,Na2S2O3溶液的平均用量為24.00mL。(已知:I2+2S2O32-=2I-+S4O62-)
①步驟I的C瓶中發(fā)生反應(yīng)的離子方程式為_________。
②蓋緊瓶塞并在暗處反應(yīng)的原因__________滴定至終點的現(xiàn)象_____________。
③C瓶溶液中NaClO含量為______g/L(保留2位小數(shù))
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】用NA表示阿伏加德羅常數(shù)的值。下列說法正確的是( )
A. 0.1molCH4和0.1molCl2充分反應(yīng),生成的C-Cl鍵和H-Cl鍵的數(shù)目均為0.2NA
B. 7.8gNa2S和Na2O2的混合物中所含陰離子的數(shù)目等于0.2NA
C. 18g固態(tài)水(冰)中含有的氫鍵的數(shù)目為2NA
D. 25℃時,Ksp(AgI)=1.0×10-16,則AgI飽和溶液中Ag+數(shù)目為1.0×10-8NA
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】三氯化硼(BCl3)是一種重要的化工原料。實驗室制備BCl3的原理B2O3+3C+3Cl2 =2BCl3+3CO,某實驗小組利用干燥的氯氣和下列裝置(裝置可重復(fù)使用)制備BCl3并驗證反應(yīng)中有CO生成。(已知:BCl3的熔點為-107.3℃,沸點為12.5℃;硝基苯的密度比水大。)請回答下列問題:

實驗Ⅰ:制備BCl3并驗證產(chǎn)物CO
(1)該實驗裝置中合理的連接順序為G→___→___→__→__→F→D→I;其中裝置E的作用是______。
(2)BCl3接觸潮濕空氣時會形成白霧,請寫出該反應(yīng)的化學(xué)方程式____。
(3)能證明反應(yīng)中有CO生成的現(xiàn)象是_____。
實驗Ⅱ:產(chǎn)品中氯含量的測定
①準確稱取少許m克產(chǎn)品,置于蒸餾水中完全水解,并配成100mL溶液。
②取10.00mL溶液于錐形瓶中
③加入V1mL濃度為C1 mol/LAgNO3溶液使氯離子完全沉淀;向其中加入少許硝基苯用力搖動。
④以硝酸鐵為指示劑,用C2 mol/L KSCN標準溶液滴定過量的AgNO3溶液。重復(fù)步驟②~④二次,達到滴定終點時用去KSCN溶液的平均體積為V2mL。
已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步驟②移取溶液時所需儀器名稱為____,步驟④中達到滴定終點的現(xiàn)象為_____。
(5)產(chǎn)品中氯元素的質(zhì)量分數(shù)為_______。
(6)下列操作,可能引起測得產(chǎn)品中氯含量偏高是_____。
A.步驟③中未加硝基苯
B.步驟①中配制100mL溶液時,定容時俯視刻度線
C.用KSCN溶液滴定剩余AgNO3溶液時,滴定前有氣泡,滴定后無氣泡
D.滴定剩余AgNO3溶液時,KSCN溶液滴到錐形瓶外面一滴
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】元素鉻(Cr)在自然界主要以+3價和+6價存在。請回答下列問題:
(1)+6價的Cr能引起細胞的突變而對人體不利,可用 Na2SO3 將Cr2O72—還原為Cr3+。該反應(yīng)的離子反應(yīng)方程式為___________。
(2)利用鉻鐵礦(FeOCr2O3)冶煉制取金屬鉻的工藝流程如圖所示:

①為加快焙燒速率和提高原料的利用率,可采取的措施之一是__________________________ 。
②“水浸”要獲得浸出液的操作是_________________________________。浸出液的主要成分為Na2CrO4,向“濾液”中加入酸化的氯化鋇溶液有白色沉淀生成,則 “還原”操作中發(fā)生反應(yīng)的離子方程式為___。
③加熱Cr(OH)3可得到Cr2O3,從工業(yè)成本角度考慮,用Cr2O3制取金屬Cr的冶煉方法是 _______。
(3)已知 Cr3+完全沉淀時溶液pH為5,(Cr3+濃度降至10-5molL-1可認為完全沉淀)則Cr(OH)3的溶度積常數(shù) Ksp=_______________。
(4)用石墨電極電解鉻酸鈉(Na2CrO4)溶液,可制重鉻酸鈉(Na2Cr2O7),實驗裝置如圖所示(已知:2Cr![]() +2H+
+2H+![]() Cr2
Cr2![]() + H2O)。
+ H2O)。
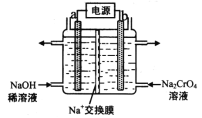
①電極b連接電源的______極(填“正”或“負”) , b 極發(fā)生的電極反應(yīng)式為_________________。
②電解一段時間后,測得陽極區(qū)溶液中Na+物質(zhì)的量由a mol變?yōu)閎 mol,則理論上生成重鉻酸鈉的物質(zhì)的量是 _______________mol 。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】亞硝酰氯(ClNO)是有機物合成中的重要試劑,其沸點為-5.5℃,易水解。已知:AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某學(xué)習(xí)小組在實驗室用Cl2和NO制備ClNO并測定其純度,相關(guān)實驗裝置如圖所示。
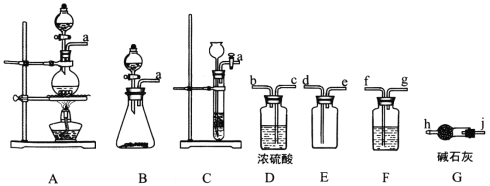
(1)制備Cl2的發(fā)生裝置可以選用___________(填字母代號)裝置,發(fā)生反應(yīng)的離子方程式為___________。
(2)欲收集一瓶干燥的氯氣,選擇合適的裝置,其連接順序為 a→________________(按氣流方向,用小寫字母表示)。
(3)實驗室可用圖示裝置制備亞硝酰氯:
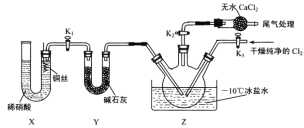
①實驗室也可用 B 裝置制備 NO , X裝置的優(yōu)點為___________________________________。
②檢驗裝置氣密性并裝入藥品,打開K2,然后再打開K3,通入一段時間氣體,其目的是____________,然后進行其他操作,當Z中有一定量液體生成時,停止實驗。
(4)已知:ClNO 與H2O反應(yīng)生成HNO2和 HCl。
①設(shè)計實驗證明 HNO2是弱酸:_____________。(僅提供的試劑:1 molL-1鹽酸、 1 molL-1HNO2溶液、 NaNO2溶液、紅色石蕊試紙、藍色石蕊試紙)。
②通過以下實驗測定ClNO樣品的純度。取Z中所得液體m g 溶于水,配制成250 mL 溶液;取出25.00 mL樣品溶于錐形瓶中,以K2CrO4溶液為指示劑,用c molL-1 AgNO3標準溶液滴定至終點,消耗標準溶液的體積為20.00mL。滴定終點的現(xiàn)象是__________,亞硝酰氯(ClNO)的質(zhì)量分數(shù)為_________。(已知: Ag2CrO4為磚紅色固體; Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】由相同金屬電極及其不同濃度的鹽溶液組成的電池,稱濃差電池,電子由溶液濃度較小的一極流向濃度較大的一極。如圖所示裝置中,X電極與Y電極初始質(zhì)量相等。進行實驗時,先閉合K2,斷開K1,一段時間后,再斷開K2,閉合K1,即可形成濃差電池,電流計指針偏轉(zhuǎn)。下列不正確的是( )
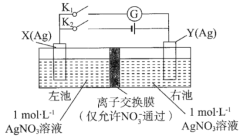
A. 充電前,該電池兩電極存在電勢差
B. 放電時,右池中的NO3-通過離了交換膜移向左池
C. 充電時,當外電路通過0.1 mol電子時,兩電極的質(zhì)量差為21.6g
D. 放電時,電極Y為電池的正極
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】已知A是化學(xué)實驗室中最常見的有機物,它易溶于水并有特殊香味;B的產(chǎn)量可以衡量一個國家石油化工發(fā)展的水平,有關(guān)物質(zhì)的轉(zhuǎn)化關(guān)系如圖所示(部分反應(yīng)條件、產(chǎn)物省略):(已知 2R-CHO + O2→2R-COOH R為烴基)
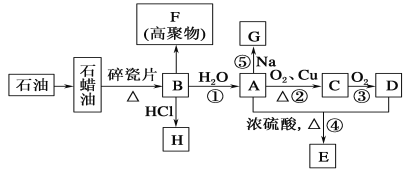
回答下列問題:
(1)①決定化合物A的化學(xué)特性的原子團的名稱為________;F的結(jié)構(gòu)簡式為______________。
②B到A的反應(yīng)類型為________,A到C的反應(yīng)類型為________;
(2)寫出下列反應(yīng)的化學(xué)方程式:
反應(yīng)②:______________________________________,
反應(yīng)⑤:________________________________________。
(3)工業(yè)上制備H有以下兩種方案:
Ⅰ.乙烷與氯氣反應(yīng); Ⅱ.乙烯與氯化氫反應(yīng)。
你認為最合理的方案是(填代號)________,理由是_________________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
【題目】新型鎂-鋰雙離子二次電池如圖,下列關(guān)于該電池的說法不正確的是

A. 放電時,Li+由左向右移動
B. 放電時,正極的電極反應(yīng)式為Li1-xFePO4+xLi++xe-= LiFePO4
C. 充電時,外加電源的正極與Y相連
D. 充電時,導(dǎo)線上每通過1mol e-,左室溶液質(zhì)量減輕12g
查看答案和解析>>
國際學(xué)校優(yōu)選 - 練習(xí)冊列表 - 試題列表
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com