
【題目】已知下列數據:
物質 | 熔點(℃) | 沸點(℃) | 密度(g·cm-3) |
乙醇 | -117.0 | 78.0 | 0.79 |
乙酸 | 16.6 | 117.9 | 1.05 |
乙酸乙酯 | -83.6 | 77.5 | 0.90 |
某學生在實驗室制取乙酸乙酯的主要步驟如下:

①配制2 mL濃硫酸、3 mL乙醇(含18O)和2 mL乙酸的混合溶液。
②按上圖連接好裝置(裝置氣密性良好)并加入混合液,用小火均勻加熱3 min~5 min。
③待試管乙收集到一定量產物后停止加熱,撤出試管乙并用力振蕩,然后靜置待分層。
④分離出乙酸乙酯,洗滌、干燥。
(1)反應中濃硫酸的作用是______________________________________;
寫出制取乙酸乙酯的化學方程式:_____________________________。
(2)上述實驗中飽和碳酸鈉溶液的作用是________(填字母)。
A.中和乙酸和乙醇 B.中和乙酸并吸收乙醇
C.減少乙酸乙酯的溶解 D.加速酯的生成,提高其產率
(3)步驟②中需要小火均勻加熱,其主要理由是___________________;
步驟③所觀察到的現象是_____________________________________;
欲將乙試管中的物質分離以得到乙酸乙酯,必須使用的儀器有________;分離時,乙酸乙酯應從儀器________(填“下口放”或“上口倒”)出。
【答案】 催化劑 吸水劑 CH3COOH+CH3CH![]() OH
OH![]() CH3CO18OCH2CH3+H2O BC 大火加熱會導致大量的原料汽化而損失 有氣泡產生,液體分層,上層為無色有香味液體,下層為淺紅色液體,振蕩后下層液體顏色變淺 分液漏斗 上口倒
CH3CO18OCH2CH3+H2O BC 大火加熱會導致大量的原料汽化而損失 有氣泡產生,液體分層,上層為無色有香味液體,下層為淺紅色液體,振蕩后下層液體顏色變淺 分液漏斗 上口倒
【解析】(1)酯化反應是可逆反應,在酯化反應中濃硫酸的主要是催化劑、吸收劑;在酯化反應中羧酸提供羥基,醇提供氫原子,反應的化學方程式為CH3COOH+CH3CH![]() OH
OH![]() CH3CO18OCH2CH3+H2O;(2)乙酸具有酸性,能和飽和碳酸鈉溶液反應而把被吸收,乙酸乙酯在飽和碳酸鈉溶液中的溶解度較小,易于分離,答案為BC;(3)反應物中乙醇、乙酸的沸點較低,若用大火加熱,大量反應物隨產物蒸發而損失原料,溫度過高還可能發生其他副反應,所以為防止乙醇、乙酸揮發,造成原料的損失,應小火加熱;(4)碳酸鈉水解呈堿性,乙酸乙酯不溶于飽和碳酸鈉溶液,密度比水小,有香味,振蕩時乙酸和碳酸鈉反應而使溶液紅色變淺,因此步驟③所觀察到的現象是:試管B中的液體分成上下兩層,上層無色,下層為紅色液體,振蕩后下層液體的紅色變淺;乙酸乙酯不溶于水,欲將乙試管中的物質分離以得到乙酸乙酯,必須使用的儀器有分液漏斗;乙酸乙酯密度小于水,分離時,乙酸乙酯應從儀器上口倒出。
CH3CO18OCH2CH3+H2O;(2)乙酸具有酸性,能和飽和碳酸鈉溶液反應而把被吸收,乙酸乙酯在飽和碳酸鈉溶液中的溶解度較小,易于分離,答案為BC;(3)反應物中乙醇、乙酸的沸點較低,若用大火加熱,大量反應物隨產物蒸發而損失原料,溫度過高還可能發生其他副反應,所以為防止乙醇、乙酸揮發,造成原料的損失,應小火加熱;(4)碳酸鈉水解呈堿性,乙酸乙酯不溶于飽和碳酸鈉溶液,密度比水小,有香味,振蕩時乙酸和碳酸鈉反應而使溶液紅色變淺,因此步驟③所觀察到的現象是:試管B中的液體分成上下兩層,上層無色,下層為紅色液體,振蕩后下層液體的紅色變淺;乙酸乙酯不溶于水,欲將乙試管中的物質分離以得到乙酸乙酯,必須使用的儀器有分液漏斗;乙酸乙酯密度小于水,分離時,乙酸乙酯應從儀器上口倒出。


 口算題卡加應用題集訓系列答案
口算題卡加應用題集訓系列答案 綜合自測系列答案
綜合自測系列答案科目:高中化學 來源: 題型:
【題目】已知A、B、C、D、E、F都是周期表中前四周期的元素,它們的核電荷數依次增加。相關信息如下表所示,根據推斷回答下列問題:(答題時A、B、C、D、E、F用所對應的元素符號表示)
A | A原子核外電子有6種不同的運動狀態 |
B | B元素的第一電離能比同周期相鄰兩個元素都大 |
C | C原子在同周期原子中半徑最大(稀有氣體除外),其單質焰色為黃色 |
D | D原子最外層電子數等于電子層數 |
E | E的基態原子最外層電子排布式為3s23p2 |
F | F與C位于不同周期,F原子核外最外層電子數與C相同,其余各層電子均充滿 |
(1)F基態原子核外價電子排布式是________________
(2)A、B、E三種元素電負性由大到小排列順序為__________________
(3)B元素可形成多種單質,其中“只有一層原子厚”的物質,被公認為目前世界上已知的最薄、最堅硬、傳導電子速度最快的新型材料,該材料晶體結構如右圖所示,其原子的雜化類型為________________

(4)煤燃燒產生的煙氣中有B的氧化物,會引起嚴重的環境問題,因此,常用AH4催化還原以消除污染,已知:
AH4(g)+2 BO2(g)= B2(g)+AO2(g)+2H2O (g) △H1=-867kJ/mol
2BO2(g) ![]() B2O4(g) △H2=-56.9 kJ/mol
B2O4(g) △H2=-56.9 kJ/mol
寫出AH4和B2O4反應的熱化學方程式__________________
(5)D單質為面心立方晶體,其晶胞邊長a=0.405nm,用NA表示阿伏伽德羅常數,列式表示D單質的密度______g·cm-3(不必計算出結果)。
(6)繼A60后,科學家又合成了E60、B60, E60分子中每個E原子只跟相鄰的3個原子形成共價鍵,且每個E原子最外層都滿足8電子穩定結構,則E60分子中π鍵的數目為_______________
(7)F的單質和過氧化氫在稀硫酸中可反應,有人將這個反應設計成原電池,請寫出該原電池正極反應方程式_______________
(8)某學生所做的有關F元素的實驗流程如下圖:
F單質![]() 棕色的煙
棕色的煙![]() 綠色溶液
綠色溶液![]() 藍色沉淀
藍色沉淀![]() 藍色溶液
藍色溶液![]() 黑色沉淀
黑色沉淀
請書寫第⑤步反應的離子方程式:___________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分子式為C9H18O2的有機物A有下列轉化關系:

其中B、C的相對分子質量相等,則A的可能的結構簡式有( )
A.6種 B.7種 C.8種 D.9種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有下述有機反應類型①消去反應,②水解反應,③加聚反應,④加成反應,⑤還原反應,⑥氧化反應,以丙醛為原料制取 1,2-丙二醇,所需進行的反應類型依次是( )
A. ⑥④②①B. ⑤②④①C. ①③②⑤D. ⑤①④②
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)維生素A對人體特別是對人的視力有重要作用,其結構簡式如下:

1 mol該化合物可與________mol Br2發生加成反應。
(2)在有機反應中,反應物相同而條件不同,可得到不同的主產物,下式中R代表烴基,副產物均已略去。

(請注意H和Br加成的位置)
請寫出實現下列轉變的各步反應的化學方程式,特別注意寫明反應條件。
①由CH3CH2CH2CH2Br分兩步轉變為CH3CH2CHBrCH3:__________________;___________________。
②由(CH3)2CHCH===CH2分兩步轉變為(CH3)2CHCH2CH2OH:__________________;____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. HCl、HBr、HI的熔、沸點最低的是 HCl
B. 磷原子核外有15個運動狀態完全不同的電子
C. 硝酸易揮發是因為形成分子內氫鍵
D. 甲烷分子間也可以形成氫鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的說法正確的是( )
A. 2-甲基丁烷也稱異丁烷B. 由乙烯生成乙醇屬于加成反應
C. C4H9Cl有3種同分異構體D. 糖類屬于高分子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】燃料電池是燃料(如CO、H2、CH4)等跟O2(或空氣)起反應將化學能轉變為電能的裝置,電解質溶液是強堿(如KOH)溶液,下列關于甲烷燃料電池的說法中不正確的是( )
A.通入氧氣的一極發生還原反應,通入甲烷的一極發生氧化反應
B.負極的電極反應式為CH4+10OH--8e-=CO32—+7H2O
C.隨著反應的進行,電解質溶液的pH保持不變
D.甲烷燃料電池的能量利用率比甲烷燃燒的大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.有機化學反應因條件不同,可生成不同的產物。
己知:
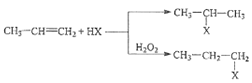 X為鹵素原子
X為鹵素原子
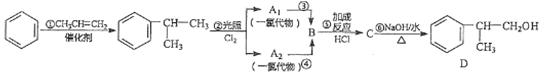
回答下列問題:
(1)反應①的反應類型:________;
(2)A1的結構簡式:__________;
(3)反應⑤的化學方程式:__________;
(4)滿足下列條件的D的同分異構體有______種。
①含有苯環 ②分子中有2個甲基 ③有-OH
II.鹵代烴(R-X)在醇類溶劑中與Mg反應可制得格氏試劑。格氏試劑在有機合成方面用途廣泛。
已知: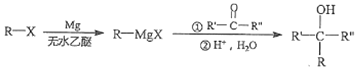 (R表示羥基,R′表示烴基或氫)
(R表示羥基,R′表示烴基或氫)
現鹵代烴E有如下轉化關系:
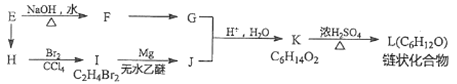
試回答下列問題:
(1)K的結構簡式是__________。
(2)L中含有的官能團名稱是__________。
(3)聚苯乙烯(PS)是一種多功能塑料,廣泛應用子食品包裝,絕緣板,商業機器設備等許多日常生活領域中。現在以G和苯為主要原料制備PS的單休苯乙烯,請寫出合成路線流程圖(無機試劑任選)_______________。
合成路線流程圖可參照II的己知寫法,箭頭后僅寫主要有機產物,箭頭上為反應所需試劑、反應條件。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com