
【題目】科學家冶煉出了純度高達99.9999%的鐵,你估計它不會具有的性質是
A.在潮濕的空氣中放置不易生銹B.硬度比生鐵大
C.與2mol/L鹽酸的反應生成氫氣D.在冷的濃H2SO4溶液中可鈍化
科目:高中化學 來源: 題型:
【題目】工業上設計用CO2來生產燃料甲醇,既減少二氧化碳氣體,又得到寶貴的能源物質.為了探究反應原理,現進行如下實驗:在體積為1L的密閉容器中,充入1molCO2和3molH2 , 某溫度下發生反應:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.0KJ/mol.測得CO2和CH3OH(g)的濃度隨時間變化如圖所示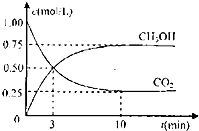
(1)該反應該溫度下,化學平衡常數的值為
(2)下列說法中能作為反應達到平衡狀態標志的是(填字母).
A.容器內壓強不再發生變化
B.平均相對分子質量不再變化
C.c(CO2)和c(H2)之比等于1:3
D.相同時間內每斷裂3molH﹣H鍵,同時斷裂3molO﹣H鍵
(3)下列措施中能使 ![]() 減小的是
減小的是
A.再充入1molCO2和3molH2
B.將H2O(g)從體系中分離
C.充入He(g),使體系壓強增大
D.升高溫度.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關表示正確的是( )
A.過氧化鈣(CaO2)的電子式: ![]()
B.某微粒的結構示意簡圖為 ![]() ,則該元素在周期表中位于第三周期、VIA族
,則該元素在周期表中位于第三周期、VIA族
C.H2CO3的電離方程式:H2CO32H++CO32﹣
D.葡萄糖的結構簡式:C6H12O6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A.某溫度下,水的離子積常數Kw=10﹣13 , 在此溫度下,將pH=12的NaOH溶液Va L與pH=2的硫酸Vb L混合,所得溶液呈中性,則Va:Vb=1:10
B.已知醋酸電離平衡常數為Ka;醋酸根水解常數為Kh;水的離子積為Kw;則三者關系為KaKh=Kw
C.常溫下,pH=1的強酸溶液,加水稀釋后,溶液中各離子濃度均降低
D.甲、乙兩溶液都是強電解質,已知甲溶液的pH是乙溶液pH的兩倍,則甲、乙兩溶液等體積混合,混合液pH可能等于7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應既屬于氧化還原反應,又是吸熱反應的是
A.鈉與冷水的反應B.甲烷在氧氣中的燃燒反應
C.灼熱的木炭與CO2反應D.Ba(OH)2·8H2O晶體與NH4Cl晶體的反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究銅與6molL﹣1硝酸反應的氣態產物中是否含NO2 , 進行如下實驗.
已知:FeSO4+NO[Fe(NO)]SO4(棕色),該反應較緩慢,待生成一定量[Fe(NO)]2+時突顯明顯棕色.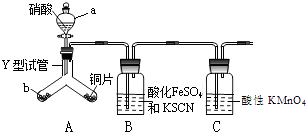
(1)實驗前需檢驗裝置的氣密性,簡述操作 .
(2)儀器a的名稱
(3)實驗開始時先將Y形試管向盛有塊狀固體b的支管傾斜,緩慢滴入稀硝酸,該實驗操作的目的是;
(4)證明有NO2的實驗現象
(5)裝置C的作用 , 反應離子方程式 .
(6)測定化學試劑綠礬(FeSO47H2O)純度的方法:稱取綠礬3.000g置于錐形瓶中,加入100mL蒸餾水,加入10mLH2SO4和5mLH3PO4 , 用0.1000molL﹣1KMnO4溶液滴定至終點,消耗KMnO4溶液20.00mL.KMnO4溶液盛放在棕色式(填“酸”或“堿”)滴定管中,列式計算綠礬的純度 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】物質分類是化學研究的重要方法之一。近年來發現,在金星大氣層中存在三氧化二碳。下列物質與它屬于同類的是 ( )
A. H2、O3 B. H2SO4、H2CO3 C. SO2、NO D. Na2SO3、KClO3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com