
【題目】以黃鐵礦為原料制硫酸產生的硫酸渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。現以硫酸渣制備鐵紅(Fe2O3),過程如下:
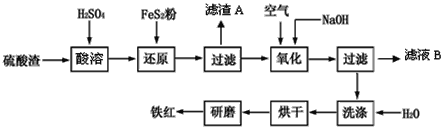
(1)酸溶過程中Fe2O3與稀硫酸反應的離子方程式是____。
(2)還原過程中加入FeS2是將溶液中的Fe3+ 還原為Fe2+,而本身被氧化為SO42-,寫出有關的離子方程式:_____。
(3)生產過程中,為了確保鐵紅的質量,氧化過程需要調節溶液的pH的范圍是__。
(部分陽離子以氫氧化物形式沉淀時溶液的pH見表)
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
開始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(二)把NaOH、MgCl2、AlCl3三種固體組成的混合物溶于足量水后,產生1.16g白色沉淀,再向所得濁液中逐漸加入1.00mol/LHCl溶液,加入HCl溶液的體積與生成沉淀的關系如圖所示。
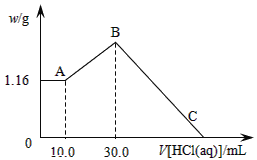
(1)原混合物中NaOH的質量是____g。
(2)C點(此時沉淀恰好完全溶解)HCl溶液的體積為___mL。
(三)二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑。回答下列問題:
實驗室用NH4Cl、鹽酸、NaClO2(亞氯酸鈉)為原料,通過如圖1過程制備ClO2:
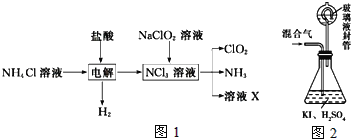
用如圖2裝置可以測定混合氣中ClO2的含量:
Ⅰ、在錐形瓶中加入足量的碘化鉀,用50mL水溶解后,再加入3mL稀硫酸;
Ⅱ、在玻璃液封裝置中加入水,使液面沒過玻璃液封管的管口;
Ⅲ、將一定量的混合氣體通入錐形瓶中吸收;
Ⅳ、將玻璃液封裝置中的水倒入錐形瓶中;
Ⅴ、用0.1000molL1硫代硫酸鈉標準溶液滴定錐形瓶中的溶液(I2+2S2O32-═2I+S4O62-),指示劑顯示終點時共用去20.00mL硫代硫酸鈉溶液。在此過程中:
①測得混合氣中ClO2的質量為___g。
②用ClO2處理過的飲用水會含有一定量的亞氯酸鹽。若要除去超標的亞氯酸鹽,下列物質最適宜的是___(填標號).
a.明礬 b.碘化鉀 c.鹽酸 d.硫酸亞鐵
【答案】Fe2O3+6H+=2Fe3++3H2O FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+ 3.2~3.8 5.20 130.0 0.02700 d
【解析】
硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不與酸反應的SiO2,加入FeS2將溶液中的Fe3+還原為Fe2+,再加氫氧化鈉和空氣,調節溶液的pH的范圍是3.2~3.8主要是使三價鐵沉淀,而二價鎂,三價鋁都不沉淀,最后洗滌、烘干、研磨使氫氧化鐵分解生成氧化鐵,從而得到鐵紅。
(1)氧化鐵與硫酸反應生成硫酸鐵和水,方程式為:Fe2O3+3H2SO4═Fe2(SO4) 3+3H2O;離子方程式為Fe2O3+6H+=2Fe3++3H2O,故答案為:Fe2O3+6H+=2Fe3+ +3H2O。
(2)FeS2中S元素的化合價從-1價升高到+6價,2個S原子轉移14個電子,Fe3+轉移1個電子,則二者的計量數之比為1:14,根據S守恒可知SO42-前面的化學計量數為2,根據氧守恒可知H20前面化學計量數為8,根據H守恒可知H+前化學計量數為16,則反應的離子方程式為:FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+,檢驗Fe3+被完全還原的實驗操作和現象為取少量試液于試管中,滴入幾滴KSCN溶液,若不顯紅色,則說明Fe3 +已被完全還原,故答案為:FeS2+14Fe3 + +8H2O=15Fe2++2SO42-+16H+。
(3)溶液pH>3.2時Fe3+沉淀完全,溶液pH=3.8時Al3+開始沉淀,故溶液的pH的范圍是3.2~3.8,根據幾種離子沉淀的pH,如果pH過大,Al3+、Mg2+形成沉淀,使制得的鐵紅不純;故答案為:3.2~3.8。
(二)A~B階段消耗鹽酸的物質的量=(0.03L-0.01L)×1.0mol/L=0.02mol,則根據方程式NaAlO2+HCl+H2O=Al(OH)3↓+NaCl可知生成氫氧化鋁的物質的量=0.02mol。所以根據原子守恒可知原混合物中氯化鋁的物質的量是0.02mol。B點沉淀達到最大值,此時的沉淀是氫氧化鎂和氫氧化鋁的混合物。而溶液則恰好是氯化鈉溶液。根據氯離子守恒可知氯化鈉的物質的量=0.03L×1.00mol/L+0.02mol×2+0.02mol×3=0.13mol。所以根據鈉離子守恒可知,氫氧化鈉的物質的量也是0.13mol,因此氫氧化鈉的質量m=n· M=40g/mol×0.13mol=5.2g。B~C階段加入的鹽酸開始溶解氫氧化鋁和氫氧化鎂,此時反應的方程式為Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O。根據氫氧化鎂和氫氧化鋁均是0.02mol可知,該階段消耗鹽酸的物質的量是0.02mol×2+0.02mol×3=0.10mol,其體積是0.10mol÷1mol/L=0.1L=100mL,所以C點(此時沉淀恰好完全溶解)HCl溶液的體積為30mL+100mL=130.0mL,故答案為:130.0mL。
(三)①含有Na2S2O3物質的量為0.02L×0.1mol/L=0.002mol,則:
根據關系式:2ClO2~5I2~10Na2S2O3,
2 10
n(ClO2) 0.002mol
所以n(ClO2)=0.0004mol,所以m(ClO2)=0.0004 mol×67.5g/mol=0.02700g,故答案為:0.02700。
②若要除去超標的亞氯酸鹽,ac均不能還原亞氯酸鹽,b中KI具有還原性但氧化產物不適合飲用水使用,只有d中Fe2+將ClO2-還原成Cl-,Fe2+ 被氧化為鐵離子,且鐵離子水解生成膠體可凈化飲用水,則最適宜的是d,故答案為:d。


科目:高中化學 來源: 題型:
【題目】閱讀下列材料后回答有關問題
一個體重50kg的健康人,體內含鐵元素2g,這2g鐵元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以給貧血者補充鐵時,應補充含Fe2+的亞鐵鹽(如FeSO4),服用維生素C可使食物中的Fe轉化成Fe2+,有利于人體對鐵的吸收
(1)人體中經常進行Fe2+與Fe3+的轉化,在此轉化過程中,Fe2+作_______劑(填氧化或還原,下同),被__________
(2)“服用維生素C可使食物中的Fe3+轉化為Fe2+這句話說明,維生素C在這個反應中作____劑(填氧化或還原,下同),具有_______性
(3)補血劑的主要成分是FeSO4請寫出產物有FeSO4的符合要求的化學方程式:
①置換反應:__________________________
②復分解反應:__________________________
(4)有人在研究硫酸亞鐵(FeSO4)熱穩定性時,作出了兩種假設
①假設它按CaCO3受熱分解的方式分解,反應的化學方程式為_________________________
②假設它按KClO3受熱分解的方式分解,已知產物都是氧化物,其中有兩種酸性氧化物生成,則分解反應的化學方程式為____________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】結合圖回答問題:如圖是中學化學中常用于混合物的分離和提純的裝置,請根據裝置回答問題:
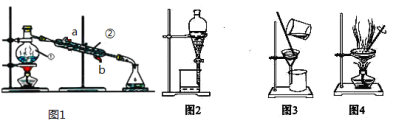
(1)寫出上述裝置中儀器的名稱:①________。
(2)若利用上述裝置分離乙酸(沸點118℃)和乙酸乙酯(沸點77.1℃)的混合物,還缺少的儀器有________,圖1中儀器 ②是從______口進水(填a或b)。
(3)圖2在分液時為使液體順利滴下,除打開活塞外,還應進行的具體操作是______
(4)從氯化鉀溶液中得到氯化鉀固體,選擇裝置______(填代表裝置圖的序號,下同);除去自來水中的Cl等雜質,選擇裝置______。
(5)實驗室常用上述裝置分離碘水中的碘,進行該操作時,需在碘水中加一試劑,在選擇試劑時,下列性質你認為哪些性質是必需的:________(填序號)。
①常溫下為液態 ②I2在其中溶解程度大 ③與水互不相容 ④密度要比水大。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組利用如圖裝置進行鐵與水蒸氣反應的實驗,并檢驗產物的性質,請回答下列問題:
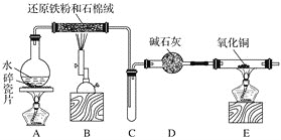
(1)A裝置的作用是____________,燒瓶底部放碎瓷片的作用是_____________。
(2)裝置B中發生反應的化學方程式是____________________________________,該反應中氧化劑是__________,氧化產物是_____________。
(3)D的作用是____________________________。
(4)E中的實驗現象是_____________________。
(5)該同學對反應后硬質試管中固體物質的組成提出了如下假設:
假設1:只有Fe;
假設2:只有________;
假設3:既有Fe也有Fe3O4。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(一)某工廠排放出有毒物質NOCl,它遇水就會生成NO3-。NOCl分子中各原子均滿足8電子穩定結構,則NOCl的電子式為_____。水源中的NO3-對人類健康會產生危害。為了降低水源中NO3-的濃度,有研究人員建議在堿性條件下用鋁粉將NO3-還原為N2,該反應的離子方程式為____
(二)某工廠用FeCl3溶液腐蝕鍍有銅的絕緣板生產印刷電路,發生反應的化學方程式為:2FeCl3+Cu==2FeCl2+CuCl2。實驗小組的同學對生產印刷電路板的廢液成分進行了如下探究:
①取少量廢液,滴加KSCN溶液顯紅色。
②取100mL廢液,加入足量的AgNO3溶液,析出沉淀43.05g。
③另取100mL廢液,加入一定質量的銅片,充分反應后,測得銅片的質量減少了2.56g,再向反應后的溶液中滴加KSCN溶液不變色。
根據探究實驗得出結論:
(1)廢液中含有的金屬離子是______。
(2)100mL廢液中Cl-的物質的量是______。
(3)原100mL廢液中銅離子的物質的量濃度是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為二氧化錳的有關轉化關系圖,下列有關說法中不正確的是( )
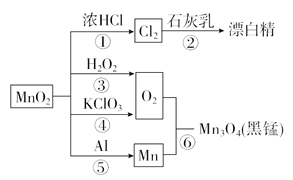
A. 反應①~⑥均屬于氧化還原反應
B. 反應⑤中氧化劑與還原劑的物質的量之比為3∶4
C. 相同條件下生成等量的O2,反應③和④轉移的電子數之比為1∶1
D. 反應①生成的Cl2經干燥后,可用鋼瓶貯運
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的值。下列說法正確的是
A. 標準狀況下,0.1mol Cl2溶于水,轉移的電子數目為0.1NA
B. 標準狀況下,2.24L NO和2.24L O2混合后氣體分子數為0.15 NA
C. 加熱條件下,1mol Fe投入足量的濃硫酸中,生成NA個SO2分子
D. 0.1mol Na2O2與足量的潮濕的二氧化碳反應轉移的電子數為0.1NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】輝銅礦主要成分Cu2S,此外還含有少量SiO2、Fe2O3等雜質,軟錳礦主要含有MnO2,以及少量SiO2、Fe2O3等雜質.研究人員開發綜合利用這兩種資源,用同槽酸浸濕法冶煉工藝,制備硫酸錳晶體和堿式碳酸銅。主要工藝流程如下:
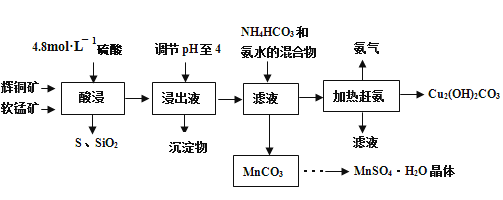
已知:
①MnO2有較強的氧化性,能將金屬硫化物中的硫氧化為單質硫;
②[Cu(NH3)4]SO4常溫穩定,在熱水溶液中會分解生成NH3;
③部分金屬陽離子生成氫氧化物沉淀的pH范圍(開始沉淀和完全沉淀的pH):
Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4
④MnSO4·H2O溶于1份冷水、0.6份沸水,不溶于乙醇。
(1)實驗室配制250mL 4.8molL-1的稀硫酸,所需的玻璃儀器除玻璃棒、量筒、燒杯以外還需要________________________。
(2)酸浸時,為了提高浸取率可采取的措施有_____________________(任寫一點)。
(3)酸浸時,得到浸出液中主要含有CuSO4、MnSO4等。寫出該反應的化學方程式:__________。
(4)調節浸出液pH=4的作用是______________。
(5)本工藝中可循環使用的物質是____________(寫化學式)。
(6)獲得的MnSO4H2O晶體需要進一步洗滌、干燥,洗滌時應用_____________洗滌。
(7)測定MnSO4H2O樣品的純度:準確稱取樣品14.00g,加蒸餾水配成100mL溶液,取出25.00mL用標準的BaCl2溶液測定,完全反應后得到了4.66g沉淀,則此樣品的純度為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】與下列反應對應的離子方程式書寫正確的是
A. 鐵跟稀硫酸反應 2Fe+6H+=2Fe3++3H2↑
B. 碳酸鈣溶于醋酸 CaCO3+2H+=Ca2++H2O+CO2↑
C. Na2CO3溶液的水解 CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. 碳酸鎂跟硫酸反應 MgCO3+2H+=Mg2++H2O+CO2↑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com