
硫酸亞鐵銨[(NH4)2SO4·FeSO4·6H2O]為淺綠色晶體,易溶于水,不溶于酒精,在水中的溶解度比FeSO4或(NH4)2SO4都要小。實驗室中常以廢鐵屑為原料來制備,其步驟如下: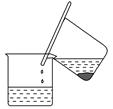
圖1
步驟1:鐵屑的處理。將廢鐵屑放入熱的碳酸鈉溶液中浸泡幾分鐘后,用圖1所示方法分離出固體并洗滌、干燥。
步驟2:FeSO4溶液的制備。將處理好的鐵屑放入錐形瓶,加入過量的3 mol·
L-1H2SO4溶液,加熱至充分反應為止。趁熱過濾(如圖2所示),收集濾液和洗滌液。
圖2
步驟3:硫酸亞鐵銨的制備。向所得FeSO4溶液中加入飽和(NH4)2SO4溶液,經過加熱濃縮、冷卻結晶、過濾、乙醇洗滌后得到硫酸亞鐵銨晶體。
請回答下列問題:
(1)步驟1中圖1分離方法稱為________法。
(2)步驟2中有一處明顯不合理的是___________________________________。
趁熱過濾的理由是________________________________________________。
(3)步驟3加熱濃縮過程中,當________時停止加熱。用無水乙醇洗滌晶體的原因是______________________________________________________________。
(4)FeSO4·7H2O在潮濕的空氣中易被氧化成Fe(OH)SO4·3H2O,寫出該反應的化學方程式________________________________________________________。
科目:高中化學 來源: 題型:實驗題
Na2SO3、SO2是中學常見的物質。
(1)某同學用下圖示裝置制取干燥純凈的SO2。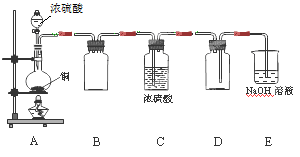
寫出制取SO2氣體的化學方程式 。請指出D裝置中的錯誤 。若實驗過程中不慎在皮膚上沾少量濃硫酸,處理的方法是 。
(2)向燒堿和Na2SO3的混合溶液中加入少量溴水,振蕩后溶液變為無色。反應后的溶液中含有大量的SO32-、SO42-、Br-、OH-等陰離子,請填寫鑒定其中SO32-、SO42-和Br-的實驗報告。限選試劑:2 mol/LHCl,1 mol/L H2SO4,l mol/LBaCl2,l mol/LBa(NO3)2,0.1 mol/LAgNO3,CCl4,新制飽和溴水,新制飽和氯水。
| 編號 | 實驗操作 | 預期現象和結論 |
| 步驟① | 在試管A中加入少量待測液,加入足量氯水,再加入四氯化碳,振蕩,靜置后觀察顏色。 | ,證明待測液中含Br-。 |
| 步驟② | 在試管B中加入少量待測液, | 有白色沉淀生成, 證明待測液中含SO42-。 |
| 步驟③ | 在試管C中加入少量待測液,滴加2 mol/LHCl至溶液呈酸性,加入幾滴______(填試劑),振蕩。 | , 證明待測液中含SO32-。 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
乙酰水楊酸俗稱阿司匹林(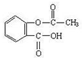 ),是世界上應用最廣泛的解熱、鎮痛和抗炎藥。乙酰水楊酸受熱易分解,分解溫度為128℃~135℃。實驗室以水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O]為主要原料合成阿司匹林,其制備原理為:
),是世界上應用最廣泛的解熱、鎮痛和抗炎藥。乙酰水楊酸受熱易分解,分解溫度為128℃~135℃。實驗室以水楊酸(鄰羥基苯甲酸)與醋酸酐[(CH3CO)2O]為主要原料合成阿司匹林,其制備原理為:


制備基本操作流程如下:
主要試劑和產品的物理常數如下表:
| 名稱 | 相對分子質量 | 熔點或沸點(℃) | 水 |
| 水楊酸 | 138 | 158(熔點) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸點) | 反應 |
| 乙酰水楊酸 | 180 | 135(熔點) | 微溶 |


 ),最終稱得產品質量為2.2g,則所得乙酰水楊酸的產率為 (百分數精確到0.1)。
),最終稱得產品質量為2.2g,則所得乙酰水楊酸的產率為 (百分數精確到0.1)。查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
固體硝酸鹽加熱易分解且產物較復雜。某學習小組以Mg(NO3)2為研究對象,擬通過實驗探究其熱分解的產物,提出如下4種猜想:
甲:Mg(NO2)2、NO2、O2
乙:MgO、NO2、O2
丙:Mg3N2、O2
丁:MgO、NO2、N2
(1)實驗小組成員經討論認定猜想丁不成立,理由是______________________________。
查閱資料得知:2NO2+2NaOH=NaNO3+NaNO2+H2O
針對甲、乙、丙猜想,設計如下圖所示的實驗裝置(圖中加熱、夾持儀器等均省略):
(2)實驗過程
①儀器連接后,放入固體試劑之前,關閉k,微熱硬質玻璃管(A),觀察到E中有氣泡連續放出,表明__________。
②稱取Mg(NO3)2固體3.7 g置于A中,加熱前通入N2以驅盡裝置內的空氣,其目的是________;關閉k,用酒精燈加熱時,正確操作是先________,然后固定在管中固體部位下加熱。
③觀察到A中有紅棕色氣體出現,C、D中未見明顯變化。
④待樣品完全分解,A裝置冷卻至室溫、稱量,測得剩余固體的質量為1.0 g。
⑤取少量剩余固體于試管中,加入適量水,未見明顯現象。
(3)實驗結果分析討論
①根據實驗現象和剩余固體的質量經分析可初步確認猜想______是正確的。
②根據D中無明顯現象,一位同學認為不能確認分解產物中有O2,因為若有O2,D中將發生氧化還原反應:______________(填寫化學方程式),溶液顏色會褪去;小組討論認定分解產物中有O2存在,未檢測到的原因是_____________________________________。
③小組討論后達成的共識是上述實驗設計仍不完善,需改進裝置進一步探究。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某化學學習小組在實驗室中探究鐵釘與熱濃硫酸的反應。其探究流程如圖所示: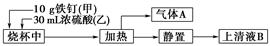
(1)從實驗安全的角度考慮,應先向燒杯中加入______(填“甲”或“乙”)。
(2)根據加入的反應物的量,實驗需要選取的燒杯的規格為________(填字母序號)。
a.50 mL b.100 mL c.500 mL d.1 000 mL
(3)上述流程圖中從“靜置”后的混合物中得到上清液B不能采用過濾的操作方法,其原因是__________________________________。
由于鐵釘生銹,上清液B中可能既含Fe3+,又含Fe2+,要檢驗上清液B中有無Fe2+,應加入的試劑是________(填字母序號)。
a.KSCN溶液和氯水
b.鐵粉和KSCN溶液
c.NaOH溶液
d.酸性KMnO4溶液
(4)氣體A的主要成分是SO2,還可能含有H2和CO2。流程圖中“加熱”時可能生成CO2的原因是________________(用化學方程式表示)。
利用下列儀器可以同時檢驗氣體A中是否含有H2和CO2(其中的夾持儀器、橡膠管和加熱裝置已經略去),則儀器的連接順序是________(填儀器的字母代號),裝置A的作用是____________________________,裝置B中試劑X的化學式是________。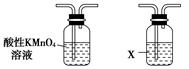
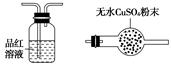
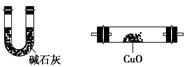
A B C D E F
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
乙二酸(H2C2O4)俗稱草酸,是一種重要的化工原料。查閱資料,了解到以下有關信息:
①乙二酸易溶于水,加熱至100℃開始升華,125℃時迅速升華,157℃時大量升華并開始分解。乙二酸受熱分解生成水、二氧化碳和一種常見的還原性氣體。
②乙二酸的鈣鹽——乙二酸鈣為不溶于水的白色晶體。
(1)請寫出乙二酸受熱分解的化學方程式______________________。
(2)化學興趣小組的同學用實驗證明乙二酸晶體受熱分解生成的氣體成分。他們利用下圖提供的裝置,自選試劑,提出了下列實驗方案:按A→B→C→C→C→D→E順序從左至右連接裝置,檢驗乙二酸晶體受熱分解生成的氣體成分。
請你按整套裝置從左至右的順序填寫下表中的空格:
| 儀器符號 | 儀器中所加物質 | 裝置作用 |
| B | | |
| C | | |
| C | 氫氧化鈉濃溶液 | |
| C | | |
| D | | |
| E | | |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某興趣小組探究SO2氣體還原Fe3+、I2,他們使用的藥品和裝置如圖所示: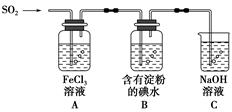
(1)SO2氣體還原Fe3+的產物是________(填離子符號),參加反應的SO2和Fe3+的物質的量之比是________。
(2)下列實驗方案適用于在實驗室制取所需SO2的是________。
A.Na2SO3溶液與HNO3 B.Na2SO3固體與濃硫酸
C.固體硫在純氧中燃燒 D.銅與熱濃H2SO4
(3)裝置C的作用是____________________________________。
(4)若要從A中所得溶液提取晶體,必須進行的實驗操作步驟:蒸發、冷卻結晶、過濾、自然干燥,在這一系列操作中沒有用到的儀器有________(填序號)。
A.蒸發皿 B.石棉網
C.漏斗 D.燒杯 E.玻璃棒 F.坩堝
(5)在上述裝置中通入過量的SO2,為了驗證A中SO2與Fe3+發生了氧化還原反應,他們取A中的溶液,分成三份,并設計了如下實驗:
方案①:往第一份試液中加入酸性KMnO4溶液,紫紅色褪去。
方案②:往第二份試液中加入KSCN溶液,不變紅,再加入新制的氯水,溶液變紅。
方案③:往第三份試液中加入用稀鹽酸酸化的BaCl2,產生白色沉淀。
上述方案不合理的是________,原因是__________________________
______________________________________________。
(6)能表明I-還原性弱于SO2的現象是_____________________________
___________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
資料顯示:鎂與飽和碳酸氫鈉溶液反應產生大量氣體和白色不溶物。某同學設計了如下實驗方案并驗證產物、探究反應原理。
(1)提出假設
實驗Ⅰ:用砂紙擦去鎂條表面氧化膜,將其放入盛有適量滴有酚酞的飽和碳酸氫鈉溶液的試管中,迅速反應,產生大量氣泡和白色不溶物,溶液由淺紅變紅。
該同學對反應中產生的白色不溶物做出如下猜測:
猜測1:白色不溶物可能為________________。
猜測2:白色不溶物可能為MgCO3。
猜測3:白色不溶物可能是堿式碳酸鎂[xMgCO3·yMg(OH)2]。
(2)設計定性實驗確定產物并驗證猜測:
| 實驗序號 | 實驗 | 實驗現象 | 結論 |
| 實驗Ⅱ | 將實驗Ⅰ中收集到的氣體點燃 | 能安靜燃燒、產生淡藍色火焰 | ①氣體成分為________ |
| 實驗Ⅲ | ②取實驗Ⅰ中的白色不溶物,洗滌,加入足量________ | ③________________ __________________ __________________ | 白色不溶物可能含有MgCO3 |
| 實驗Ⅳ | 取實驗Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 產生白色沉淀 | ④溶液中存在________ |

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某化學研究性學習小組探究Fe3+和SO32-之間發生的反應。
(1)取5mLFeCl3濃溶液于試管中,逐滴加入Na2SO3濃溶液,觀察到溶液顏色由黃色變為紅棕色,繼續加入Na2SO3濃溶液至過量,溶液顏色加深,最終變為紅褐色。無氣泡產生,無沉淀生成。這種紅褐色液體是___________________。
(2)除了觀察到以上的現象外,有成員提出了另一種可能:發生氧化還原反應。反應的離子方程式為 。
研究性學習小組設計了兩種實驗方案證明發生了氧化還原反應。請把實驗方案補充完整:
方案一:檢驗溶液中含有Fe2+證明發生了氧化還原反應
方案二:檢驗溶液中含有 證明發生了氧化還原反應
實驗用品:0.1mol/L BaCl2、3mol/L鹽酸、0.1mol/LKMnO4(H+)、氯水、20%KSCN、0.5mol/LKI;試管若干、膠頭滴管若干
Ⅰ預處理:將(1)中獲得的混合物放在如圖裝置中處理足夠時間。
Ⅱ檢驗過程
| 操 作 | 現象及結論 |
| 基于方案一: | |
| 基于方案二: | |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com