
【題目】下列金屬中,表面自然形成的氧化層能保護內層金屬不被空氣氧化的是( )
A. K B. Na C. Fe D. Al
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列反應屬于吸熱反應的是
A. Fe片與稀H2SO4的反應 B. Ba(OH)28H2O和NH4Cl反應
C. 鹽酸和氫氧化鈉的反應 D. 鎂條在空氣中的燃燒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,針對表中的①~⑧中元素,回答以下問題:
主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在③~⑦元素中,原子半徑最大的是__________用元素符號或化學式填空,下同),其離子的原子結構示意圖為________。
(2)元素的最高價氧化物對應的水化物中酸性最強的是_____;堿性最強的是______,寫出該物質和呈兩性的氫氧化物的化學反應方程式____________________;
(span>3)在以上元素的單質中,化學性質最不活潑的是____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇是一種可再生能源,具有開發和應用的廣闊前景,工業上采用如下反應合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
(1)分析該反應并回答下列問題:
①該反應的平衡常數表達式為K=____________。
②下列選項能判斷該反應達到平衡狀態的依據有__________(填序號)。
A.2v(正)(H2)= v(逆)(CO)
B.一定條件下,單位時間內消耗2molH2的同時生成 1mol CH3OH
C.恒溫、恒容時,容器內的壓強不再變化
D.恒溫、恒容時,容器內混合氣體的密度不再變化
E.混合氣體的平均相對分子質量不隨時間而變化
(2))下圖是該反應在不同溫度下CO轉化率隨時間的變化曲線:
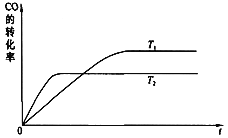
①該反應的△H________0(填“>”、“<”或“=”)。
②T1和T2溫度下的平衡常數:K1 ________ K2(填“>”、“<”或“=”)。
(3)某溫度下,將2 mol CO和6 mol H2充入2L的密閉容器中,充分反應,達到平衡后,測得c(CO)= 0.2 mol/L,則CO的轉化率為________________。
(4)已知在常溫常壓下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O(g) ΔH1=-1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH2=-566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH3=-44.0 kJ/mol
寫出甲醇不完全燃燒生成一氧化碳和液態水的熱化學方程式________________________。
(5)2009年10月,中國科學院長春應用化學研究所在甲醇燃料電池技術方面獲得新突破,組裝出了自呼吸電池及主動式電堆。甲醇燃料電池的工作原理如圖所示。
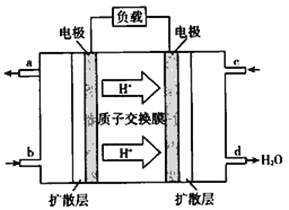
①該電池工作時,b口通入的物質為__________(填 化學式,下同),c 口通入的物質為__________。 ②該電池正極的電極反應式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某原電池結構如圖所示,回答下列問題:
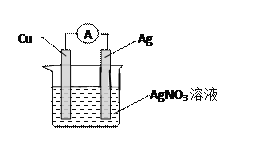
(1)銅作原電池的_______極,發生_______反應 ,電極反應式為 _____________________ ;
(2)銀作原電池的_______極,發生_______反正,電極反應式為 _____________________;
(3)電子從_______經外電路流向_______,銀離子向_______極移動,硝酸根離子向_______極移動(填“正極”或“負極”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:△G=△H-T△S,當△G<0,反應能自發進行,△G>0反應不能自發進行。某反應2AB(g)C(g)+3D(g)在高溫時能自發進行,在低溫下不能自發進行,則該反應的正反應的△H、△S應為
A.ΔH<0,△S<0B.△H<0, △S>0
C.△H>0,△S<0D.△H>0,△S>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、W四種金屬片在稀鹽酸中,用導線連接,可以組成原電池,實驗結果如圖所示:則四種金屬的活潑性由強到弱的順序為( )
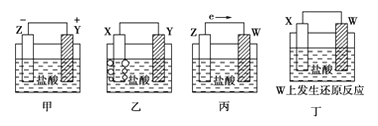
A. Z>Y>X>WB. Z>X>Y>WC. Z>Y>W>XD. Y>Z>X>W
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com