
【題目】實驗室配制物質的量濃度均為0.2mol/L 的NaCl溶液和稀H2SO4 各480mL.提供的試劑是:NaCl固體和98%的濃H2SO4(密度為1.84g/cm3)及蒸餾水.
(1)應用托盤天平稱量NaClg,應用10mL量筒量取H2SO4mL;
(2)配制兩種溶液時都需要的儀器是;
(3)稀釋濃H2SO4時應注意;
(4)在配制上述溶液實驗中,下列操作引起結果偏低的有(填序號)
A.在燒杯中溶解溶質攪拌時,濺出少量溶液
B.沒有用蒸餾水洗燒杯2~3次,并將洗液移入容量瓶中
C.定容時,加水超過了刻度線,倒出一些再重新加水到刻度線
D.將所配溶液從容量瓶轉移到試劑瓶時,有少量濺出
E.把配好的溶液倒入剛用蒸餾水洗凈的試劑瓶中備用
F.容量瓶剛用蒸餾水洗凈,沒有烘干
G.量筒量取濃H2SO4后沒有用蒸餾水洗滌2~3次,并將洗液移入容量瓶中.
H.容量瓶加水定容時俯視刻度線.
【答案】
(1)5.9;5.4
(2)燒杯、玻璃棒、500ml容量瓶、膠頭滴管
(3)將濃硫酸沿燒杯內壁注入水中,邊倒邊用玻璃棒攪拌
(4)ABCE
【解析】解:(1)配制480mL0.2mol/L 的NaCl溶液,應選擇500mL容量瓶,需要溶質的質量m=0.2mol/L×58.5g/mol×0.5L=5.9g; 98%的濃H2SO4(密度為1.84g/cm3)的物質的量濃度c= ![]() =18.4mol/L,配制480mL0.2mol/L 的稀H2SO4 , 應選擇500mL容量瓶,設需要濃硫酸體積為V,則依據溶液稀釋過程中所含溶質的物質的量不變得:0.2mol/L×0.5L=18.4mol/L×V,解得V=0.0054L,即5.4mL;所以答案是:5.9;5.4;(2)配制NaCl溶液的步驟是計算、稱量、溶解、洗滌、定容、搖勻、裝瓶,用到的儀器是:托盤天平、燒杯、玻璃棒、500ml容量瓶、膠頭滴管;配制稀H2SO4的步驟是計算、量取、稀釋、洗滌、定容、搖勻、裝瓶,用到的儀器是:量筒、燒杯、玻璃棒、500ml容量瓶、膠頭滴管;配制兩種溶液時都需要儀器:燒杯、玻璃棒、500ml容量瓶、膠頭滴管;所以答案是:燒杯、玻璃棒、500ml容量瓶、膠頭滴管;(3)由于濃硫酸密度大、溶于水放熱,故稀釋濃硫酸的方法:將濃硫酸沿燒杯內壁注入水中,邊倒邊用玻璃棒攪拌.所以答案是:將濃硫酸沿燒杯內壁注入水中,邊倒邊用玻璃棒攪拌;(4)A、在燒杯中溶解溶質攪拌時,濺出少量溶液,導致溶質的物質的量偏低,溶液濃度偏低,故A選;B、沒有用蒸餾水洗燒杯2~3次,并將洗液移入容量瓶中,導致溶質的物質的量偏低,溶液濃度偏低,故B選;C、定容時,加水超過了刻度線,倒出一些再重新加水到刻度線,導致溶質的物質的量偏低,溶液濃度偏低,故C選;D、將所配溶液從容量瓶轉移到試劑瓶時,有少量濺出,溶液濃度不變,故D不選;E、把配好的溶液倒入剛用蒸餾水洗凈的試劑瓶中備用,溶液稀釋,溶液濃度降低,故E選;F、容量瓶剛用蒸餾水洗凈,沒有烘干,對溶質的物質的量和溶液的體積都不產生影響,溶液濃度不變,故F不選;G、量筒量取濃H2SO4后沒有用蒸餾水洗滌2~3次,并將洗液移入容量瓶中,量取的濃硫酸物質的量偏大,溶液濃度偏高,故G不選;H、容量瓶加水定容時俯視刻度線,導致溶液的體積偏低,溶液濃度偏高,故H不選;故選:ABCE;
=18.4mol/L,配制480mL0.2mol/L 的稀H2SO4 , 應選擇500mL容量瓶,設需要濃硫酸體積為V,則依據溶液稀釋過程中所含溶質的物質的量不變得:0.2mol/L×0.5L=18.4mol/L×V,解得V=0.0054L,即5.4mL;所以答案是:5.9;5.4;(2)配制NaCl溶液的步驟是計算、稱量、溶解、洗滌、定容、搖勻、裝瓶,用到的儀器是:托盤天平、燒杯、玻璃棒、500ml容量瓶、膠頭滴管;配制稀H2SO4的步驟是計算、量取、稀釋、洗滌、定容、搖勻、裝瓶,用到的儀器是:量筒、燒杯、玻璃棒、500ml容量瓶、膠頭滴管;配制兩種溶液時都需要儀器:燒杯、玻璃棒、500ml容量瓶、膠頭滴管;所以答案是:燒杯、玻璃棒、500ml容量瓶、膠頭滴管;(3)由于濃硫酸密度大、溶于水放熱,故稀釋濃硫酸的方法:將濃硫酸沿燒杯內壁注入水中,邊倒邊用玻璃棒攪拌.所以答案是:將濃硫酸沿燒杯內壁注入水中,邊倒邊用玻璃棒攪拌;(4)A、在燒杯中溶解溶質攪拌時,濺出少量溶液,導致溶質的物質的量偏低,溶液濃度偏低,故A選;B、沒有用蒸餾水洗燒杯2~3次,并將洗液移入容量瓶中,導致溶質的物質的量偏低,溶液濃度偏低,故B選;C、定容時,加水超過了刻度線,倒出一些再重新加水到刻度線,導致溶質的物質的量偏低,溶液濃度偏低,故C選;D、將所配溶液從容量瓶轉移到試劑瓶時,有少量濺出,溶液濃度不變,故D不選;E、把配好的溶液倒入剛用蒸餾水洗凈的試劑瓶中備用,溶液稀釋,溶液濃度降低,故E選;F、容量瓶剛用蒸餾水洗凈,沒有烘干,對溶質的物質的量和溶液的體積都不產生影響,溶液濃度不變,故F不選;G、量筒量取濃H2SO4后沒有用蒸餾水洗滌2~3次,并將洗液移入容量瓶中,量取的濃硫酸物質的量偏大,溶液濃度偏高,故G不選;H、容量瓶加水定容時俯視刻度線,導致溶液的體積偏低,溶液濃度偏高,故H不選;故選:ABCE;


 七彩題卡口算應用一點通系列答案
七彩題卡口算應用一點通系列答案科目:高中化學 來源: 題型:
【題目】下列關于同分異構體數目的敘述不正確的是( )
A.甲苯苯環上的1個氫原子被含3個碳原子的烷基取代,所得產物有6種
B.已知丙烷的二氯代物有4種異構體,則其六氯代物的異構體數目也為4種
C.含有5個碳原子的某飽和鏈烴,其一氯代物有3種
D.菲的結構為 ,它與硝酸反應,可生成5種一硝基取代物
,它與硝酸反應,可生成5種一硝基取代物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知1g氫氣完全燃燒生成水蒸氣時放出熱量121kJ,且氧氣中1mol O=O鍵完全斷 裂時吸收熱量496kJ,氫氣中1mol H﹣H鍵斷裂時吸收熱量為436kJ,求水蒸氣中1mol H﹣O鍵形成時放出熱量( )
A.463kJ
B.557kJ
C.486kJ
D.188kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在相同條件下,兩個體積相等的容器,一個充滿一氧化氮氣體,另一個充滿氮氣和氧氣的混合氣體,這兩個容器內一定具有相同的
A、原子總數 B、質子總數 C、電子總數 D、質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知鋅及其化合物的性質與鋁及其化合物相似。如圖,橫坐標為溶液的pH,縱坐標為Zn2+或[Zn(OH)4]2-的物質的量濃度(假設Zn2+濃度為10-5 mol·L-1時,Zn2+已沉淀完全)。下列說法不正確的是( )
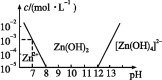
A.往ZnCl2溶液中加入足量氫氧化鈉溶液,離子方程式為Zn2++4OH-![]() [Zn(OH)4]2-
[Zn(OH)4]2-
B.從圖中數據計算可得Zn(OH)2的溶度積Ksp=10-17
C.某廢液中含Zn2+,沉淀Zn2+可以控制溶液pH的范圍是8~12
D.向1 L 1 mol·L-1 ZnCl2溶液中加入NaOH固體至pH=6,需NaOH 2 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】固定容積為2L的密閉容器中發生反應xA(g)+yB(g)zC(g),圖I表示t℃時容器中各物質的量隨時間的變化關系,圖II表示平衡常數K隨溫度變化的關系.結合圖象判斷,下列結論正確的是( ) 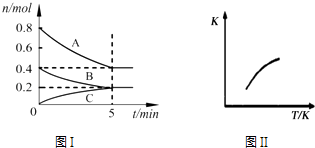
A.該反應可表示為:2A(g)+B(g)C(g)△H<0
B.t℃時該反應的平衡常數K=6.25
C.當容器中氣體密度不再變化時,該反應達到平衡狀態
D.t℃,在第6 min時再向體系中充入0.4 mol C,再次達到平衡時C的體積分數大于0.25
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于金屬鈉的敘述中正確的是( )
A. 金屬鈉可以保存在少量水中 B. 金屬鈉是銀白色, 但露置于空氣中會變暗
C. 鈉在空氣中燃燒生成白色的 Na2O D. 鈉投入CuSO4溶液中可觀察到有紅色物質析出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A.含氧酸能起氧化作用,無氧酸則不能
B.陽離子只有氧化性,陰離子只有還原性
C.失電子難的原子獲得電子的能力一定強
D.化學反應中,某元素由化合態變成游離態,此元素可能被氧化,也可能被還原
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com