
| ||
| △ |
| 11.2L |
| 22.4L/mol |
| 4.48L |
| 22.4L/mol |
| 0.1mol |
| 0.2mol |


 期末沖刺100分創新金卷完全試卷系列答案
期末沖刺100分創新金卷完全試卷系列答案科目:高中化學 來源:2012屆江蘇省淮安市范集中學高三第一次全真模擬測試化學試卷(帶解析) 題型:填空題
(12分)過氧化氫和臭氧都是常見的綠色氧化劑,在工業生產中有著重要的用途。
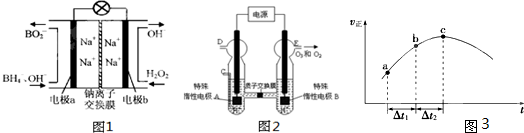
(1)據報道以硼氫化合物NaBH4(B的化合價為+3價)和H2O2作原料的燃料電池,可用作通信衛星電源。負極材料采用Pt/C,正極材料采用MnO2,其工作原理如圖7所示。該電池放電時正極的電極反應式為: ;以MnO2做正極材料,可能是因為 。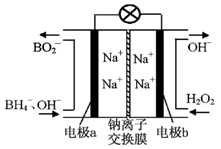
(2)火箭發射常以液態肼(N2H4)為燃料,液態過氧化氫為助燃劑。
已知:N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H =" –" 534 kJ·mol—1
H2O2(l) = H2O(l) + 1/2O2(g) △H =" –" 98.64 kJ·mol—1
H2O(l) = H2O(g) △H=" +" 44kJ·mol—1
反應N2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) 的△H= 。
(3)O3 可由臭氧發生器(原理如圖所示)電解稀硫酸制得。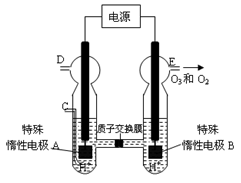
①圖中陰極為 (填“A”或“B”)。
②若C處通入O 2,則A極的電極反應式為: 。
③若C處不通入O 2 ,D、E處分別收集到11.2L和有4.48L氣體(標準狀況下),則E處收集的氣體中O3所占的體積分數為 (忽略 O 3 的分解)。 (4)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx 95%以上是以NO形式存在的,可發生反應NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應,正反應速率隨時間變化的示意圖(如圖9)所示。由圖可得出的正確說法是
(4)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx 95%以上是以NO形式存在的,可發生反應NO(g)+ O3 (g) NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應,正反應速率隨時間變化的示意圖(如圖9)所示。由圖可得出的正確說法是 
a.反應在c點達到平衡狀態
b.反應物濃度:b點小于c點
c.反應物的總能量低于生成物的總能量
d.Δt1=Δt2時,NO的轉化率:a~b段小于b~c段
查看答案和解析>>
科目:高中化學 來源:2013屆江蘇省鹽城市明達中學高三上學期學情調研考試化學試卷(帶解析) 題型:填空題
(14 分)過氧化氫和臭氧都是常見的綠色氧化劑,在工業生產中有著重要的用途。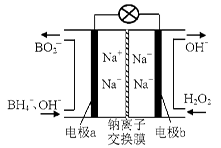
(1)據報道以硼氫化合物NaBH4(B的化合價為+3價)和H2O2作原料的燃料電池,可用作通信衛星電源。負極材料采用Pt/C,正極材料采用MnO2,其工作原理如右圖所示。該電池放電時正極的電極反應式為: ;
以MnO2做正極材料,可能是因為 。
(2)火箭發射常以液態肼(N2H4)為燃料,液態過氧化氫
為助燃劑。已知:
N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H =" –" 534 kJ·mol-1
H2O2(l) = H2O(l) + 1/2O2(g) △H =" –" 98.64 kJ·mol-1
H2O(l) = H2O(g) △H=" +" 44kJ·mol-1
則反應N2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) 的△H= 。
(3)O3 可由臭氧發生器(原理如右圖所示)電解稀硫酸制得。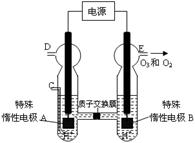
② 圖中陰極為 (填“A”或“B”)。
②若C處通入O 2,則A極的電極反應式為: 。
③若C處不通入O 2 ,D、E處分別收集到15.68L和有6.72L氣體(標準狀況下),則E處收集的氣體中O2和O3的體積之比為 (忽略 O 3 的分解)。
(4)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx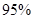 以上是以NO形式存在的,可發生反應NO(g)+ O3 (g)
以上是以NO形式存在的,可發生反應NO(g)+ O3 (g) 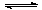 NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應 ,正反應速率隨時間變化的示意圖(如下圖)所示。由圖可得出的正確說法是
NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應 ,正反應速率隨時間變化的示意圖(如下圖)所示。由圖可得出的正確說法是 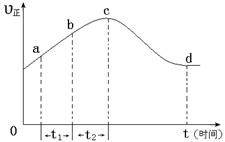
a.反應在c點達到平衡狀態
b.反應物濃度:b點小于c點
c.該反應為放熱反應
d.Δt1=Δt2時,NO的轉化量:a~b段小于b~c段
查看答案和解析>>
科目:高中化學 來源:2012-2013學年江蘇省鹽城市高三上學期學情調研考試化學試卷(解析版) 題型:填空題
(14 分)過氧化氫和臭氧都是常見的綠色氧化劑,在工業生產中有著重要的用途。
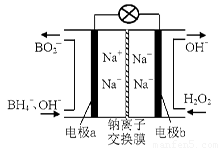
(1)據報道以硼氫化合物NaBH4(B的化合價為+3價)和H2O2作原料的燃料電池,可用作通信衛星電源。負極材料采用Pt/C,正極材料采用MnO2,其工作原理如右圖所示。該電池放電時正極的電極反應式為: ;
以MnO2做正極材料,可能是因為 。
(2)火箭發射常以液態肼(N2H4)為燃料,液態過氧化氫
為助燃劑。已知:
N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H =" –" 534 kJ·mol-1
H2O2(l) = H2O(l) + 1/2O2(g) △H =" –" 98.64 kJ·mol-1
H2O(l) = H2O(g) △H=" +" 44kJ·mol-1
則反應N2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) 的△H= 。
(3)O3 可由臭氧發生器(原理如右圖所示)電解稀硫酸制得。
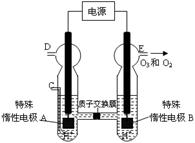
② 圖中陰極為 (填“A”或“B”)。
②若C處通入O 2,則A極的電極反應式為: 。
③若C處不通入O 2 ,D、E處分別收集到15.68L和有6.72L氣體(標準狀況下),則E處收集的氣體中O2和O3的體積之比為 (忽略 O 3 的分解)。
(4)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx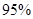 以上是以NO形式存在的,可發生反應NO(g)+ O3 (g)
以上是以NO形式存在的,可發生反應NO(g)+ O3 (g)  NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應 ,正反應速率隨時間變化的示意圖(如下圖)所示。由圖可得出的正確說法是
NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應 ,正反應速率隨時間變化的示意圖(如下圖)所示。由圖可得出的正確說法是
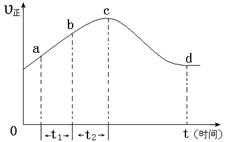
a.反應在c點達到平衡狀態
b.反應物濃度:b點小于c點
c.該反應為放熱反應
d.Δt1=Δt2時,NO的轉化量:a~b段小于b~c段
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省淮安市高三第一次全真模擬測試化學試卷(解析版) 題型:填空題
(12分)過氧化氫和臭氧都是常見的綠色氧化劑,在工業生產中有著重要的用途。
(1)據報道以硼氫化合物NaBH4(B的化合價為+3價)和H2O2作原料的燃料電池,可用作通信衛星電源。負極材料采用Pt/C,正極材料采用MnO2,其工作原理如圖7所示。該電池放電時正極的電極反應式為: ;以MnO2做正極材料,可能是因為 。
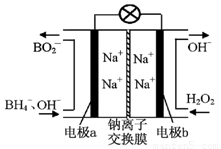
(2)火箭發射常以液態肼(N2H4)為燃料,液態過氧化氫為助燃劑。
已知: N2H4(g) + O2(g) = N2(g) + 2H2O(g) △H = – 534 kJ·mol—1
H2O2(l) = H2O(l) + 1/2O2(g) △H = – 98.64 kJ·mol—1
H2O(l) = H2O(g) △H= + 44kJ·mol—1
反應N2H4(g) + 2H2O2(l) = N2(g) + 4H2O(g) 的 △H= 。
(3)O3 可由臭氧發生器(原理如圖所示)電解稀硫酸制得。
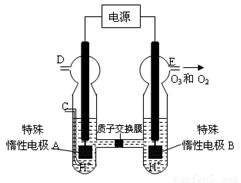
①圖中陰極為 (填“A”或“B”)。
②若C處通入O 2,則A極的電極反應式為: 。
③若C處不通入O 2 ,D、E處分別收集到11.2L和有4.48L氣體(標準狀況下),則E處收集的氣體中O3所占的體積分數為 (忽略 O 3 的分解)。
 (4)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx 95%以上是以NO形式存在的,可發生反應NO(g)+ O3
(g) NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應 ,正反應速率隨時間變化的示意圖(如圖9)所示。由圖可得出的正確說法是
(4)新型O3氧化技術對燃煤煙氣中的NOx和SO2脫除效果顯著,鍋爐煙氣中的NOx 95%以上是以NO形式存在的,可發生反應NO(g)+ O3
(g) NO2(g)+ O2 (g)。在一定條件下,將NO和O3通入絕熱恒容密閉容器中發生上述反應 ,正反應速率隨時間變化的示意圖(如圖9)所示。由圖可得出的正確說法是
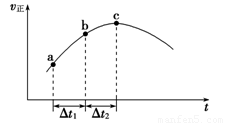
a.反應在c點達到平衡狀態
b.反應物濃度:b點小于c點
c.反應物的總能量低于生成物的總能量
d.Δt1=Δt2時,NO的轉化率:a~b段小于b~c段
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com