
工業上可以利用廢氣中的CO2為原料制取甲醇,其反應方程式為:CO2+3H2 CH3OH+H2O。請回答下列問題:
CH3OH+H2O。請回答下列問題:
(1)已知常溫常壓下下列反應的能量變化如下圖所示:
|
|
|
|

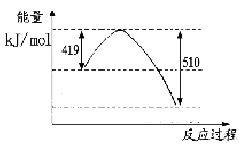 寫出由二氧化碳和氫氣制備甲醇的熱化學方程式__ _。
寫出由二氧化碳和氫氣制備甲醇的熱化學方程式__ _。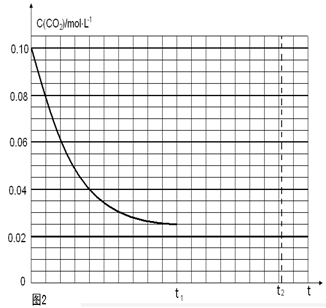
(1)3H2(g) + CO2(g)= CH3OH(l)+ H2O(l);ΔH=-50KJ/mol;<; 低溫;(2)A、D;
(3)CD;(4)0.01mol.L-1.min-1;畫圖
解析試題分析:(1)根據題意可得熱化學方程式:①CO(g)+H2O(l)=CO2(g)+H2(g) ΔH=-41KJ/mol; ②CO(g) +H2(g) =CH3OH(l)ΔH=-91KJ/mol; ②-①,整理可得3H2(g) + CO2(g)= CH3OH(l)+ H2O(l);ΔH=-50KJ/mol;由方程式可知,該反應是一個體系的混亂程度減小的反應。所以△S<0;由于該反應的正反應是放熱反應,所以反應在低溫情況下有利于該反應自發進行。(2)由于該反應的正反應是放熱反應,所以上述反應方程式的平衡常數K值變大,則平衡正向移動。由于K只與溫度有關,而與壓強、濃度等無關,所以只有溫度降低才可以滿足條件。當降溫時,V正、V逆都減小,V逆減小的多,V正>V逆,平衡正向移動,逆反應速率先減小后又略有增加。因此選項為A、D。(3)A.若反應達到平衡,則v正(H2)= 3v逆(CO2)。錯誤。B.由于二者消耗時是按照3:1的物質的量的關系消耗的,所以在開始加入的這兩種氣體只有按照某一確定的比例混合,達到平衡時才有關系:C(H2) = C(CO2)。因此不能作為判斷平衡的標志。錯誤。C.由于生成物有液態物質,若反應未達到平衡,則氣體的質量就會發生變化,氣體的密度也會發生改變。因此容器內氣體的密度不變,可以作為判斷平衡的標志。正確。D.該反應是反應前后氣體體積不等的反應,如果未達到平衡,則氣體的物質的量就會發生變化,則容器內氣體的壓強就會改變。因此容器內壓強不變可以作為判斷平衡的標志。正確。(4)反應的容器容積為2.0L,容器內氣體的密度增大了2.0g/L,則氣體的質量增加了2.0g/L×2.0L=4.0g.其中增加的CO2的質量為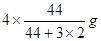 ;所以Δn(CO2)=" Δm÷M="
;所以Δn(CO2)=" Δm÷M="  =0.08mol,因此V(CO2)= Δc(CO2)÷Δt="(0.08mol" ÷2L)÷4min = 0.01mol/(L·min)。
=0.08mol,因此V(CO2)= Δc(CO2)÷Δt="(0.08mol" ÷2L)÷4min = 0.01mol/(L·min)。
由圖像可知:反應CO2(g)+3H2(g) CH3OH(l)+H2O(l)中起始時c(CO2)=0.10mol/L,平衡時c(CO2)=0.025mol/L,則Δc(CO2)=0.075mol/L,所以平衡時各物質的濃度為:c(H2)=0.075mol/L,該反應的平衡常數
CH3OH(l)+H2O(l)中起始時c(CO2)=0.10mol/L,平衡時c(CO2)=0.025mol/L,則Δc(CO2)=0.075mol/L,所以平衡時各物質的濃度為:c(H2)=0.075mol/L,該反應的平衡常數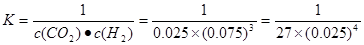 ;當保持其他條件不變,t1時將容器體積壓縮到1L,c(CO2)=0.05mol/L,c(H2)=0.15mol/L,平衡向右移動,設消耗c(CO2)=xmol/L,則消耗c(H2)=3xmol/L,平衡時各物質的濃度分別為c(CO2)="(0.05-x)mol/L" ,c(H2)="(0.15-3x)mol/L" ,平衡常數不變。即
;當保持其他條件不變,t1時將容器體積壓縮到1L,c(CO2)=0.05mol/L,c(H2)=0.15mol/L,平衡向右移動,設消耗c(CO2)=xmol/L,則消耗c(H2)=3xmol/L,平衡時各物質的濃度分別為c(CO2)="(0.05-x)mol/L" ,c(H2)="(0.15-3x)mol/L" ,平衡常數不變。即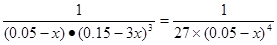 ,解得x= 0.025mol/L,則t2達到新的平衡時c(CO2)=0.025mol/L.故t1后c(CO2)隨時間t變化趨勢曲線為如圖所示。
,解得x= 0.025mol/L,則t2達到新的平衡時c(CO2)=0.025mol/L.故t1后c(CO2)隨時間t變化趨勢曲線為如圖所示。
考點:考查熱化學方程式的書寫、化學平衡狀態的判斷、反應的方向性、化學反應速率的計算、CO2濃度與時間圖像的表示。


 云南師大附小一線名師提優作業系列答案
云南師大附小一線名師提優作業系列答案科目:高中化學 來源: 題型:填空題
我國有豐富的天然氣資源。以天然氣為原料合成尿素的主要步驟如下圖所示(圖中某些轉化步驟及生成物未列出):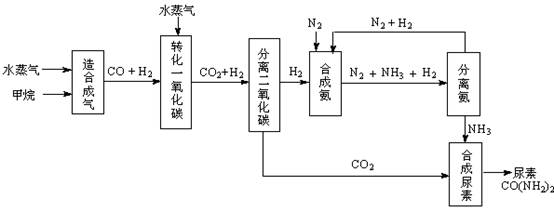
(1)“造合成氣”發生的熱化學方程式是CH4(g)+H2O(g) 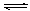 CO(g)+3H2(g);△H>0
CO(g)+3H2(g);△H>0
在恒溫恒容的條件下,欲提高CH4的反應速率和轉化率,下列措施可行的是 。
A、增大壓強 B、升高溫度 C、充入He氣 D、增大水蒸氣濃度
(2)“轉化一氧化碳”發生的方程式是H2O(g) +CO(g) 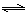 H2(g)+CO2(g),該反應平衡常數隨溫度的變化如下:
H2(g)+CO2(g),該反應平衡常數隨溫度的變化如下:
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在下列事實中,什么因素影響了化學反應的速率?
(1)黃鐵礦煅燒時要粉碎成細小的礦粒:________;
(2)熔化的KClO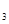 放出氣泡很慢,加入少量MnO
放出氣泡很慢,加入少量MnO 很快產生氣體:________;
很快產生氣體:________;
(3)同濃度、同體積的鹽酸中放入大小相同的鐵片和鎂片產生氣體有快有慢:________;
(4)同樣大小的石灰石分別在0.1mol/L的鹽酸和1mol/L的鹽酸中反應速率不同:________________;
(5)夏天的食品易霉變,冬天就不易發生類似現象:________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在一定條件下,反應x A+YB zC達到平衡:
zC達到平衡:
(1)若A、B、C均為氣體,則該反應的平衡常數表達式為_______________________;
(2)若A、B、C均為氣體,減壓后平衡向逆反應方向移動,則x、y、z間的關系是___________;
(3)已知C是氣體,且x+y=z,在增大壓強時,若平衡發生移動,則一定向________(填“正”或“逆”)反應方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(16分)Ⅰ.硅是信息產業、太陽能電池光電轉化的基礎材料。鋅還原四氯化硅是一種有著良好應用前景的制備硅的方法,該制備過程示意圖如下: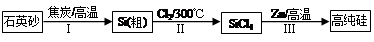
(1)焦炭在過程Ⅰ中做 劑。
(2)過程Ⅱ中Cl2用電解飽和食鹽水制備,制備Cl2的化學方程式為 。
(3)整過生產過程必須嚴格控制無水。
①SiCl4遇水劇烈水解生成SiO2和一種酸,反應方程式為 。
②干燥Cl2時從有利于充分干燥和操作安全的角度考慮,需將約90℃的潮濕氯氣先冷卻至12℃,然后再通入濃H2SO4中。冷卻的作用是 。
(4)Zn還原SiCl4的反應如下:
反應①:400℃~756℃,SiCl4(g)+2Zn(l) Si(S)+2ZnCl2(l) △H1<0
Si(S)+2ZnCl2(l) △H1<0
反應②:756℃~907℃,SiCl4(g)+2Zn(l) Si(S)+2ZnCl2(g) △H2<0
Si(S)+2ZnCl2(g) △H2<0
反應③:907℃~1410℃,SiCl4(g)+2Zn(g) Si(S)+2ZnCl2(g) △H3<0
Si(S)+2ZnCl2(g) △H3<0
i. 反應②的平衡常數表達式為 。
ii. 對于上述三個反應,下列說明合理的是 。
a.升高溫度會提高SiCl4的轉化率 b.還原過程需在無氧的氣氛中進行
c.增大壓強能提高反應速率 d.Na、Mg可以代替Zn還原SiCl4
(5)用硅制作太陽能電池時,為減弱光在硅表面的反射,可用化學腐蝕法在其表面形成粗糙的多孔硅層。腐蝕劑常用稀HNO3和HF的混合液。硅表面首先形成SiO2,最后轉化成H2SiF6。用化學方程式表示SiO2轉化為H2SiF6的過程 。
Ⅱ.(1)甲烷、氫氣、一氧化碳的燃燒熱分別為akJ·mol-1,bkJ·mol-1,ckJ·mol-1,工業上利用天燃氣和二氧化碳反應制備合成氣(CO、H2),其熱化學反應方程式為 。
(2)已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,三種難溶鹽的飽和溶液中,Ag+濃度大小的順序為 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(18分)碳、氮、硫是中學化學重要的非金屬元素,在工農業生產中有廣泛的應用。
(1)用于發射“天宮一號”的長征二號F火箭的燃料是液態偏二甲肼(CH3-NH-NH-CH3),氧化劑是液態四氧化二氮。二者在反應過程中放出大量能量,同時生成無毒、無污染的氣體。已知室溫下,1 g燃料完全燃燒釋放出的能量為42.5kJ,請寫出該反應的熱化學方程式________________________________________。
(2)298 K時,在2L的密閉容器中,發生可逆反應:2NO2(g) N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物質的量濃度隨時間變化如圖。達平衡時, N2O4的濃度為NO2的2倍,回答下列問題。
N2O4(g) ΔH=-a kJ·mol-1 (a>0) 。N2O4的物質的量濃度隨時間變化如圖。達平衡時, N2O4的濃度為NO2的2倍,回答下列問題。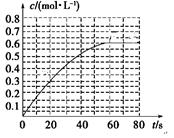
①298k時,該反應的平衡常數為________ L ·mol-1。
②下列事實能判斷該反應處于平衡狀態的是
a.混合氣體的密度保持不變
b.混合氣體的顏色不再變化
c. V(N2O4)正=2V(NO2)逆
③若反應在398K進行,某時刻測得n(NO2)="0.6" mol n(N2O4)=1.2mol,則此時
V(正) V(逆)(填“>”“<”或“=”)。
(3)NH4HSO4在分析試劑、醫藥、電子工業中用途廣泛。現向100 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH與NaOH溶液體積的關系曲線如圖所示。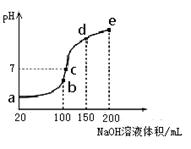
試分析圖中a、b、c、d、e五個點,
①水的電離程度最大的是__________;
②其溶液中c(OH-)的數值最接近NH3·H2O的電離常
數K數值的是 ;
③在c點,溶液中各離子濃度由大到小的排列順序
是__________。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(16分)高鐵酸鈉(Na2FeO4)具有很強的氧化性,廣泛應用于凈水、電池工業等領域。以粗FeO(含有CuO、Al2O3和SiO2等雜質)制備高鐵酸鈉的生產流程如下,回答下列問題: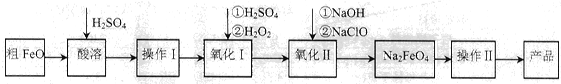
已知:NaClO不穩定,受熱易分解。
(1)粗FeO酸溶過程中通入水蒸氣(高溫),其目的是__________________________。
(2)操作I目的是得到高純度FeSO4溶液,則氧化I中反應的離子方程式為_________。
(3)本工藝中需要高濃度NaClO溶液,可用Cl2與NaOH溶液反應制備
①Cl2與NaOH溶液反應的離子方程式為_________________。
②在不同溫度下進行該反應,反應相同一段時間后,測得生成NaClO濃度如下:
| 溫度/℃ | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| NaClO濃度/mol·L-1 | 4.6 | 5.2 | 5.4 | 5.5 | 4.5 | 3.5 | 2 |

查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(6分)把6 molA氣體和5 molB氣體混合放入4L恒容密閉容器中。在一定條件下發生反應:3A(g)+B(g) 2C(g)+xD(g),經過5 min后達到化學平衡,此時生成2 molC。又知在此時D的平均速率為0.15 mol·L-1·min-1。
2C(g)+xD(g),經過5 min后達到化學平衡,此時生成2 molC。又知在此時D的平均速率為0.15 mol·L-1·min-1。
求:(1)平衡時A的物質的量濃度; (2) B的轉化率;(3) x的值。(要求寫出計算過程)
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
甲醇可作為燃料電池的原料。以CH4和H2O為原料,通過下列反應來制備甲醇。
I:CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.0kJ?molˉ1
CO(g)+3H2(g) △H=+206.0kJ?molˉ1
II:CO(g)+2H2(g) CH3OH(g) △H=-129.0kJ?molˉ1
CH3OH(g) △H=-129.0kJ?molˉ1
(1)CH4(g)與H2O(g)反應生成CH3OH(g)和H2(g)的熱化學方程式為 。
(2)將1.0mol CH4和1.0mol H2O(g)通入容積為100 L的反應室,在一定條件下發生反應I,測得在一定的壓強下CH4的轉化率與溫度的關系如圖。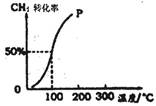
①假設100℃時達到平衡所需構時間為5min,則用H2表示該反應的平均反應速率為 。
②1000C時反應I的平衡常數為 。
(3)在壓強為0.1 MPa、溫度為300℃條件下,將a molCO與2a mol H2的混合氣體在催化劑作用下發生反應II生成甲醇,平衡后將容器舶容積壓縮到原來的1/2,其他條件不變,對平衡體系產生的影響是 (填字母序號)。
| A.平衡常數K增大 | B.正反應速率加快,逆反應速率減慢 |
| C.CH3OH的物質的量增加 | D.重新平衡c(H2)/c(CH3OH)減小 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com