
 CH3OH(g)+H2O(g) 。
CH3OH(g)+H2O(g) 。
 CH3OH (g) ΔH=-90.8 kJ·mol-1
CH3OH (g) ΔH=-90.8 kJ·mol-1 CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1 CO2 (g)+H2(g) ΔH=-41.3 kJ·mol-1
CO2 (g)+H2(g) ΔH=-41.3 kJ·mol-1| A.高溫高壓 |
| B.加入催化劑 |
| C.減少CO2的濃度 |
| D.增加CO的濃度E.分離出二甲醚 |
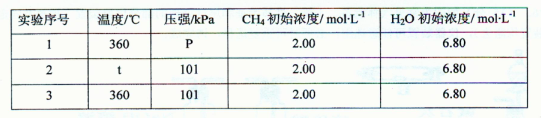
 CH3OCH3(g)+H2O(g)在某溫度下的平衡常數K = 400。此溫度下,在密閉容器中加入CH3OH,反應到某時刻測得各組分的濃度如下:
CH3OCH3(g)+H2O(g)在某溫度下的平衡常數K = 400。此溫度下,在密閉容器中加入CH3OH,反應到某時刻測得各組分的濃度如下:| 物質 | CH3OH | CH3OCH3 | H2O |
| c / mol·L-1 | 0.44 | 0.60 | 0.60 |

 CH3OCH3(g)+CO2 (g) ΔH =-246.4 kJ·mol-1(3分)
CH3OCH3(g)+CO2 (g) ΔH =-246.4 kJ·mol-1(3分)


 CH3OCH3(g)+CO2 (g) ΔH =-246.4 kJ·mol-1
CH3OCH3(g)+CO2 (g) ΔH =-246.4 kJ·mol-1 CH3OCH3(g)+H2O(g)的
CH3OCH3(g)+H2O(g)的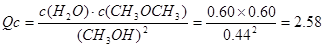 <K=400,所以反應向正反應方向進行,即v (正)>v (逆)
<K=400,所以反應向正反應方向進行,即v (正)>v (逆)

科目:高中化學 來源:不詳 題型:單選題
| A.反應:2CO(g)+2NO(g) |
| B.0.1mol/L NH4C1溶液加蒸餾水稀釋,溶液的pH不斷減小 |
| C.為保護浸入海水中的鋼閘門,可在閘門表面鑲上銅錠 |
D.反應:2A(g)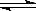 B(g)+2C(g),增大壓強反應速率加快,A的轉化率減小 B(g)+2C(g),增大壓強反應速率加快,A的轉化率減小 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 。H2應從電解池的________ (填電極名稱)通入;其中b電極的電極反應方程式為________。
。H2應從電解池的________ (填電極名稱)通入;其中b電極的電極反應方程式為________。
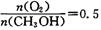 時,制備反應分兩步進行,其中一步是
時,制備反應分兩步進行,其中一步是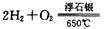
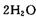 ,則另一步是____________ (寫化學方程式)。
,則另一步是____________ (寫化學方程式)。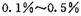 的HCHO可用于殺菌消毒,其原因是________。
的HCHO可用于殺菌消毒,其原因是________。查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 還含有碳氫化合物等污染物,下圖是汽車尾氣轉化研究的示意圖:表示的是Pt/Al2O3/Ba表面吸附與解吸作用的機理,氮氧
還含有碳氫化合物等污染物,下圖是汽車尾氣轉化研究的示意圖:表示的是Pt/Al2O3/Ba表面吸附與解吸作用的機理,氮氧 化物是NO2,碳氫化合物是CxHy
化物是NO2,碳氫化合物是CxHy ,寫出兩者反應的化學方程式: ,Pt/Al2O3/Ba的作用是 ;
,寫出兩者反應的化學方程式: ,Pt/Al2O3/Ba的作用是 ;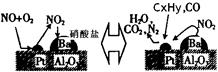
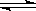 2NO(g) K1=1×10-30 ㈠
2NO(g) K1=1×10-30 ㈠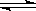 2H2O(g) K2=2×1081 ㈡
2H2O(g) K2=2×1081 ㈡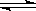 2CO(g)+O2(g) K3=4×10-92 ㈢
2CO(g)+O2(g) K3=4×10-92 ㈢ ①常溫下,反應2H2O(g) 2H2(g)
①常溫下,反應2H2O(g) 2H2(g) +O2(g) 平衡常數K= ;
+O2(g) 平衡常數K= ;A. 常溫下,NO,H2O,CO2三種化合物分解放出氧氣的傾向大小順序:NO>H2O>CO2 常溫下,NO,H2O,CO2三種化合物分解放出氧氣的傾向大小順序:NO>H2O>CO2 |
| B.若升高溫度,反應㈢的平衡常數K3將增大 |
| C.若只增加壓強,且反應物、生成物狀態不變,反應㈠平衡不發生移動,平衡常數不變;反應㈡平衡朝正向移動,平衡常數增大 |
| D.若增加汽車發動機空氣的進氣量,可同時減少氮氧化物和一氧化碳的排放 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 CO(g)+3H2(g);△H=+206.lkJ·mol-l。
CO(g)+3H2(g);△H=+206.lkJ·mol-l。
| A.v(正)>v(逆) | B.v(正)<v(逆) |
| C.v(正)=v(逆) | D.無法判斷 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.明礬凈水的原理是Al3+水解產生Al(OH)3膠體,Al(OH)3膠體能吸附水中的懸浮雜質,并使之沉降 |
| B.摩爾鹽的制備原理為:6H2O+FeSO4+(NH4)2SO4=(NH4)2Fe(SO4)?6H2O,反應之所以能進行的原因是(NH4)2Fe(SO4)?6H2O溶解度最小 |
| C.鍍鋅鐵皮在酸中溶解,當鍍層反應完全時,產生氫氣的速率會突然減慢 |
| D.將火柴頭直接浸入品紅溶液中,可以檢驗火柴頭中是否含有硫元素 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
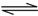 2NH3(g)的△H= 。
2NH3(g)的△H= 。 積分數為 。
積分數為 。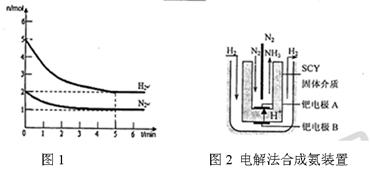
 內外
內外 表面上的金屬鈀多品薄膜做電極,實現了高轉化率的電解法合成氨(裝置如圖2)。鈀電極A
表面上的金屬鈀多品薄膜做電極,實現了高轉化率的電解法合成氨(裝置如圖2)。鈀電極A 上發生的電極反應式是 。
上發生的電極反應式是 。 查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 cC(g)(△H<0)在等容條件下進行。改變其他反應條件,在I、II、III階段體系中各物質濃度隨時間變化的曲線如下圖所示:
cC(g)(△H<0)在等容條件下進行。改變其他反應條件,在I、II、III階段體系中各物質濃度隨時間變化的曲線如下圖所示: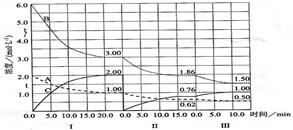
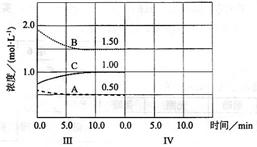
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com