
【題目】工業上,以鈦鐵礦為原料制備二氧化鈦的工藝流程如下圖所示。鈦鐵礦主要成分為鈦酸亞鐵(FeTiO3),其中一部分Fe2+在風化過程中會轉化為+3價。

已知:TiO(OH)2(即H2TiO3)為兩性氫氧化物
(1)步驟②中,發生反應的主要離子方程式為______________。
(2)步驟③中,實現混合物的分離是利用物質的____________(填字母序號)。
A.熔沸點差異 B.溶解性差異 C.氧化性、還原性差異
(3)步驟②、③、④中,均需用到的操作是____________(填操作名稱)。
(4)請結合化學用語用化學平衡理論解釋步驟④中將TiO2+轉化為H2TiO3的原理:__________________________。
(5)上述工藝流程中可以循環利用的物質是____________。
(6)研究發現,可以用石墨作陽極、鐵網作陰極、熔觸CaF2-CaO作電解質,利用如圖所示裝置獲得金屬鈣,并以鈣為還原劑,還原二氧化鈦制備金屬鈦。

①寫出陽極所發生反應的電極反應式_________________________。
②在制備金屬Ti前后,CaO的質量將______(填“增大”、“不變”或“減小”)
【答案】 2Fe3++Fe=3Fe2+ B 過濾 溶液中存在平衡:TiO2++2H2O![]() H2TiO3+2H+,當加入熱水將溶液稀釋、升溫后,平衡正向移動,生成H2TiO3。 H2SO4或硫酸 2O2--4e-=O2↑或C+O2--2e-=CO↑ 不變
H2TiO3+2H+,當加入熱水將溶液稀釋、升溫后,平衡正向移動,生成H2TiO3。 H2SO4或硫酸 2O2--4e-=O2↑或C+O2--2e-=CO↑ 不變
【解析】(1)步驟②中,用鐵粉將Fe3+轉化為Fe2+的反應的離子方程式為:2Fe3++Fe=3Fe2+;(2)步驟③冷卻結晶得到硫酸亞鐵晶體,利用的是物質溶解度的不同,通過冷卻熱飽和溶液得到,故答案為:B;(3)②③④步驟的操作過程中都得到沉淀或晶體,所以需要過濾得到固體和溶液;(4)④中使用熱水的目的是促進TiO2+水解生成H2TiO3,分離出固體加熱得到TiO2;這是由于溶液中存在平衡:TiO2++2H2O![]() H2TiO3+2H+,當加入熱水將溶液稀釋、升溫后,平衡正向移動,生成H2TiO3。(5)根據流程圖可知廢液中含有硫酸,所以循環利用的物質是硫酸;(6)①用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,陽極發生氧化反應,陰極析出鈣金屬發生還原反應,陽極圖示產物可可知,陽極生成二氧化碳氣體,是電解質中的氧離子失電子生成氧氣,氧氣和陽極石墨反應生成的二氧化碳,所以電極反應為2O2--4e-=O2↑或C+O2--2e-=CO↑;②制備TiO2時,在電解槽發生如下反應:2CaO=2Ca+O2↑,2Ca+TiO2=Ti+2CaO,由此可見,CaO的量不變。
H2TiO3+2H+,當加入熱水將溶液稀釋、升溫后,平衡正向移動,生成H2TiO3。(5)根據流程圖可知廢液中含有硫酸,所以循環利用的物質是硫酸;(6)①用石墨作陽極、鈦網作陰極、熔融CaF2-CaO作電解質,陽極發生氧化反應,陰極析出鈣金屬發生還原反應,陽極圖示產物可可知,陽極生成二氧化碳氣體,是電解質中的氧離子失電子生成氧氣,氧氣和陽極石墨反應生成的二氧化碳,所以電極反應為2O2--4e-=O2↑或C+O2--2e-=CO↑;②制備TiO2時,在電解槽發生如下反應:2CaO=2Ca+O2↑,2Ca+TiO2=Ti+2CaO,由此可見,CaO的量不變。


科目:高中化學 來源: 題型:
【題目】以淀粉為主要原料合成一種具有果香味有機物C和高分子化合物E的合成路線如下圖所示。
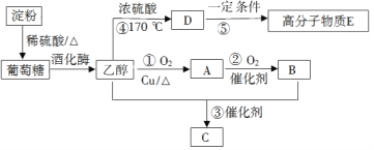
請回答下列問題:
(1)寫出C的結構簡式:__________________,A分子內含有的官能團是_______(填名稱)。
(2)寫出下列反應的反應類型:①________________,③________________。
(3)寫出下列反應的化學方程式:①________________________;⑤________________________。
(4)某同學欲用下圖裝置制備物質C,將試管B中的物質C分離出來,用到的主要玻璃儀器有:燒杯、________,插入試管B的導管接有一個球狀物,其作用為________________________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能說明非金屬性C1>I的是
A. C12+2I-=2C1-+I2 B. 穩定性:HC1>HI
C. 酸性:HC1O4>HIO4 D. 酸性:HC1O3>HIO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】原子序數依次增大的短周期元素A、B、C、D分別位于不同的主族,m、p、n分別是元素A、B、C的單質, D的單質可與熱水發生置換反應;x、y、z是由A、B、C組成的二元化合物,其中y、z是氣體,且z可用于配制碳酸飲料。它們之間有如下轉化關系,

下列說法正確的是
A. D的單質起火燃燒時可用z作滅火劑
B. 元素的非金屬性:C >A >B
C. B、C與A形成化合物的沸點:C >B
D. 原子半徑:D >B >C >A
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列變化過程中,屬于放熱反應的是( )
① 煅燒石灰石制生石灰 ② 木炭取暖③ 固體 NaOH溶于水 ④ 酸與堿的中和反應⑤ 鋁熱反應⑥ NH4Cl晶體與Ba(OH)2·8H2O混合攪拌
A. ① ③ ⑥B. ② ④ ⑤C. ② ③ ④D. ② ④ ⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于化學鍵的相關敘述正確的是
A. 共價鍵只存在于共價化合物和非金屬單質中
B. 離子化合物中一定有離子鍵,也可能存在共價鍵
C. 化學鍵的斷裂或形成一定伴隨著化學反應的發生
D. 熔融狀態或水溶液可導電的化合物一定是離子化合物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氣態烴X在標準狀態下的密度為1.16gL-1,D能發生銀鏡反應,E為聚氯乙烯,有關物質的轉化關系如下:請回答下列問題:

(1)反應②的反應類型為_____________,一定條件下X能發生類似于⑤的反應,
所得高分子化合物的結構簡式為_________________。
(2)A與F在催化劑作用下直接生成G的化學方程式為___________________________。
(3)下列說法正確的是_________。
A.A、B、E均能使酸性高錳酸鉀溶液褪色
B.G的同分異構體中能與碳酸氫鈉反應生成CO2氣體的物質有4種
C.F、G都能與NaOH溶液反應,且都生成鈉鹽
D.X先后與F、H2反應也可以制得G
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組同學用下圖所示裝置制取氨氣并驗證氨氣的性質。

請回答:
(1)制取氨氣的化學方程式是 ___________________________________。
(2)收集氨氣的方法是_____________________(填“向上排空氣法”或“向下排空氣法”)。
(3)將濕潤的紅色石蕊試紙靠近集滿氨氣的試管口,試紙變藍,說明氨氣溶于水呈 _______________(填“酸”或“堿性”)。
(4)實驗中加入5.35g的NH4Cl和足量的Ca(OH)2,充分反應,理論上收集到氨氣的體積為 ____________________ L(標準狀況)。
(5)已知生石灰遇水生成Ca(OH)2且放出大量的熱,實驗室也可以利用往生石灰中滴入濃氨水,快速制氨氣。利用此方法制氨氣選用的氣體發生裝置是 _________(填“a”或“b”)。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com