
【題目】下列研究目的和示意圖相符的是( )
① | ② | ③ | ④ | |
研 | 固定容積的密閉容器中,壓強對反應: | 固定容積的密閉容器中,溫度對反應: | 固定容積的密閉容器中,增大CO2濃度,對已達平衡的反應: | 等質量Na、K 分別與足量水反應 |
示 |
|
|
|
|
A. ①B. ②C. ③D. ④
 名師伴你成長課時同步學練測系列答案
名師伴你成長課時同步學練測系列答案科目:高中化學 來源: 題型:
【題目】溫度為T1時,在三個容積均為1L的恒容密閉容器中僅發生反應:2NO2(g)![]() 2NO(g)+O2(g)(正反應吸熱)。實驗測得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆為速率常數,受溫度影響。下列說法正確的是( )
2NO(g)+O2(g)(正反應吸熱)。實驗測得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆為速率常數,受溫度影響。下列說法正確的是( )
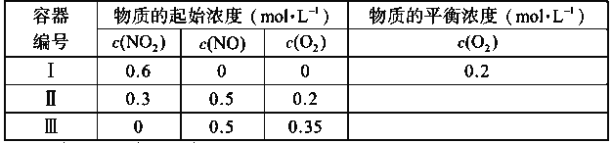
A.達平衡時,容器Ⅰ與容器Ⅱ中的總壓強之比為4∶5
B.達平衡時,容器Ⅱ中![]() 比容器Ⅰ中的大
比容器Ⅰ中的大
C.達平衡時,容器Ⅲ中NO的體積分數小于50%
D.當溫度改變為T2時,若k正=k逆,則T2>T1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】小王要制備純凈的二氧化碳氣體,可供選用的儀器如圖所示。可供選用的藥品如下:①石灰石②澄清石灰水③稀硫酸④濃硫酸⑤鹽酸溶液⑥燒堿溶液⑦蒸餾水。下列裝置連接順序及組合最恰當的是( )

A. A(①⑤)、B(④)、C(⑦)、DB. A(①③)、B(④)、C(⑦)、D
C. A(①⑤)、B(⑦)、C(④)、DD. A(①⑤)、B(⑥)、C(④)、D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】含氯消毒劑有多種,二氧化氯可用于自來水消毒,84消毒液用于家庭、賓館的消毒。
I.實驗室可用亞氯酸鈉固體與應制備ClO2:2NaClO2+Cl2=2ClO2+2NaCl,裝置如圖所示:
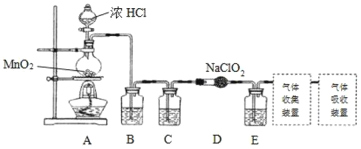
(1)裝置A中,盛裝濃鹽酸的儀器名稱為___,開始反應后,圓底燒瓶內發生的反應的離子反應方程式為:__。
(2)已知常溫常壓下,ClO2和Cl2是氣體,在不同溶劑中溶解性如表所示:B、C、E裝置中的試劑依次是___(填編號)
ClO2 | Cl2 | |
水 | 極易溶于水 | 溶 |
CCl4 | 難溶 | 易溶 |
a.濃硫酸 b.飽和食鹽水 c.NaOH溶液 d.CCl4
(3)使用ClO2在給自來水消毒的過程中會產生有害的副產物亞氯酸根(ClO2-),可用Fe2+將其去除。已知ClO2-與Fe2+在pH=5~7的條件下能快速反應,最終形成紅褐色沉淀,而ClO2-則被還原成Cl-。Fe2+消除ClO2-的離子方程式為__。
II.某同學在家中自制出與“84消毒液”成分(NaClO和水)相同的消毒液。主要器材有6V變壓器、兩支木桿鉛筆、廢純凈水瓶、食鹽、衛生紙、絕緣膠布、小刀等。
(4)實驗過程:向一個廢棄的純凈水瓶中灌入大半瓶自來水,并加入3調味匙食鹽,用衛生紙將用鉛筆做成的電極包好,并插入純凈水瓶中,使電極恰好卡在瓶口,裝置如圖,接通電源后,可以看到一側電極無明顯現象,另一側電極有細小的氣泡產生,請寫出該電極反應式為:___;持續通電約3小時后,發現原先無明顯現象的電極附近也開始產生一定量的細小氣泡,此電極此時的電極反應式___。看到該現象后停止通電。

(5)用該方法制備消毒液的總化學方程式是:___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 乙醇燃燒是生成物總能量高于反應物總能量的反應
B. 稀溶液中,H+(aq)+OH﹣(aq)=H2O(l)△H=﹣57.3 kJ/mol可表示稀硫酸與稀Ba(OH)2溶液反應的中和熱為△H=﹣57.3 kJ/mol
C. 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=﹣QkJ/mol可以表示H2S的燃燒熱
D. 高溫下,某反應達到平衡,平衡常數為K=![]() ,恒容時,溫度升高,H2濃度減小,故該反應的焓變為正值
,恒容時,溫度升高,H2濃度減小,故該反應的焓變為正值
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列熱化學方程式或敘述正確的是
A. 1 mol液態肼在足量氧氣中完全燃燒生成水蒸氣,放出642 kJ的熱量:N2H4(l)+O2(g) ===N2(g)+2H2O(g) ΔH=+642 kJ·mol-1
B. 12 g石墨轉化為CO時,放出110.5 kJ的熱量:2C(石墨,s)+O2(g) ===2CO(g) ΔH=-110.5 kJ·mol-1
C. 已知:H2(g)+ ![]() O2(g) ===H2O(l) ΔH=-286 kJ·mol-1,則:2H2O(l) ===2H2(g)+O2(g)的ΔH=+572 kJ·mol-1
O2(g) ===H2O(l) ΔH=-286 kJ·mol-1,則:2H2O(l) ===2H2(g)+O2(g)的ΔH=+572 kJ·mol-1
D. 已知N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,則在一定條件下向密閉容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反應放出46.2 kJ的熱量
2NH3(g) ΔH=-92.4 kJ·mol-1,則在一定條件下向密閉容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反應放出46.2 kJ的熱量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A(g)+B(g)![]() C(g)+D(g)反應的平衡常數和溫度的關系如下:
C(g)+D(g)反應的平衡常數和溫度的關系如下:
|溫度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常數 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列問題:
(1)該反應的平衡常數表達式K=____________,△H____0(填“<”“ >”“ =”);
(2)830℃時,向一個5 L的密閉容器中充入0.20mol的A和0.80mol的B,如反應初始6s內A的平均反應速率v(A)=0.003 mol·L-1·s-1。則6s時c(A)=_____mol·L-1, C的物質的量為______mol;若反應經一段時間后,達到平衡時A的轉化率為_____,如果這時向該密閉容器中再充入1 mol氬氣,平衡時A的轉化率為_________;
(3)判斷該反應是否達到平衡的依據為______(填正確選項前的字母):
a.壓強不隨時間改變 b.氣體的密度不隨時間改變
c.c(A)不隨時間改變 d.單位時間里生成C和D的物質的量相等
(4)1200℃時反應C(g)+D(g)![]() A(g)+B(g)的平衡常數的值為_____________。
A(g)+B(g)的平衡常數的值為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于熱化學反應的描述中正確的是
A.HCl和NaOH反應的中和熱ΔH=57.3kJ/mol,則H2SO4和Ba(OH)2反應的中和熱ΔH=2×(57.3)kJ/mol
B.CO(g)的燃燒熱是ΔH=283.0kJ/mol,則2CO(g)+O2(g)=2CO2(g)反應的ΔH=(2×283.0)kJ/mol
C.需要加熱才能發生的反應一定是吸熱反應
D.1mol甲烷燃燒生成氣態水和二氧化碳所放出的熱量是甲烷的燃燒熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】采用如圖裝置制取一定量的飽和氯水,并進行氯水的性質實驗。
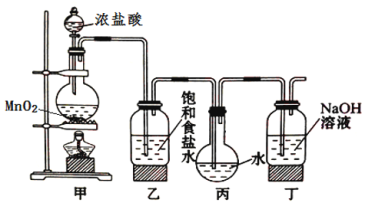
(1)在裝入藥品前應進行的操作____________________________________________。
(2)寫出丁裝置中發生反應的離子方程式:_______________________。
(3)用制得的飽和氯水分別進行下列實驗:
①滴入碳酸鈉溶液中,有氣體生成,說明氯水中發生反應的粒子是___________;
②滴到藍色石蕊試紙上的現象:_________________________________________。
(4)久置的氯水漂白效果明顯不足或消失,用化學方程式表示:_________________。
(5)將制得的飽和氯水慢慢滴入含有酚酞的NaOH稀溶液中,當滴到一定量時,紅色突然褪去。產生上述現象的原因可能有兩種(簡要文字說明):
①__________________________________________________________________;
②__________________________________________________________________。
用實驗證明紅色褪去的原因是①或者②的實驗方法是:___________。
(6)科學家提出,使用氯氣對自來水消毒時,氯氣會與水里的有機物反應,生成的有機氯化物可能對人體有害,現已開始使用新的自來水消毒劑,如_________________(舉兩例,寫化學式)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com