運用化學反應原理研究氮、硫、氯等單質及其化合物的反應有重要的意義.
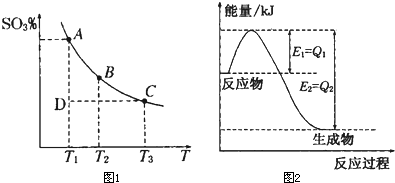
(1)放熱反應2SO
2(g)+O
2(g)=2SO
3(g)是硫酸工業上的重要反應,在體積不變的條件下,下列措施有利于提高SO
2平衡轉化率的有
(填字母).
A、升高溫度 B、降低溫度 C、減小壓強 D、加入催化劑 E.移出氧氣
(2)氮是大氣中含量最多的一種元素,氮及其化合物在工農業生產、生活中有著重要應用.用CH
4將氮氧化物(用NO
x表示)催化還原為N
2可以消除氮氧化物帶來的污染,該反應的化學方程式為
.現有1L由NO、NO
2組成的混合氣體,若將其還原為N
2、需同溫同壓下0.4LCH
4,則混合氣體中NO、NO
2的物質的量之比為
.
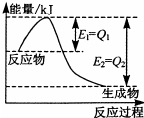
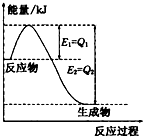
(3)如圖是一定的溫度和壓強下,N
2和H
2反應生成1mol NH
3過程中的能量變化圖,請寫出工業合成氨的熱化學方程式
.(△H的數值用含字母Q
1、Q
2的代數式表示).
(4)在25℃下,將xmol/L的氨水與y mol/L的鹽酸等體積混合,反應后溶液顯中性,則c(NH
4+ )
c(Cl
-)(填“>”、“<”或“=”);用含x和y的代數式表示該混合溶液中氨水的電離平衡常
.
(5)已知:25℃時,K
sp(AgCl)=1.8×10
-10、K
sp(AgBr)=4.9×10
-13.現在向0.001mol/L KBr和0.01mol/L KCl混合溶液中滴加0.1mol/L AgNO
3溶液(反應過程中溶液體積變化忽略不計),當出現AgCl沉淀時.c(Br
-)=
(保留兩位有效數字).

 運用化學反應原理研究氮、硫、氯等單質及其化合物的反應有重要的意義.
運用化學反應原理研究氮、硫、氯等單質及其化合物的反應有重要的意義.

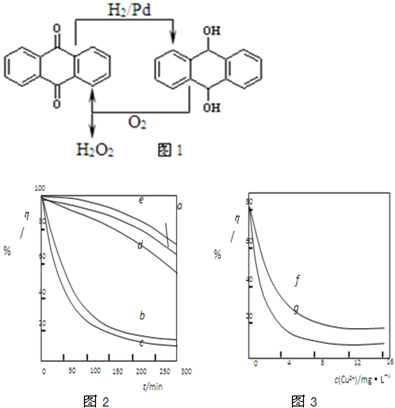
 運用化學反應原理研究氮、氯、碘等單質及其化合物的反應有重要意義.
運用化學反應原理研究氮、氯、碘等單質及其化合物的反應有重要意義.