
蛇紋石是一種含水的富鎂硅酸鹽礦物的總稱,可以看作由MgO、Fe2O3、Al2O3、SiO2組成。實驗室以蛇紋石為原料制取水合堿式碳酸鎂,已知:
氫氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
開始沉淀的pH | 1.5 | 3.3 | 9.4 |
完全沉淀的pH | 3.7 | 5.2 | 11.0 |
實驗步驟如下:
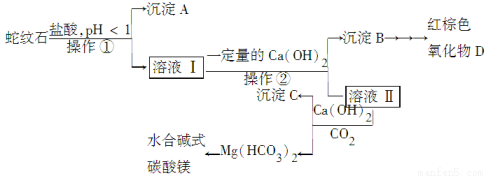
(1)實驗室完成操作①所用到的玻璃儀器有:________。
(2)操作②中應控制溶液pH的合理范圍是________(填序號)。
A.小于1.5 B.1.5~3.3 C.7~8 D.大小9.4
(3)檢驗溶液Ⅱ中是否含有Fe3+的操作與結論是______________________。
(4)從沉淀混合物B中制取D,應加入一種試劑進行分離,其反應的離子方程式為________,再進行________、洗滌、________(依次填寫實驗操作名稱)。
(1)玻璃棒、漏斗、燒杯
(2)C
(3)取少量溶液Ⅱ于試管中,加入KSCN溶液,若無明顯現象,說明溶液Ⅱ不含Fe3+;若溶液變紅色,說明溶液Ⅱ含有Fe3+
(4)OH-+Al(OH)3=AlO2— +2H2O 過濾、加熱或灼燒
【解析】 (1)操作①是過濾,所以需要的玻璃儀器是玻璃棒、漏斗、燒杯。
(2)操作②的目的是沉淀鐵離子和鋁離子,但不能沉淀鎂離子,所以根據沉淀的pH可知,應控制溶液pH的合理范圍是5.2~9.4,答案選C。
(3)檢驗鐵離子的試劑是KSCN溶液,即取少量溶液Ⅱ于試管中,加入KSCN溶液,若無明顯現象,說明溶液Ⅱ不含Fe3+;若溶液變紅色,說明溶液Ⅱ含有Fe3+。
(4)B中沉淀是氫氧化鋁和氫氧化鐵,由于氫氧化鋁是兩性氫氧化物,所以得到氫氧化鐵的方法是加入氫氧化鈉溶液,過濾即可,反應的離子方程式是OH-+Al(OH)3=AlO+2H2O;由于在氫氧化鐵表面有吸附的離子,所以在過濾之后還需要洗滌,最后加熱或灼燒。


科目:高中化學 來源:2014年高考化學指導沖關 第3練化學反應與能量變化練習卷(解析版) 題型:選擇題
化學與社會、環境等密切相關。下列說法錯誤的是( )
A.“低碳經濟”是指減少對化石燃料的依賴,達到低污染、低排放的模式
B.“低碳生活”倡導生活中耗用能量盡量減少,從而減少CO2的排放
C.所有垃圾都可以采用露天焚燒或深埋的方法處理
D.“靜電除塵”、“燃煤固硫”、“汽車尾氣催化凈化”都能提高空氣質量
查看答案和解析>>
科目:高中化學 來源:2014年高考化學指導沖關 第14練有機物的組成、結構和性質練習卷(解析版) 題型:選擇題
合成香料香豆素過程的中間產物的結構簡式如下,關于該物質的說法不正確的是( )
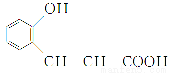
A.分子式為C9H8O3
B.有兩種含氧官能團
C.1 mol該物質最多能與5 mol H2發生加成反應
D.該物質在一定條件下可發生酯化反應
查看答案和解析>>
科目:高中化學 來源:2014年高考化學指導沖關 第13練物質結構與性質練習卷(解析版) 題型:選擇題
PH3一種無色劇毒氣體,其分子結構和NH3相似,但PH鍵鍵能比NH鍵鍵能低。下列判斷錯誤的是( )
A.PH3分子呈三角錐形
B.PH3分子是極性分子
C.PH3沸點低于NH3沸點,因為PH鍵鍵能低
D.PH3分子穩定性低于NH3分子,因為NH鍵鍵能高
查看答案和解析>>
科目:高中化學 來源:2014年高考化學指導沖關 第12練物質制備方案的設計與評價練習卷(解析版) 題型:實驗題
四氯化鈦是無色液體,沸點為136℃。它極易水解,遇空氣中的水蒸氣即產生“白煙”(TiCl4+H2O=TiOCl2+2HCl↑)。在650~850℃下,將氯氣通過二氧化鈦和炭粉的混合物可得到四氯化鈦和一種有毒氣體。如圖是某科研小組制備TiCl4的反應裝置,其主要操作步驟如下:
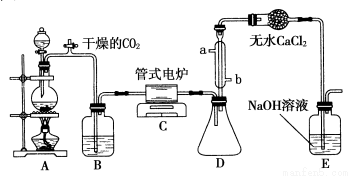
①連接好整套裝置,在通Cl2前先通入CO2氣體并持續一段時間;
②當錐形瓶中TiCl4的量不再增加時,停止加熱,從側管中改通CO2氣體直到電爐中的瓷管冷卻為止;
③將TiO2、炭粉混合均勻后,裝入管式電爐中;
④將電爐升溫到800℃,一段時間后改通Cl2,同時在冷凝管中通冷凝水。
試回答下列問題:
(1)正確的操作順序為(填序號)________。
(2)C裝置中的反應的化學方程式為_________________________________。
(3)B中的試劑為________;其作用是__________________________。
(4)D裝置的作用是_________________________________________。
(5)干燥管中無水CaCl2的作用是_____________________________。
(6)從環境保護的角度,提出一個優化方案:__________________________。
查看答案和解析>>
科目:高中化學 來源:2014年高考化學指導沖關 第11練化學實驗基礎知識練習卷(解析版) 題型:選擇題
某未知溶液中已檢驗出含大量的Fe2+、SO42— ,且pH=1。欲檢驗此溶液中是否大量存在以下離子:①NH4+、② SiO32—、③Mg2+、④Cl-、⑤Ca2+、⑥ClO-,其中不需要檢驗就可以否定的離子是( )
A.①③⑤ B.②⑤⑥ C.①②⑥ D.③④⑥
查看答案和解析>>
科目:高中化學 來源:2014年高考化學指導沖關 第10練常見有機化合物及其應用練習卷(解析版) 題型:選擇題
酯類物質廣泛存在于香蕉、梨等水果中。某實驗小組先從梨中分離出一種酯,然后將分離出的酯水解,得到乙酸和另一種化學式為C6H14O的物質。對于此過程,以下分析中不正確的是( )
A.C6H14O分子含有羥基
B.C6H14O可與金屬鈉發生反應
C.實驗小組分離出的酯可表示為CH3COOC6H13
D.不需要催化劑,這種酯在水中加熱即可大量分解
查看答案和解析>>
科目:高中化學 來源:2014年高考化學指導沖關 第10練常見有機化合物及其應用練習卷(解析版) 題型:選擇題
下列說法正確的是( )
A.食用白糖的主要成分是蔗糖
B.小蘇打的主要成分是碳酸鈉
C.煤氣的主要成分是丁烷
D.植物油的主要成分是高級脂肪酸
查看答案和解析>>
科目:高中化學 來源:2014年高考化學二輪復習專題滾動練4 化學實驗練習卷(解析版) 題型:填空題
碳酸鈣常用作牙膏的摩擦劑。某同學設計了一種制備碳酸鈣的方案,其流程圖如下:(所用石灰石含有雜質SiO2)

回答下列問題:
(1)充分煅燒110噸石灰石得到固體66噸。標準狀況下生成二氧化碳的體積為______________L,石灰石中碳酸鈣的質量分數為______________%。
(2)假設第①步反應完全進行,則第②步反應過濾后得到的不溶性濾渣的成分為________________________。
(3)第③步反應一般不采用通入CO2的主要原因是______________________,
相應的離子方程式為_____________________________________。
(4)CaCO3是一種難溶物質,25℃時其Ksp=2.8×10-9。現將等體積的CaCl2溶液與Na2CO3溶液混合,若Na2CO3溶液的濃度為2.0×10-4 mol/L,則生成沉淀所需CaCl2溶液的物質的量濃度最小是______________。
(5)某學生用石灰石為原料,設計了另一種制備碳酸鈣的實驗方案,其流程圖如下:

與前一方案相比較,該方案的優點是_________________________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com