
原電池中, B極逐漸變粗,A極逐漸變細,C為電解質溶液,則A、B、C應是下列各組中的( )
A.A是Zn,B是Cu,C為稀硫酸
B.A是Cu,B是Zn,C為稀硫酸
C.A是Fe,B是Ag,C為稀AgNO3溶液
D.A是Ag,B是Fe,C為稀AgNO3溶液
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源:2015-2016學年吉林省高一下學期期末化學試卷(解析版) 題型:填空題
根據下列敘述,畫出對應微粒結構示意圖:
(1)A元素原子的最外層電子數為電子層數的3倍: 。
(2)與Ar原子電子層結構相同的-1價陰離子: 。
(3)質量數為23,中子數為12的原子 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高一下學期期末化學試卷(解析版) 題型:選擇題
蔬菜、水果中富含纖維素,纖維素被食入人體后在作用是
A.為人體內的化學反應提供原料
B.為維持人體生命活動提供能量
C.加強胃腸蠕動,具有通便功能
D.人體中沒有水解纖維素的酶,所以纖維素在人體中沒有任何作用
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高一下學期期末化學試卷(解析版) 題型:選擇題
2010年5月2日,某煤礦發生瓦斯爆炸事故,造成多人傷亡,因此在礦井里,必須采取安全措施,如通風、嚴禁煙火等,而且要隨時檢查瓦斯的體積分數,如果空氣中含甲烷5%~15.4%,遇明火會發生爆炸。發生最強烈爆炸時空氣中甲烷所占的體積分數是( )
A.5%
B.9.1%
C.10.5%
D.15.4%
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高二下學期期末化學試卷(解析版) 題型:填空題
不同元素的原子電負性不同,若用x值來表示,x值越大,其原子的電負性就越大,吸引電子的能力越強,在所形成的分子中成為帶負電荷的一方,下面是某些短周期元素的電負性的值:
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA
第二周期 Li Be B C N O F
電負性值 0.98 1.57 2.04 2.55 3.44 3.98
第三周期 Na Mg Al Si P S Cl
電負性值 0.93 1.61 1.90 2.19 2.58 3.16
(1)通過分析x值的變化規律,確定Mg、N的x值的范圍: <x(Mg)< ,
<x(Mg)< 。
(2)推測x值與原子半徑的關系是 .根據短周期元素x值變化特點,體現了元素性質的
變化規律.
(3)某有機物結構簡式如圖,其中C﹣N中,你認為共用電子對偏向 原子(填原子名稱).
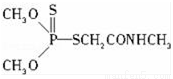
(4)經驗規律告訴我們,當成鍵的兩原子的x差值,即△x>1.7時,一般為離子鍵,當△x<1.7時,一般為共價鍵.試推斷AlBr3中化學鍵的類型為
(5)預測元素周期表中x值最小的元素是 (填元素符號,放射性元素除外).
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高二下學期期末化學試卷(解析版) 題型:選擇題
現有四種元素的基態原子的電子排布式如下:① 1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p5
則下列有關比較中正確的是
A.第一電離能:③>②>①
B.原子半徑:③>②>①
C.電負性:③>②>①
D.最高正化合價:③>②>①
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省高二下學期期末化學試卷(解析版) 題型:選擇題
已知某元素M原子的最外層電子排布式為nS1,,下列說法正確的是
A. M一定是金屬元素
B. M一定是S區元素
C. M的最高價是+1價
D. M可能呈現出﹣1價
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖北省黃岡市高二下期末化學試卷(解析版) 題型:推斷題
現有A、B、C、D、E五種元素,原子序數依次增大,且不超過36.A元素的基態原子最外層電子數是次外層的三倍;B元素的基態原子核外有13種不同運動狀態的電子;C與B同一周期,原子中未成對電子數是同周期中最多的;D2-的核外電子排布與氬原子相同;E元素的基態原子價電子排布式為3d104s1.請根據相關信息,回答下列問題:
(1)在A、B、C、D四種元素中第一電離能最小的是___________,電負性最大的是___________ (用相應的元素符號表示)
(2)寫出DA2的水化物在水中的電離方程式___________.DA3是___________分子(填“極性”或“非極性”)
(3)A、C的簡單氫化物中,哪種物質的沸點高,原因是什么? ___________________________
(4)若[E(NH3)4]2+具有對稱的空間構型,且當[E(NH3)4]2+中的兩個NH3分子被兩個Cl-取代時,能得到兩種不同結構的產物,則[E(NH3)4]2+的空間構型為_________ (填序號)
a.正四面體 b.平面正方形 c.三角錐形 d.V形
(5)單質E晶胞如圖所示,已知E元素相對原子質量為M,原子半徑為a pm,密度為dg·cm-3(1pm=10-10cm)寫出阿伏加德羅常數NA的表達式___________.(用M、a、d表示)
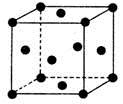
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com