(2012?崇明縣二模)下表為元素周期表的一部分,請參照元素①-⑧在表中的位置,用化學用語回答下列問題:
| 族周期 |
IA |
|
|
|
|
|
|
0 |
| 1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
|
|
|
② |
③ |
④ |
|
|
| 3 |
⑤ |
|
⑥ |
|
⑦ |
|
⑧ |
|
(1)④、⑤、⑥的原子半徑由大到小的順序為
Na>Al>O
Na>Al>O
(填元素符號).
②、⑦、⑧的最高價含氧酸的酸性由強到弱的順序是
HClO4>H3PO4>H2CO3
HClO4>H3PO4>H2CO3
(填化學式).
(2)①、④、⑤、⑧四種元素中,某些元素間可形成既含離子鍵又含極性共價鍵的化合物,寫出其中一種化合物的電子式:
.
(3)由表中兩種元素的原子按1:1組成的常見液態化合物的稀液易被催化分解,可使用的催化劑為(填序號)
A
A
.
A.MnO
2 B.Na
2SO
4 C.Na
2SO
3 D.CaCO
3(4)由表中元素形成的物質X、Y、Z、M、N可發生以下反應:
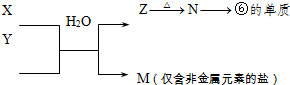
X溶液與Y溶液反應的離子方程式為
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
;
常溫下,為使0.1mol/L M溶液中電離出的陰、陽離子濃度相等,應向溶液中加入一定量的Y溶液至pH=
7
7
.




 ,故答案為:
,故答案為: 等;
等;
