
【題目】人體血液的正常pH約為7.35~7.45,若在外界因素作用下突然發生改變就會引起“酸中毒”或“堿中毒”,甚至有生命危險。由于人體體液的緩沖系統中存在如下平衡:
H++HCO3-![]() H2CO3
H2CO3![]() CO2+H2O
CO2+H2O
H++PO43-![]() HPO42-
HPO42-
H++HPO42-![]() H2PO4-
H2PO4-
故能維持血液pH的相對穩定,以保證正常生理活動。下列說法中不合理的是
A.當強酸性物質進入人體的體液后,上述緩沖系統的平衡向右移,從而維持pH穩定
B.當強堿性物質進入人體的體液后,上述緩沖系統的平衡向左移,從而維持pH穩定
C.某病人在靜脈滴注的大量生理鹽水后,血液被稀釋,會導致c(H+)顯著減少,pH值顯著增大,可能會引起堿中毒
D.在人體進行呼吸活動時,如CO2進入血液,會使平衡向左移動,c(H+)增大,pH值略減小
 激活思維優加課堂系列答案
激活思維優加課堂系列答案 活力試卷系列答案
活力試卷系列答案科目:高中化學 來源: 題型:
【題目】制取氯化鐵粉末,已知氯化鐵粉末很容易吸水生成結晶化合物FeCl3+6H2O===FeCl3·6H2O。
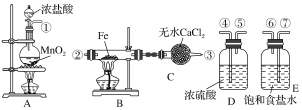
(1)按照氣體流向從左到右順序連接儀器應是(填儀器接口順序):
①接_______________________________________________________
(2)燒瓶A發生的反應中,氧化劑是________(填物質名稱),B中反應的化學方程式是___________________。
(3)容器D的作用是_____________________________________________,容器E的作用是__________________________________________________。
(4)A、B中的酒精燈應先點燃________處(填“A”或“B”)的酒精燈,理由是___________________。
(5)這套實驗裝置是否完整?________(填“是”或“否”),若不完整,還須補充________裝置(若第一問填“是”,則此問不需要作答)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】純堿是生活中常用的去油污洗滌劑。某同學欲用碳酸鈉晶體(Na2CO310H2O)配制100mL1molL-1的純堿溶液。請回答下列問題:
(1)計算所需要Na2CO310H2O的質量為________g;
(2)取該溶液20mL稀釋到100mL后的溶液中c(Na+)為_______molL-1。
(3)完成上述實驗,除下圖所示的儀器外,還需要添加的玻璃儀器是__________________________。
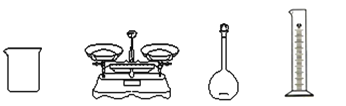
(4)配制溶液時,下列實驗操作會使配制溶液濃度偏低的是__________。
A.容量瓶內有水,未經過干燥處理
B.定容操作時,俯視刻度線
C.向容量瓶中轉移時有少量液體濺出
D.定容后倒轉容量瓶幾次,發現液面最低點低于刻度線,再補加幾滴水到刻度線
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電子工業中,常用FeCl3溶液腐蝕絕緣板上的銅箔,制造印刷電路板。某同學為了從腐蝕廢液中回收銅,并重新獲得FeCl3溶液,設計如下流程圖
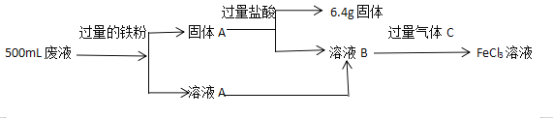
請回答下列問題:
(1)FeCl3溶液腐蝕銅箔反應的離子方程式為___________。
(2)固體A的成分是_______,氣體C的化學式為____________。
(3)設計實驗方案證明FeCl3溶液中的金屬陽離子_____________。
(4)反應消耗鐵粉11.2g,則廢液中Fe3+的物質的量濃度是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家發現對冶金硅進行電解精煉提純可降低高純硅制備成本。相關電解槽裝置如圖所示,用Cu-Si合金作硅源,在950℃利用三層液熔鹽進行電解精煉,有關說法不正確的是
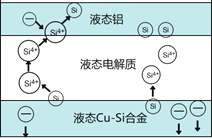
A. 在該液相熔體中Cu優先于Si被氧化,Si4+優先于Cu2+被還原
B. 電子由液態Cu-Si合金流出,從液態鋁流入
C. 三層液熔鹽的作用是增大電解反應面積,提高硅沉積效率
D. 電流強度不同,會影響硅提純速率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】云陽龍缸云端廊橋曾被詟為“世界第一懸挑玻璃景觀廊橋”,所用鋼化玻璃因其優良的性能廣泛應用于日常生活,但由于制作玻璃時里面含有極少量硫化鎳,使得鋼化玻璃在極限條件下的使用受到限制.
(1)基態硫原子價層電子的軌道表達式(電子排布圖)為____________,基態鎳原子中核外電子占據最高能層的符號為_____________.
(2)Ni(CO)4常用于制備純鎳,溶于乙醇、CCl4、苯等有機溶劑,為___________晶體,Ni(CO)4空間構型與甲烷相同,中心原子的雜化軌道類型為___________,寫出與配體互為等電子體的陰離子__________________________________________________________(任寫一種).
(3)與硫同族的硒元素有兩種常見的二元含氧酸,請比較它們酸性強弱 > (填化學式)______,理由是_______________________________________________________________.
(4)H2S的鍵角__________(填“大于”“小于””等于”)H2O的鍵角,請從電負性的角度說明理由___________________________________________________.
(5)NiO與NaCl的晶胞結構相似,如圖所示,陰離子采取面心立方堆積,陽離子填充在位于陰離子構成的空隙中,已知Ni2+半徑為69nm,O2-半徑為140nm,阿伏伽德羅常數為NA,NiO晶體的密度為_________g/cm3(只列出計算式).

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于常見有機物的說法不正確的是
A. 乙醇與乙酸都可以與鈉反應
B. 油脂是油和脂肪的統稱,都是高級脂肪酸與甘油形成的酯
C. 1mol有機物 一定條件下能和6molNaOH反應
一定條件下能和6molNaOH反應
D. 分于式為C4H7ClO2,可與NaHCO3溶液反應產生CO2的有機物可能結構有6種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定質量的鎂銅合金加入到稀硝酸中,兩者恰好完全反應,假設反應過程中還原產物全是NO,向所得溶液中加入物質的量濃度為3 mol·L-1 NaOH溶液至沉淀完全,測得生成沉淀的質量比原合金的質量增加5.1 g,則下列有關敘述中正確的是( )
A. 加入合金的質量不可能為6.4 g
B. 參加反應的硝酸的物質的量為0.1 mol
C. 沉淀完全時消耗NaOH溶液的體積為150 mL
D. 溶解合金時收集到NO氣體的體積在標準狀況下為2.24 L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某微粒的核外電子排布式為1s22s22p63s23p6,下列關于該微粒的說法正確的是( )
A.它的質子數一定是18
B.它的原子和37Cl可能互為同位數
C.它的單質一定是強還原劑
D.可以確定該微粒為Ar
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com