(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示
可逆反應進行的程度越大
可逆反應進行的程度越大
;K值大小與溫度的關系是:溫度升高,K值
可能增大也可能減小
可能增大也可能減小
(填“一定增大”、“一定減小”、或“可能增大也可能減小”).
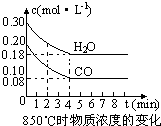
(2)在一體積為10L的容器中,通入一定量的CO和H
2O,在850℃時發生如下反應:CO(g)+H
2O(g)?CO
2(g)+H
2 (g)△H<0 CO和H
2O濃度變化如右圖,則 0-4min的平均反應速率v(CO)=
0.03mol/(L?min)
0.03mol/(L?min)
,該溫度下平衡常數K的數值為
1
1
.
(3)t
1℃(t
1>850℃)時,在相同容器中發生上述反應,容器內各物質的濃度變化如右表.
①表中3min-4min之間反應處于
平衡
平衡
狀態; c
1數值
大于
大于
0.08mol/L (填大于、小于或等于).
②反應在4min-5min間,平衡向逆方向移動,可能的原因是
d
d
(單選),表中5min-6min之間數值發生變化,可能的原因是
a
a
(單選).a.增加水蒸氣 b.降低溫度 c.使用催化劑 d.增加氫氣濃度
| 時間(min) |
CO |
H2O |
CO2 |
H2 |
| 0 |
0.200 |
0.300 |
0 |
0 |
| 2 |
0.138 |
0.238 |
0.062 |
0.062 |
| 3 |
c1 |
c2 |
c3 |
c3 |
| 4 |
c1 |
c2 |
c3 |
c3 |
| 5 |
0.116 |
0.216 |
0.084 |
|
| 6 |
0.096 |
0.266 |
0.104 |
|

 (1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示
(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示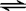 CO2(g)十H2 (g)
CO2(g)十H2 (g)

 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案 (1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示
(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示 (1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示
(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示 (1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示
(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示