
| |||||||||||||||||||||||||||
(1) |
答案:D 解析:CuCl2與CuSO4溶液中均含有Cu2+,但CuSO4溶液不與鋁片反應.故鋁片與CuCl2溶液的反應一定是Cl-起到了破壞鋁表面氧化物薄膜的作用. CuCl2中的Cl-破壞掉氧化膜以后,Al能置換出CuCl2溶液中的Cu而使鋁片表面呈暗紅色,反應方程式為:2Al+3Cu2+ 因此設法除去鋁表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使鋁片與CuSO4溶液發生反應. |
(2) |
答案:Cu 解析:CuCl2與CuSO4溶液中均含有Cu2+,但CuSO4溶液不與鋁片反應.故鋁片與CuCl2溶液的反應一定是Cl-起到了破壞鋁表面氧化物薄膜的作用. CuCl2中的Cl-破壞掉氧化膜以后,Al能置換出CuCl2溶液中的Cu而使鋁片表面呈暗紅色,反應方程式為:2Al+3Cu2+ 因此設法除去鋁表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使鋁片與CuSO4溶液發生反應. |
(3) |
答案:H2 ①隨著反應的進行生成鋁離子濃度增大,水解程度增大,產生H+的濃度增大,②該反應放熱,升高溫度反應加快,③銅與鋁構成原電池,加快鋁溶解 解析:CuCl2與CuSO4溶液中均含有Cu2+,但CuSO4溶液不與鋁片反應.故鋁片與CuCl2溶液的反應一定是Cl-起到了破壞鋁表面氧化物薄膜的作用. CuCl2中的Cl-破壞掉氧化膜以后,Al能置換出CuCl2溶液中的Cu而使鋁片表面呈暗紅色,反應方程式為:2Al+3Cu2+ 因此設法除去鋁表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使鋁片與CuSO4溶液發生反應. |
(4) |
CuCl2與CuSO4溶液中均含有Cu2+,但CuSO4溶液不與鋁片反應.故鋁片與CuCl2溶液的反應一定是Cl-起到了破壞鋁表面氧化物薄膜的作用. CuCl2中的Cl-破壞掉氧化膜以后,Al能置換出CuCl2溶液中的Cu而使鋁片表面呈暗紅色,反應方程式為:2Al+3Cu2+ 因此設法除去鋁表面的氧化物薄膜,或者往CuSO4溶液中加入Cl-均可使鋁片與CuSO4溶液發生反應. |


 千里馬走向假期期末仿真試卷寒假系列答案
千里馬走向假期期末仿真試卷寒假系列答案科目:高中化學 來源: 題型:
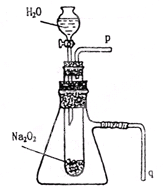 用脫脂棉花包住約0.2g過氧化鈉粉末,置于石棉網上,往脫脂棉上滴水,可觀察到脫脂棉劇烈燃燒起來.
用脫脂棉花包住約0.2g過氧化鈉粉末,置于石棉網上,往脫脂棉上滴水,可觀察到脫脂棉劇烈燃燒起來.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
| 選項 | 鋁電極 | 電解質 | 負極反應 | 正極反應 |
| A | 負極 | NaOH | 2Al-6e-+8OH-=2AlO2-+4H2O | 6H2O+6e-=6OH-+3H2↑ |
| B | 負極 | 稀鹽酸 | 2Al-6e-=2Al3+ | 6H++6e-=3H2↑ |
| C | 正極 | 濃硝酸 | Mg+2e-=Mg2+ | 2NO3-+4H+-4e-=2NO2↑+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 Ⅰ.某學校研究性學習小組開展“不同條件對化學反應速率影響的探究”課題,選用4mL 0.01mol?L-1KMnO4溶液與2mL 0.1mol?L-1 H2C2O4溶液進行實驗,改變條件如下:
Ⅰ.某學校研究性學習小組開展“不同條件對化學反應速率影響的探究”課題,選用4mL 0.01mol?L-1KMnO4溶液與2mL 0.1mol?L-1 H2C2O4溶液進行實驗,改變條件如下:| 組別 | 10%硫酸的體積(mL) | 溫度/℃ | 其他物質 |
| Ⅰ | 2mL | 20 | |
| Ⅱ | 2mL | 20 | 10滴飽和MnSO4溶液 |
| Ⅲ | 2mL | 30 | |
| Ⅳ | 1mL | 20 | 1mL蒸餾水 |
查看答案和解析>>
科目:高中化學 來源: 題型:
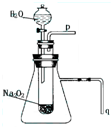 有演示實驗:用脫脂棉花包住約0.2g過氧化鈉粉末,置于石棉網上,往脫脂棉上滴水,可觀察到脫脂棉劇烈燃燒起來.
有演示實驗:用脫脂棉花包住約0.2g過氧化鈉粉末,置于石棉網上,往脫脂棉上滴水,可觀察到脫脂棉劇烈燃燒起來.查看答案和解析>>
科目:高中化學 來源: 題型:
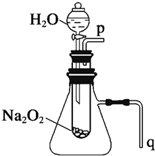 用脫脂棉花包住約0.2g過氧化鈉粉末,置于石棉網上,往脫脂棉上滴水,可觀察到脫脂棉劇烈燃燒起來.
用脫脂棉花包住約0.2g過氧化鈉粉末,置于石棉網上,往脫脂棉上滴水,可觀察到脫脂棉劇烈燃燒起來.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com